2,2-Diméthylbutane - 2,2-Dimethylbutane
|
|||
|
|
|||
| Des noms | |||
|---|---|---|---|
|
Nom IUPAC préféré
2,2-Diméthylbutane |
|||
| Autres noms
Néohexane, 22DMB
|
|||
| Identifiants | |||
|
Modèle 3D ( JSmol )
|
|||
| 1730736 | |||
| ChEMBL | |||
| ChemSpider | |||
| Carte d'information de l'ECHA |
100.000.825 |
||
| Numéro CE | |||
|
CID PubChem
|
|||
| Numéro RTECS | |||
| UNII | |||
| Numéro ONU | 1208 | ||
|
Tableau de bord CompTox ( EPA )
|
|||
|
|||
|
|||
| Propriétés | |||
| C 6 H 14 | |||
| Masse molaire | 86,178 g·mol -1 | ||
| Apparence | Liquide incolore | ||
| Odeur | Inodore | ||
| Densité | 649 mg ml -1 | ||
| Point de fusion | -102 à -98 °C ; -152 à -145 °F; 171 à 175 K | ||
| Point d'ébullition | 49,7 à 49,9 °C ; 121,4 à 121,7 °F ; 322,8 à 323,0 K | ||
| log P | 3,51 | ||
| La pression de vapeur | 36,88 kPa (à 20 °C) | ||
|
Constante de la loi de Henry ( k H ) |
6,5 nmol Pa -1 kg -1 | ||
| -76,24·10 -6 cm 3 /mol | |||
|
Indice de réfraction ( n D )
|
1,369 | ||
| Thermochimie | |||
|
Capacité calorifique ( C )
|
189,67 JK -1 mol -1 | ||
|
Entropie molaire standard ( S |
272,00 JK -1 mol -1 | ||
|
Std enthalpie de
formation (Δ f H ⦵ 298 ) |
−214,4–−212,4 kJ mol −1 | ||
|
Std enthalpie de
combustion (Δ c H ⦵ 298 ) |
−4.1494–−4.1476 MJ mol −1 | ||
| Dangers | |||
| Pictogrammes SGH |
   
|
||
| Mention d'avertissement SGH | Danger | ||
| H225 , H304 , H315 , H336 , H411 | |||
| P210 , P261 , P273 , P301+310 , P331 | |||
| NFPA 704 (diamant de feu) | |||
| point de rupture | −29 °C (−20 °F; 244 K) | ||
| 425 °C (797 °F; 698 K) | |||
| Limites d'explosivité | 1,2-7,7% | ||
| NIOSH (limites d'exposition pour la santé aux États-Unis) : | |||
|
PEL (Autorisé)
|
rien | ||
| Composés apparentés | |||
|
Alcanes apparentés
|
|||
|
Sauf indication contraire, les données sont données pour les matériaux dans leur état standard (à 25 °C [77 °F], 100 kPa). |
|||
|
|
|||
| Références de l'infobox | |||
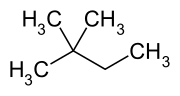
Le 2,2-diméthylbutane , appelé trivialement néohexane , est un composé organique de formule C 6 H 14 ou (H 3 C-) 3 -C-CH 2 -CH 3 . Il s'agit donc d'un alcane , en effet le plus compact et le plus ramifié des isomères de l' hexane , le seul à avoir un carbone quaternaire et un squelette butane (C 4 ).
La synthèse
Le 2,2-diméthylbutane peut être synthétisé par hydroisomérisation du 2,3-diméthylbutane en utilisant un catalyseur acide.
Il peut également être synthétisé par isomérisation du n- pentane en présence d'un catalyseur contenant des combinaisons d'un ou plusieurs du palladium, du platine, du rhodium et du rhénium sur une matrice de zéolite, d'alumine, de dioxyde de silicium ou d'autres matériaux. De telles réactions créent un mélange de produits finaux comprenant l'isopentane, le n- hexane, le 3-méthylpentane, le 2-méthylpentane, le 2,3-diméthylbutane et le 2,2-diméthylbutane. Etant donné que la composition du mélange final dépend de la température, le composant final souhaité peut être obtenu par le choix du catalyseur et par des combinaisons de contrôle de température et de distillations.
Les usages
Le néohexane est utilisé comme additif dans les carburants et dans la fabrication de produits chimiques agricoles. Il est également utilisé dans un certain nombre de produits d'entretien commerciaux, automobiles et domestiques, tels que les adhésifs, les nettoyants pour contacts électroniques et les sprays de polissage pour meubles rembourrés.
En laboratoire, il est couramment utilisé comme molécule sonde dans les techniques qui étudient les sites actifs des catalyseurs métalliques. De tels catalyseurs sont utilisés dans les réactions d'échange hydrogène-deutérium, d'hydrogénolyse et d'isomérisation. Il est bien adapté à cette fin car le 2,2-diméthylbutane contient à la fois un groupe isobutyle et un groupe éthyle.
Voir également
- Méthylbutane (isopentane)
- 2-Méthylpentane (isohexane)



