Chaîne de désintégration - Decay chain
| Physique nucléaire |
|---|
 |
| Nucleus · nucléons ( p , n ) · matière nucléaire · force nucléaire · Structure nucléaire · Réaction nucléaire |
|
Isotopes - égales Z
isobares - égalité A isotones - égaux N Isodiaphers - égale N - Z Isomères - l' égalité ci - dessus tous les noyaux Miroir - Z ↔ N Stable · magie · pair / impair · Halo ( bo ) |
|
Stabilité nucléaire
|
|
Processus à haute énergie
|
|
Processus de fusion nucléaire : Stellaire · Big Bang · Nucléides de supernova : Primordial · Cosmogénique · Artificiel |
|
Alvarez · Becquerel · Bethe · A. Bohr · N. Bohr · Chadwick · Cockcroft · Ir. Curie · Fr. Curie · Pi. Curie · Skłodowska-Curie · Davisson · Fermi · Hahn · Jensen · Lawrence · Mayer · Meitner · Oliphant · Oppenheimer · Proca · Purcell · Rabi · Rutherford · Soddy · Strassmann · Świątecki · Szilárd · Teller · Thomson · Walton · Wigner
|
En science nucléaire , la chaîne de désintégration fait référence à une série de désintégrations radioactives de différents produits de désintégration radioactive sous la forme d'une série séquentielle de transformations. Elle est également connue sous le nom de «cascade radioactive». La plupart des radio - isotopes ne se désintègrent pas directement à un état stable, mais subissent plutôt une série de désintégrations jusqu'à ce qu'un isotope stable soit finalement atteint.
Les étapes de désintégration sont désignées par leur relation avec les étapes précédentes ou suivantes. Un isotope parent est un isotope qui subit une désintégration pour former un isotope fille . Un exemple de ceci est la décomposition de l'uranium (numéro atomique 92) en thorium (numéro atomique 90). L'isotope fille peut être stable ou il peut se désintégrer pour former un isotope fille qui lui est propre. La fille d'un isotope fille est parfois appelée isotope petite - fille .
Le temps qu'il faut à un atome parent unique pour se désintégrer en un atome de son isotope fille peut varier considérablement, non seulement entre différentes paires parent-fille, mais aussi de manière aléatoire entre des appariements identiques d'isotopes parent et fille. La désintégration de chaque atome se produit spontanément et la désintégration d'une population initiale d'atomes identiques au cours du temps t suit une distribution exponentielle décroissante, e −λt , où λ est appelée constante de désintégration . L'une des propriétés d'un isotope est sa demi-vie , le temps pendant lequel la moitié d'un nombre initial de radio-isotopes parents identiques s'est désintégrée en leurs filles, qui est inversement proportionnelle à λ. Les demi-vies ont été déterminées en laboratoire pour de nombreux radio-isotopes (ou radionucléides). Celles-ci peuvent aller de presque instantanées (moins de 10 à 21 secondes) à plus de 10 à 19 ans.
Les étages intermédiaires émettent chacun la même quantité de radioactivité que le radio-isotope d'origine (c'est-à-dire qu'il existe une relation biunivoque entre les nombres de désintégrations dans les étapes successives) mais chaque étage libère une quantité d'énergie différente. Si et quand l'équilibre est atteint, chaque isotope fille successif est présent en proportion directe de sa demi-vie; mais comme son activité est inversement proportionnelle à sa demi-vie, chaque nucléide de la chaîne de désintégration contribue finalement autant de transformations individuelles que la tête de chaîne, mais pas la même énergie. Par exemple, l'uranium-238 est faiblement radioactif, mais la pitchblende , un minerai d'uranium, est 13 fois plus radioactif que l'uranium pur à cause du radium et des autres isotopes filles qu'il contient. Non seulement les isotopes instables du radium sont des émetteurs de radioactivité importants, mais en tant qu'étape suivante de la chaîne de désintégration, ils génèrent également du radon , un gaz radioactif naturel, lourd et inerte. Les roches contenant du thorium et / ou de l'uranium (comme certains granites) émettent du radon qui peut s'accumuler dans des endroits clos tels que des sous-sols ou des mines souterraines.
La quantité d'isotopes dans les chaînes de désintégration à un certain moment est calculée avec l' équation de Bateman .
Histoire
Tous les éléments et isotopes trouvés sur Terre, à l'exception de l'hydrogène, du deutérium, de l'hélium, de l'hélium-3 et peut-être des traces d'isotopes stables de lithium et de béryllium qui ont été créés dans le Big Bang , ont été créés par le processus s ou le Le processus r dans les étoiles, et pour que celles-ci fassent aujourd'hui partie de la Terre, doit avoir été créé il y a au plus 4,5 milliards d'années . Tous les éléments créés il y a plus de 4,5 milliards d'années sont appelés primordiaux , ce qui signifie qu'ils ont été générés par les processus stellaires de l'univers. Au moment de leur création, ceux qui étaient instables ont commencé à se décomposer immédiatement. Tous les isotopes dont la demi-vie est inférieure à 100 millions d'années ont été réduits à2,8 × 10 −12 % ou moins des quantités originales créées et capturées par l'accrétion de la Terre; ils sont aujourd'hui peu nombreux ou se sont complètement désintégrés. Il n'y a que deux autres méthodes pour créer des isotopes: artificiellement , à l'intérieur d'un réacteur artificiel (ou peut-être naturel ), ou par désintégration d'une espèce isotopique parente, le processus connu sous le nom de chaîne de désintégration .
Les isotopes instables se désintègrent en produits filles (qui peuvent parfois être encore plus instables) à une vitesse donnée; finalement, souvent après une série de désintégrations, un isotope stable est atteint: il y a environ 200 isotopes stables dans l'univers. Dans les isotopes stables, les éléments légers ont généralement un rapport neutrons / protons dans leur noyau plus faible que les éléments plus lourds. Les éléments légers tels que l' hélium-4 ont un rapport neutron: proton proche de 1: 1. Les éléments les plus lourds comme le plomb ont près de 1,5 neutrons par proton (par exemple 1,536 dans le plomb-208 ). Aucun nucléide plus lourd que le plomb-208 n'est stable; ces éléments plus lourds doivent perdre de la masse pour atteindre la stabilité, le plus souvent sous forme de désintégration alpha . L'autre méthode de désintégration commune pour les isotopes avec un rapport neutron / proton élevé (n / p) est la désintégration bêta , dans laquelle le nucléide change d'identité élémentaire tout en gardant la même masse et en abaissant son rapport n / p. Pour certains isotopes avec un rapport n / p relativement faible, il y a une désintégration bêta inverse , par laquelle un proton est transformé en neutron, se déplaçant ainsi vers un isotope stable; cependant, comme la fission produit presque toujours des produits lourds en neutrons, l'émission de positons est relativement rare par rapport à l'émission d'électrons. Il existe de nombreuses chaînes de désintégration bêta relativement courtes, au moins deux (une désintégration bêta lourde et une désintégration légère en positons ) pour chaque poids discret jusqu'à environ 207 et certains au-delà, mais pour les éléments de masse plus élevés (isotopes plus lourds que le plomb) sont seulement quatre voies qui englobent toutes les chaînes de désintégration. En effet, il n'y a que deux méthodes de désintégration principales: le rayonnement alpha , qui réduit la masse de 4 unités de masse atomique (amu), et bêta, qui ne change pas du tout la masse atomique (juste le numéro atomique et le rapport p / n ). Les quatre chemins sont appelés 4n, 4n + 1, 4n + 2 et 4n + 3; le reste de la division de la masse atomique par quatre donne la chaîne que l'isotope utilisera pour se désintégrer. Il existe d'autres modes de désintégration, mais ils se produisent invariablement à une probabilité plus faible que la désintégration alpha ou bêta. (Il ne faut pas supposer que ces chaînes n'ont pas de branches: le diagramme ci-dessous montre quelques branches de chaînes, et en réalité il y en a beaucoup plus, car il y a beaucoup plus d'isotopes possibles que ce qui est montré dans le diagramme.) Par exemple, le le troisième atome de nihonium-278 synthétisé a subi six désintégrations alpha jusqu'au mendélévium-254 , suivis d'une capture d'électrons (une forme de désintégration bêta ) en fermium-254 , puis d'un septième alpha en californium-250 , sur lequel il aurait suivi la chaîne 4n + 2 comme indiqué dans cet article. Cependant, les nucléides super- lourds les plus lourds synthétisés n'atteignent pas les quatre chaînes de désintégration, car ils atteignent un nucléide en fission spontanée après quelques désintégrations alpha qui terminent la chaîne: c'est ce qui est arrivé aux deux premiers atomes de nihonium-278 synthétisés, ainsi que à tous les nucléides plus lourds produits.
Trois de ces chaînes ont un isotope (ou nucléide) à vie longue près du sommet; cet isotope à vie longue est un goulot d'étranglement dans le processus à travers lequel la chaîne s'écoule très lentement, et maintient la chaîne sous eux "vivante" avec l'écoulement. Les trois nucléides à vie longue sont l'uranium-238 (demi-vie = 4,5 milliards d'années), l'uranium-235 (demi-vie = 700 millions d'années) et le thorium-232 (demi-vie = 14 milliards d'années). La quatrième chaîne n'a pas d'isotope de goulot d'étranglement aussi durable, de sorte que presque tous les isotopes de cette chaîne se sont désintégrés depuis longtemps jusqu'à très près de la stabilité en bas. Près de la fin de cette chaîne se trouve le bismuth-209, qui a longtemps été considéré comme stable. Récemment, cependant, le bismuth-209 s'est avéré instable avec une demi-vie de 19 milliards de milliards d'années; c'est la dernière étape avant le thallium-205 stable. Dans un passé lointain, à l'époque de la formation du système solaire, il y avait plus de types d'isotopes instables de poids élevé disponibles, et les quatre chaînes étaient plus longues avec des isotopes qui se sont désintégrés depuis. Aujourd'hui, nous avons fabriqué des isotopes éteints, qui reprennent leurs anciennes places: le plutonium-239, le combustible de la bombe nucléaire, comme l'exemple majeur a une demi-vie de "seulement" 24 500 ans, et se désintègre par émission alpha en uranium-235. En particulier, grâce à la production à grande échelle de neptunium-237, nous avons réussi à ressusciter la quatrième chaîne jusqu'à présent éteinte. Les tableaux ci-dessous démarrent donc les quatre chaînes de désintégration aux isotopes du californium avec des nombres de masse de 249 à 252.
Types de désintégration
Les quatre modes les plus courants de la désintégration radioactive sont: la désintégration alpha , désintégration bêta , la désintégration bêta inverse (considéré à la fois comme émission de positons et capture d'électrons ), et la transition isomérique . Parmi ces processus de désintégration, seule la désintégration alpha modifie le nombre de masse atomique ( A ) du noyau et le diminue toujours de quatre. Pour cette raison, presque toute désintégration se traduira par un noyau dont le numéro de masse atomique a le même résidu mod 4, divisant tous les nucléides en quatre chaînes. Les membres de toute chaîne de désintégration possible doivent être entièrement tirés de l'une de ces classes. Les quatre chaînes produisent également de l' hélium-4 (les particules alpha sont des noyaux d'hélium-4).
Trois chaînes de désintégration principales (ou familles) sont observées dans la nature, communément appelées série thorium, série radium ou uranium et série actinium , représentant trois de ces quatre classes et se terminant par trois isotopes stables et différents du plomb . Le nombre de masse de chaque isotope dans ces chaînes peut être représenté par A = 4 n , A = 4 n + 2 et A = 4 n + 3, respectivement. Les isotopes de départ à vie longue de ces trois isotopes, respectivement le thorium-232 , l' uranium-238 et l' uranium-235 , existent depuis la formation de la terre, ignorant les isotopes artificiels et leurs désintégrations depuis les années 1940.
En raison de la demi-vie relativement courte de son isotope de départ neptunium-237 (2,14 millions d'années), la quatrième chaîne, la série du neptunium avec A = 4 n + 1, est déjà éteinte dans la nature, à l'exception de l'étape finale de limitation de la vitesse , désintégration du bismuth-209 . Cependant, des traces de 237 Np et de ses produits de désintégration se produisent encore dans la nature en raison de la capture de neutrons dans le minerai d'uranium. L'isotope de terminaison de cette chaîne est maintenant connu pour être le thallium-205 . Certaines sources plus anciennes donnent l'isotope final comme le bismuth-209, mais il a été récemment découvert qu'il est très légèrement radioactif, avec une demi-vie de2,01 × 10 19 ans .
Il existe également des chaînes de désintégration non transuraniennes d'isotopes instables d'éléments légers, par exemple celles du magnésium-28 et du chlore-39 . Sur Terre, la plupart des isotopes de départ de ces chaînes avant 1945 étaient générés par le rayonnement cosmique . Depuis 1945, les essais et l'utilisation d'armes nucléaires ont également libéré de nombreux produits de fission radioactifs . Presque tous ces isotopes se désintègrent selon les modes de désintégration β - ou β + , passant d'un élément à un autre sans changer de masse atomique. Ces derniers produits, étant plus proches de la stabilité, ont généralement des demi-vies plus longues jusqu'à ce qu'ils se désintègrent finalement en stabilité.
Chaînes de désintégration alpha des actinides
|
Actinides et produits de fission par demi-vie
|
||||||||
|---|---|---|---|---|---|---|---|---|
| Actinides par chaîne de désintégration |
Gamme de demi-vie ( y ) |
Produits de fission de 235 U par rendement | ||||||
| 4 n | 4 n +1 | 4 n +2 | 4 n +3 | |||||
| 4,5 à 7% | 0,04 à 1,25% | <0,001% | ||||||
| 228 Ra№ | 4–6 | † | 155 Euþ | |||||
| 244 cmƒ | 241 Puƒ | 250 Cf | 227 Ac№ | 10–29 | 90 Sr | 85 Kr | 113m Cdþ | |
| 232 Uƒ | 238 Puƒ | 243 cmƒ | 29–97 | 137 Cs | 151 Smþ | 121m Sn | ||
| 248 Bk | 249 Cfƒ | 242m Amƒ | 141–351 |
Aucun produit de fission |
||||
| 241 amƒ | 251 Cfƒ | 430 à 900 | ||||||
| 226 Ra№ | 247 Bk | 1,3 k à 1,6 k | ||||||
| 240 Pu | 229 ème | 246 cmƒ | 243 amƒ | 4,7 k à 7,4 k | ||||
| 245 cmƒ | 250 cm | 8,3 k à 8,5 k | ||||||
| 239 Puƒ | 24,1 km | |||||||
| 230 Th№ | 231 Pa№ | 32 k - 76 k | ||||||
| 236 Npƒ | 233 Uƒ | 234 U№ | 150 k à 250 k | ‡ | 99 Tc₡ | 126 Sn | ||
| 248 cm | 242 Pu | 327 k - 375 k | 79 Se₡ | |||||
| 1,53 M | 93 Zr | |||||||
| 237 Npƒ | 2,1 M - 6,5 M | 135 Cs₡ | 107 Pd | |||||
| 236 U | 247 cmƒ | 15 à 24 mois | 129 Je₡ | |||||
| 244 Pu | 80 millions |
... ni au-delà de 15,7 millions d'années |
||||||
| 232 Th№ | 238 U№ | 235 Uƒ№ | 0,7 G à 14,1 G | |||||
|
Légende des symboles en exposant |
||||||||
Dans les quatre tableaux ci-dessous, les branches mineures de désintégration (avec une probabilité de ramification inférieure à 0,0001%) sont omises. La libération d'énergie comprend l'énergie cinétique totale de toutes les particules émises ( électrons , particules alpha , quanta gamma , neutrinos , électrons Auger et rayons X ) et le noyau de recul, en supposant que le noyau d'origine était au repos. La lettre «a» représente une année (du latin annus ).
Dans les tableaux ci-dessous (sauf neptunium), les noms historiques des nucléides naturels sont également donnés. Ces noms ont été utilisés au moment où les chaînes de désintégration ont été découvertes et étudiées pour la première fois. A partir de ces noms historiques, on peut localiser la chaîne particulière à laquelle appartient le nucléide et la remplacer par son nom moderne.
Les trois chaînes de désintégration alpha de l'actinide d'origine naturelle indiquées ci-dessous - thorium, uranium / radium (à partir de l'U-238) et actinium (à partir de l'U-235) - se terminent chacune par son propre isotope de plomb et Pb-207 respectivement). Tous ces isotopes sont stables et sont également présents dans la nature sous forme de nucléides primordiaux , mais leurs excès par rapport au plomb-204 (qui n'a qu'une origine primordiale) peuvent être utilisés dans la technique de datation uranium-plomb aux roches dattes.
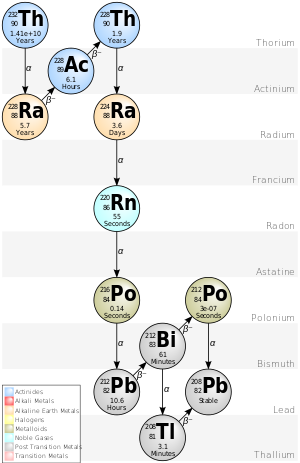
Série Thorium
La chaîne 4n de Th-232 est communément appelée «série de thorium» ou «cascade de thorium». À partir du thorium- 232 naturel , cette série comprend les éléments suivants: actinium , bismuth , plomb , polonium , radium , radon et thallium . Tous sont présents, au moins de manière transitoire, dans tout échantillon naturel contenant du thorium, qu'il soit métallique, composé ou minéral. La série se termine par le plomb-208.
L'énergie totale libérée du thorium-232 au plomb-208, y compris l'énergie perdue aux neutrinos , est de 42,6 MeV.
| nucléide | nom historique (court) | nom historique (long) | mode de désintégration | demi-vie ( a = année) |
énergie libérée, MeV | produit de la décomposition |
|---|---|---|---|---|---|---|
| 252 Cf | α | 2.645 un | 6.1181 | 248 cm | ||
| 248 cm | α | 3,4 × 10 5 a | 5,162 | 244 Pu | ||
| 244 Pu | α | 8 × 10 7 un | 4,589 | 240 U | ||
| 240 U | β - | 14,1 heures | .39 | 240 Np | ||
| 240 Np | β - | 1,032 h | 2.2 | 240 Pu | ||
| 240 Pu | α | 6561 a | 5.1683 | 236 U | ||
| 236 U | Thoruranium | α | 2,3 × 10 7 un | 4,494 | 232 ème | |
| 232 ème | Th | Thorium | α | 1,405 × 10 10 a | 4,081 | 228 Ra |
| 228 Ra | MsTh 1 | Mésothoire 1 | β - | 5.75 a | 0,046 | 228 Ac |
| 228 Ac | MsTh 2 | Mésothorium 2 | β - | 6,25 heures | 2.124 | 228 ème |
| 228 ème | RdTh | Radiothorium | α | 1.9116 un | 5,520 | 224 Ra |
| 224 Ra | THX | Thorium X | α | 3.6319 j | 5,789 | 220 Rn |
| 220 Rn | Tn | Thoron, émanation de thorium |
α | 55,6 s | 6,404 | 216 Po |
| 216 Po | ThA | Thorium A | α | 0,145 s | 6,906 | 212 Pb |
| 212 Pb | ThB | Thorium B | β - | 10,64 heures | 0,570 | 212 Bi |
| 212 Bi | ThC | Thorium C | β - 64,06% α 35,94% |
60,55 minutes | 2,252 6,208 |
212 Po 208 Tl |
| 212 Po | ThC ′ | Thorium C ′ | α | 299 ns | 8,784 | 208 Pb |
| 208 Tl | ThC ″ | Thorium C ″ | β - | 3,053 minutes | 1,803 | 208 Pb |
| 208 Pb | ThD | Thorium D | stable | . | . | . |
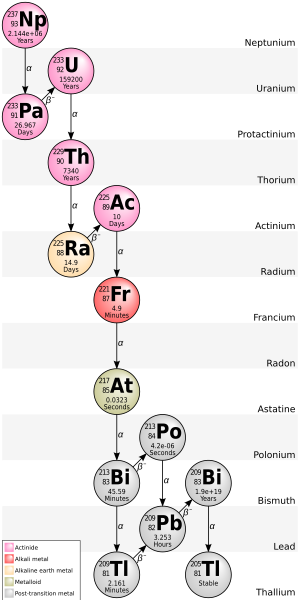
Série Neptunium
La chaîne 4n + 1 de 237 Np est communément appelée «série neptunium» ou «cascade neptunium». Dans cette série, seuls deux des isotopes impliqués se retrouvent naturellement en quantités significatives, à savoir les deux derniers: le bismuth-209 et le thallium-205 . Certains des autres isotopes ont été détectés dans la nature, provenant de traces de 237 Np produites par la réaction knock-out (n, 2n) dans le 238 U primordial.Un détecteur de fumée contenant une chambre d'ionisation à l' américium -241 accumule une quantité importante de neptunium - 237 à mesure que son américium se désintègre; les éléments suivants y sont également présents, au moins de manière transitoire, comme produits de désintégration du neptunium: actinium , astatine , bismuth, francium , plomb , polonium , protactinium , radium , thallium, thorium et uranium . Puisque cette série n'a été découverte et étudiée qu'en 1947–1948, ses nucléides n'ont pas de noms historiques. Un trait unique de cette chaîne de désintégration est que le radon, gaz rare, n'est produit que dans une branche rare et non dans la séquence de désintégration principale; ainsi, il ne migre pas à travers la roche autant que les trois autres chaînes de désintégration.
L'énergie totale libérée du californium-249 au thallium-205, y compris l'énergie perdue aux neutrinos , est de 66,8 MeV.
| nucléide | mode de désintégration | demi-vie ( a = année) |
énergie libérée, MeV | produit de la décomposition |
|---|---|---|---|---|
| 249 Cf | α | 351 un | 5,813 + 0,388 | 245 cm |
| 245 cm | α | 8500 un | 5,362 + 0,175 | 241 Pu |
| 241 Pu | β - | 14,4 un | 0,021 | 241 heures |
| 241 heures | α | 432,7 un | 5,638 | 237 Np |
| 237 Np | α | 2.14 · 10 6 a | 4,959 | 233 Pa |
| 233 Pa | β - | 27,0 j | 0,571 | 233 U |
| 233 U | α | 1,592 · 10 5 a | 4,909 | 229 ème |
| 229 ème | α | 7340 un | 5,168 | 225 Ra |
| 225 Ra | β - | 14,9 j | 0,36 | 225 Ac |
| 225 Ac | α | 10,0 j | 5,935 | 221 Fr |
| 221 Fr | α 99,9952% β - 0,0048% |
4,8 min | 6,3 0,314 |
217 à 221 Ra |
| 221 Ra | α | 28 s | 6,9 | 217 Rn |
| 217 À | α 99,992% β - 0,008% |
32 ms | 7,0 0,737 |
213 Bi 217 Rn |
| 217 Rn | α | 540 µs | 7,9 | 213 Po |
| 213 Bi | β - 97,80% α 2,20% |
46,5 minutes | 1,423 5,87 |
213 Po 209 Tl |
| 213 Po | α | 3,72 μs | 8,536 | 209 Pb |
| 209 Tl | β - | 2,2 min | 3,99 | 209 Pb |
| 209 Pb | β - | 3,25 heures | 0,644 | 209 Bi |
| 209 Bi | α | 1,9 · 10 19 a | 3,137 | 205 Tl |
| 205 Tl | . | stable | . | . |
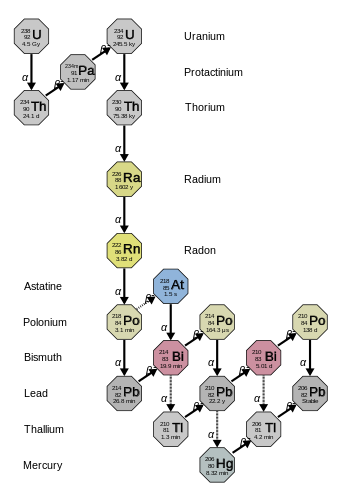
Série Uranium
La chaîne 4n + 2 de l'uranium-238 est appelée «série de l'uranium» ou «série du radium». En commençant par l' uranium 238 d'origine naturelle , cette série comprend les éléments suivants: astatine , bismuth , plomb , polonium , protactinium , radium , radon , thallium et thorium . Tous sont présents, au moins de façon transitoire, dans tout échantillon naturel contenant de l'uranium, qu'il soit métallique, composé ou minéral. La série se termine par le plomb-206.
L'énergie totale libérée de l'uranium-238 au plomb-206, y compris l'énergie perdue aux neutrinos , est de 51,7 MeV.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
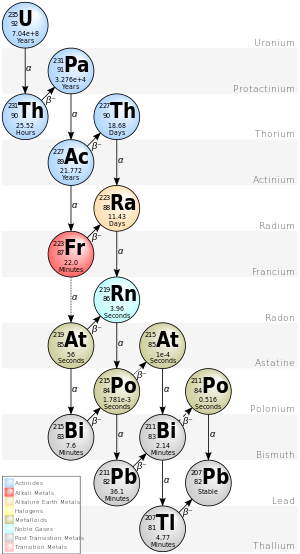
Série Actinium
La chaîne 4n + 3 de l' uranium 235 est communément appelée «série actinium» ou «cascade actinium». En commençant par l'isotope naturel U-235, cette série de désintégration comprend les éléments suivants: actinium , astatine , bismuth , francium , plomb , polonium , protactinium , radium , radon , thallium et thorium . Tous sont présents, au moins de manière transitoire, dans tout échantillon contenant de l'uranium 235, qu'il soit métallique, composé, minerai ou minéral. Cette série se termine par l'isotope stable plomb-207 .
L'énergie totale libérée de l'uranium 235 au plomb 207, y compris l'énergie perdue aux neutrinos , est de 46,4 MeV.
| nucléide | nom historique (court) | nom historique (long) | mode de désintégration | demi-vie ( a = année) |
énergie libérée, MeV | produit de la décomposition |
|---|---|---|---|---|---|---|
| 251 Cf | α | 900,6 un | 6,176 | 247 cm | ||
| 247 cm | α | 1,56 · 10 7 a | 5,353 | 243 Pu | ||
| 243 Pu | β - | 4,95556 heures | 0,579 | 243 heures | ||
| 243 heures | α | 7388 un | 5,439 | 239 Np | ||
| 239 Np | β - | 2,3565 j | 0,723 | 239 Pu | ||
| 239 Pu | α | 2,41 · 10 4 a | 5,244 | 235 U | ||
| 235 U | AcU | Actine Uranium | α | 7,04 · 10 8 a | 4,678 | 231 ème |
| 231 ème | UY | Uranium Y | β - | 25,52 heures | 0,391 | 231 Pa |
| 231 Pa | Pennsylvanie | Protactinium | α | 32760 a | 5,150 | 227 Ac |
| 227 Ac | Ac | Actinium | β - 98,62% α 1,38% |
21.772 a | 0,045 5,042 |
227 Th 223 Fr |
| 227 ème | RdAc | Radioactinium | α | 18,68 j | 6,147 | 223 Ra |
| 223 Fr | AcK | Actinium K | β - 99,994% α 0,006% |
22.00 min | 1,149 5,340 |
223 Ra 219 At |
| 223 Ra | AcX | Actinium X | α | 11,43 j | 5,979 | 219 Rn |
| 219 À | α 97,00% β - 3,00% |
56 s | 6,275 1,700 |
215 Bi 219 Rn |
||
| 219 Rn | Un | Actinon, émanation d'actinium |
α | 3,96 s | 6,946 | 215 Po |
| 215 Bi | β - | 7,6 min | 2,250 | 215 Po | ||
| 215 Po | AcA | Actinium A | α 99,99977% β - 0,00023% |
1,781 ms | 7,527 0,715 |
211 Pb 215 À |
| 215 À | α | 0,1 ms | 8,178 | 211 Bi | ||
| 211 Pb | AcB | Actinium B | β - | 36,1 minutes | 1,367 | 211 Bi |
| 211 Bi | AcC | Actinium C | α 99,724% β - 0,276% |
2,14 min | 6,751 0,575 |
207 Tl 211 Po |
| 211 Po | AcC ' | Actinium C ' | α | 516 ms | 7,595 | 207 Pb |
| 207 Tl | AcC " | Actinium C " | β - | 4,77 minutes | 1,418 | 207 Pb |
| 207 Pb | AcD | Actinium D | . | stable | . | . |
Voir également
- Physique nucléaire
- Désintégration radioactive
- Vallée de la stabilité
- Produit de désintégration
- Radio-isotopes ( radionucléide )
- Datation radiométrique
Remarques
Les références
- CM Lederer; JM Hollander; I. Perlman (1968). Table of Isotopes (6e éd.). New York: John Wiley & Sons .
Liens externes
- Portail des sciences nucléaires Nucleonica
- Decay Engine de Nucleonica pour des calculs de désintégration en ligne professionnels
- EPA - Désintégration radioactive
- Site Web du gouvernement répertoriant les isotopes et les énergies de désintégration
- Centre national de données nucléaires - bases de données disponibles gratuitement qui peuvent être utilisées pour vérifier ou construire des chaînes de désintégration
-
 IAEA - Graphique en direct des nucléides (avec chaînes de désintégration)
IAEA - Graphique en direct des nucléides (avec chaînes de désintégration) - Recherche de chaîne de désintégration