Zone active - Active zone
| Zone active | |
|---|---|
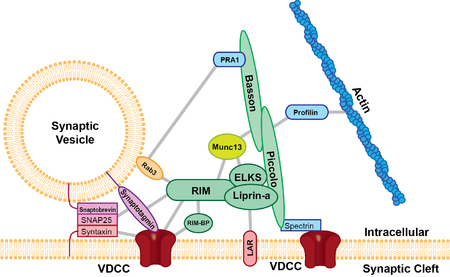
 Un diagramme d'une synapse typique du système nerveux central. Les protéines de la zone active sont représentées sous forme de pyramides brun foncé sur la terminaison neuronale supérieure
| |
| Des détails | |
| Identifiants | |
| Latin | zone active |
| E | H2.00.06.2.00012 |
|
Termes anatomiques de la microanatomie | |
La zone active ou zone active synaptique est un terme utilisé pour la première fois par Couteaux et Pecot-Dechavassinein en 1970 pour définir le site de libération des neurotransmetteurs . Deux neurones entrent en contact étroit à travers des structures appelées synapses leur permettant de communiquer entre eux. Comme le montre le diagramme adjacent, une synapse se compose du bouton présynaptique d'un neurone qui stocke des vésicules contenant le neurotransmetteur (en haut sur l'image) et d'un deuxième neurone postsynaptique qui porte des récepteurs pour le neurotransmetteur (en bas), ainsi qu'un espace entre les deux appelé la fente synaptique (avec des molécules d'adhésion synaptique, SAM, tenant les deux ensemble). Lorsqu'un potentiel d'action atteint le bouton présynaptique, le contenu des vésicules est libéré dans la fente synaptique et le neurotransmetteur libéré traverse la fente jusqu'au neurone postsynaptique (la structure inférieure sur l'image) et active les récepteurs sur la membrane postsynaptique.
La zone active est la région du bouton présynaptique qui médie la libération des neurotransmetteurs et est composée de la membrane présynaptique et d'une collection dense de protéines appelée cytomatrice au niveau de la zone active (CAZ). Le CAZ est vu au microscope électronique comme une zone sombre (dense en électrons) proche de la membrane. Les protéines au sein de la CAZ attachent les vésicules synaptiques à la membrane présynaptique et assurent la médiation de la fusion des vésicules synaptiques , permettant ainsi au neurotransmetteur d'être libéré de manière fiable et rapide lorsqu'un potentiel d'action arrive.
Une fonction
La fonction de la zone active est de garantir que les neurotransmetteurs peuvent être libérés de manière fiable dans un emplacement spécifique d'un neurone et uniquement libérés lorsque le neurone déclenche un potentiel d'action. Comme un potentiel d'action se propage vers le bas un axone il atteint la terminaison axonale appelé le présynaptique bouton. Dans le bouton présynaptique, le potentiel d'action active les canaux calciques (VDCC) qui provoquent un afflux local de calcium. L'augmentation du calcium est détectée par les protéines de la zone active et force les vésicules contenant le neurotransmetteur à fusionner avec la membrane. Cette fusion des vésicules avec la membrane libère les neurotransmetteurs dans la fente synaptique (espace entre le bouton présynaptique et la membrane postsynaptique). Les neurotransmetteurs diffusent ensuite à travers la fente et se lient aux canaux ioniques dépendants du ligand et aux récepteurs couplés aux protéines G sur la membrane postsynaptique. La liaison des neurotransmetteurs aux récepteurs postsynaptiques induit alors une modification du neurone postsynaptique. Le processus de libération de neurotransmetteurs et de liaison aux récepteurs postsynaptiques pour provoquer un changement dans le neurone postsynaptique est appelé neurotransmission.
Structure
La zone active est présente dans toutes les synapses chimiques examinées jusqu'à présent et est présente dans toutes les espèces animales. Les zones actives examinées jusqu'à présent ont au moins deux caractéristiques en commun, elles ont toutes un matériau dense en protéines qui fait saillie de la membrane et attache des vésicules synaptiques près de la membrane et elles ont de longues projections filamenteuses provenant de la membrane et se terminant à des vésicules légèrement plus éloignées de la membrane présynaptique. Les projections denses en protéines varient en taille et en forme selon le type de synapse examiné. Un exemple frappant de la projection dense est la synapse en ruban (voir ci-dessous) qui contient un "ruban" de matière dense en protéines qui est entouré d'un halo de vésicules synaptiques et s'étend perpendiculairement à la membrane présynaptique et peut atteindre 500 nm. La synapse du glutamate contient des structures pyramidales plus petites qui s'étendent à environ 50 nm de la membrane. La synapse neuromusculaire contient deux rangées de vésicules avec une longue bande protéique entre elles qui est reliée à des côtes horizontales régulièrement espacées s'étendant perpendiculairement à la bande et parallèlement à la membrane. Ces nervures sont ensuite reliées aux vésicules qui sont chacune positionnées au-dessus d'une cheville dans la membrane (vraisemblablement un canal calcique). Des recherches antérieures ont indiqué que la zone active des neurones glutamatergiques contenait un réseau très régulier de matériau dense en protéines en forme de pyramide et a indiqué que ces pyramides étaient reliées par des filaments. Cette structure ressemblait à un réseau géométrique où les vésicules étaient guidées dans les trous du réseau. Ce modèle attractif a été remis en cause par des expériences récentes. Des données récentes montrent que la zone active glutamatergique contient les projections de matière protéique dense, mais ces projections n'étaient pas dans un réseau régulier et contenaient de longs filaments projetant environ 80 nm dans le cytoplasme.
Il existe au moins cinq protéines d'échafaudage majeures qui sont enrichies dans la zone active ; UNC13B /Munc13, RIMS1 (molécule interagissant avec Rab3), Basson, Piccolo /aczonine, ELKS et liprines-α . On pense que ces protéines d'échafaudage sont les constituants des structures pyramidales denses de la zone active et qu'elles rapprochent les vésicules synaptiques de la membrane présynaptique et des canaux calciques. La protéine ELKS se lie à la protéine d' adhésion cellulaire , la -neurexine , et à d'autres protéines au sein du complexe telles que Piccolo et Basson. La -neurexine se lie alors à la molécule d'adhésion cellulaire, la neuroligine située sur la membrane postsynaptique. La neuroligine interagit alors avec des protéines qui se lient aux récepteurs postsynaptiques. Les interactions protéiques comme celle observée entre Piccolo/ELKS/β-neurexine/neuroligine garantissent que la machinerie qui médie la fusion des vésicules est à proximité immédiate des canaux calciques et que la fusion des vésicules est adjacente aux récepteurs postsynaptiques. Cette fusion de vésicules et de récepteurs postsynaptiques à proximité garantit qu'il y a peu de retard entre l'activation des récepteurs postsynaptiques et la libération de neurotransmetteurs.
Mécanisme de libération des neurotransmetteurs
La libération du neurotransmetteur est accomplie par la fusion des vésicules du neurotransmetteur à la membrane présynaptique. Bien que les détails de ce mécanisme soient encore à l'étude, il existe un consensus sur certains détails du processus. La fusion des vésicules synaptiques avec la membrane présynaptique est connue pour nécessiter une augmentation locale du calcium à partir d'un seul canal calcique étroitement associé et la formation de complexes SNARE hautement stables . Un modèle dominant de fusion de vésicules synaptiques est que la formation du complexe SNARE est catalysée par les protéines de la zone active telles que Munc18, Munc13 et RIM. On pense que la formation de ce complexe « prépare » la vésicule à être prête pour la fusion des vésicules et la libération du neurotransmetteur (voir ci-dessous : pool libérable). Une fois que la vésicule est amorcée, la complexine se lie au complexe SNARE, c'est ce qu'on appelle « super-amorcée ». Les vésicules qui sont surprimées se trouvent dans le pool facilement libérable (voir ci-dessous) et sont prêtes à être rapidement libérées. L'arrivée d'un potentiel d'action ouvre des canaux calciques voltage-dépendants près du complexe SNARE/complexine. Le calcium se lie alors pour modifier la conformation de la synaptotagmine . Ce changement de conformation permet à la synaptotagmine de déloger ensuite la complexine, de se lier au complexe SNARE et de se lier à la membrane cible. Lorsque la synaptotagmine se lie à la fois au complexe SNARE et à la membrane, cela induit une force mécanique sur la membrane de sorte qu'elle provoque la fusion de la membrane vésiculaire et de la membrane présynaptique. Cette fusion ouvre un pore membranaire qui libère le neurotransmetteur. Le pore augmente de taille jusqu'à ce que toute la membrane vésiculaire soit indiscernable de la membrane présynaptique.
Cycle des vésicules synaptiques
Le bouton présynaptique a un processus efficacement orchestré pour fusionner les vésicules à la membrane présynaptique pour libérer les neurotransmetteurs et régénérer les vésicules des neurotransmetteurs. Ce processus appelé cycle des vésicules synaptiques maintient le nombre de vésicules dans le bouton présynaptique et permet au terminal synaptique d'être une unité autonome. Le cycle commence par (1) une région de l' appareil de Golgi est pincée pour former la vésicule synaptique et cette vésicule est transportée vers la terminaison synaptique. Au terminal (2), la vésicule est remplie de neurotransmetteur. (3) La vésicule est transportée vers la zone active et amarrée à proximité immédiate de la membrane plasmique. (4) Au cours d'un potentiel d'action, la vésicule fusionne avec la membrane, libère le neurotransmetteur et permet aux protéines membranaires précédemment présentes sur la vésicule de diffuser vers la zone périactive. (5) Dans la zone périactive, les protéines membranaires sont séquestrées et sont endocytosées en formant une vésicule recouverte de clathrine . (6) La vésicule est ensuite remplie de neurotransmetteur et est ensuite transportée vers la zone active.
Le mécanisme d'endocytose est plus lent que le mécanisme d' exocytose . Cela signifie qu'en cas d'activité intense, la vésicule dans le terminal peut s'épuiser et ne plus être disponible pour être libérée. Pour aider à prévenir l'épuisement des vésicules synaptiques, l'augmentation du calcium pendant une activité intense peut activer la calcineurine qui déphosphoryle les protéines impliquées dans l'endocytose médiée par la clathrine.
Piscines de vésicules
La synapse contient au moins deux groupes de vésicules synaptiques, le pool facilement libérable et le pool de réserve. Le pool facilement libérable est situé dans la zone active et connecté directement à la membrane présynaptique tandis que le pool de réserve est regroupé par le cytosquelette et n'est pas directement connecté à la zone active.
Piscine libérable
La piscine libérable est située dans la zone active et est liée directement à la membrane présynaptique. Il est stabilisé par des protéines au sein de la zone active et lié à la membrane présynaptique par des protéines SNARE . Ces vésicules sont prêtes à être libérées par un seul potentiel d'action et sont reconstituées par les vésicules du pool de réserve. Le pool libérable est parfois subdivisé en pool facilement libérable et en pool libérable.
Réserver la piscine
Le pool de réserve n'est pas directement connecté à la zone active. L'augmentation de la concentration de calcium présynaptique active la protéine kinase dépendante du calcium-calmoduline (CaMK). CaMK phosphoryle une protéine, la synapsine , qui médie le regroupement des vésicules du pool de réserve et la fixation au cytosquelette. La phosphorylation de la synapsine mobilise les vésicules dans le pool de réserve et leur permet de migrer vers la zone active et de reconstituer le pool facilement libérable.
Zone périactive
La zone périactive entoure la zone active et est le site d'endocytose de la terminaison présynaptique. Dans la zone périactive, les protéines d'échafaudage telles que l' intersectine 1 recrutent des protéines qui interviennent dans l'endocytose telles que la dynamine , la clathrine et l'endophiline. Chez la drosophilie, l'homologue d'intersection, Dap160, est situé dans la zone périactive de la jonction neuromusculaire et le mutant Dap160 épuise les vésicules synaptiques lors d'une stimulation à haute fréquence.
Zone active de la synapse du ruban
La synapse ruban est un type spécial de synapse que l'on trouve dans les neurones sensoriels tels que les cellules photoréceptrices , les cellules bipolaires rétiniennes et les cellules ciliées . Les synapses rubanées contiennent une structure protéique dense qui attache un réseau de vésicules perpendiculaires à la membrane présynaptique. Dans une micrographie électronique, il apparaît comme une structure en forme de ruban perpendiculaire à la membrane. Contrairement à la synapse «traditionnelle», les synapses en ruban peuvent maintenir une libération progressive de vésicules. En d'autres termes, plus un neurone est dépolarisé, plus le taux de fusion des vésicules est élevé. La zone active de la synapse du ruban est séparée en deux régions, la densité archiforme et le ruban. La densité archiforme est le site de la fusion des vésicules et le ruban stocke le pool libérable de vésicules. La structure du ruban est composée principalement de la protéine RIBEYE, environ 64 à 69 % du volume du ruban, et est attachée à la densité archiforme par des protéines d'échafaudage telles que le basson.
Protéines
| Protéine | Structure/Fonction |
| Protéines structurelles | |
| Piccolo | |
| Basson | |
| JANTES | |
| ELKS (ERC ou CAST) | |
| FÛT | |
| menthe | |
| Liprine-alpha-1 | |
| Amarrage et amorçage | |
| Munc-13 | |
| Munc-18 | |
| COLLIERS | |
| SNAP25 | |
| VAMP2 | |
| syntaxine | Situé sur la membrane synaptique et se lie à SNAP-25 et à la synaptobrevine pour médier la fusion des vésicules. |
| Protéines du cytosquelette | |
| Actine | |
| Tubuline | |
| myosine De multiples molécules de myosine II génèrent de la force dans le muscle squelettique grâce à un mécanisme de coup de puissance alimenté par l'énergie libérée par l'hydrolyse de l'ATP | |
| spectrine | |
| β-caténine | |
| Canal de calcium | |
| Canal calcique voltage-dépendant (VDCC) | Permet l'afflux rapide de calcium lors d'un potentiel d'action. |
Mesurer la libération de neurotransmetteurs
La libération de neurotransmetteurs peut être mesurée en déterminant l'amplitude du potentiel postsynaptique après avoir déclenché un potentiel d'action dans le neurone présynaptique. Mesurer la libération de neurotransmetteur de cette manière peut être problématique car l'effet du neurone postsynaptique sur la même quantité de neurotransmetteur libéré peut changer avec le temps. Une autre méthode consiste à mesurer la fusion des vésicules avec la membrane présynaptique directement à l'aide d'une pipette à patch . Une membrane cellulaire peut être considérée comme un condensateur dans la mesure où les ions positifs et négatifs sont stockés des deux côtés de la membrane. Plus la surface de la membrane est grande, plus il faut d'ions pour maintenir la membrane à un certain potentiel. En électrophysiologie, cela signifie qu'une injection de courant dans le terminal prendra moins de temps pour charger une membrane à un potentiel donné avant la fusion des vésicules qu'après la fusion des vésicules. Le temps nécessaire pour charger la membrane à un potentiel et la résistance de la membrane sont mesurés et avec ces valeurs, la capacité de la membrane peut être calculée par l'équation Tau/Résistance = Capacité. Avec cette technique, les chercheurs peuvent mesurer directement la libération des vésicules synaptiques en mesurant les augmentations de la capacité membranaire de la terminaison présynaptique.