Alamethicine - Alamethicin

|
|
| Noms | |
|---|---|
|
Nom IUPAC
N -acétyl-2-méthylalanyl- L -prolyl-2-méthylalanyl- L -alanyl-2-méthylalanyl- L -alanyl- L -glutaminyl-2-méthylalanyl- L -valyl-2-méthylalanylglycyl- L -leucyl-2- méthylalanyl- L -prolyl- L -valyl-2-méthylalanyl-2-méthylalanyl- L -α-glutamyl- N 1 -[(1 S )-1-benzyl-2-hydroxyéthyl]- L -glutamamide
|
|
| Identifiants | |
|
Modèle 3D ( JSmol )
|
|
| ChEMBL | |
| ChemSpider | |
| Carte d'information de l'ECHA |
100.121.626 |
|
CID PubChem
|
|
| UNII | |
|
Tableau de bord CompTox ( EPA )
|
|
|
|
|
|
| Propriétés | |
| C 92 H 150 N 22 O 25 | |
| Masse molaire | 1964,31 g/mol |
| Apparence | Solide blanc cassé |
| Point de fusion | 255 à 270 °C (491 à 518 °F ; 528 à 543 K) |
| Insoluble | |
| Solubilité dans DMSO , méthanol , éthanol | Soluble |
|
Sauf indication contraire, les données sont données pour les matériaux dans leur état standard (à 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Références de l'infobox | |
L' alaméthicine est un antibiotique peptidique formant des canaux , produit par le champignon Trichoderma viride . Il appartient aux peptides peptaibol qui contiennent le résidu d'acide aminé non protéinogène Aib ( acide 2-aminoisobutyrique ). Ce résidu induit fortement la formation d' une structure en hélice alpha . La séquence peptidique est :
Ac-Aib-Pro-Aib-Ala-Aib-Ala-Gln-Aib-Val-Aib-Gly-Leu-Aib-Pro-Val-Aib-Aib-Glu-Gln-Phl
(Ac = acétyle, Phl = phénylalaninol , Aib = acide 2-aminoisobutyrique )
Dans les membranes cellulaires , il forme des canaux ioniques voltage- dépendants par agrégation de quatre à six molécules .
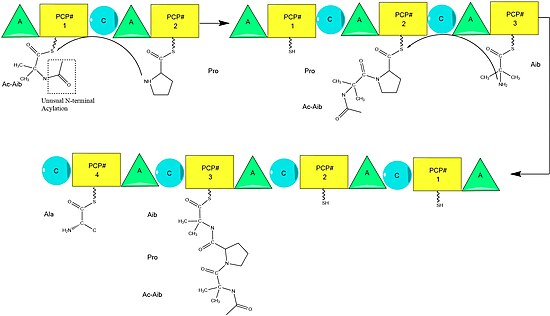
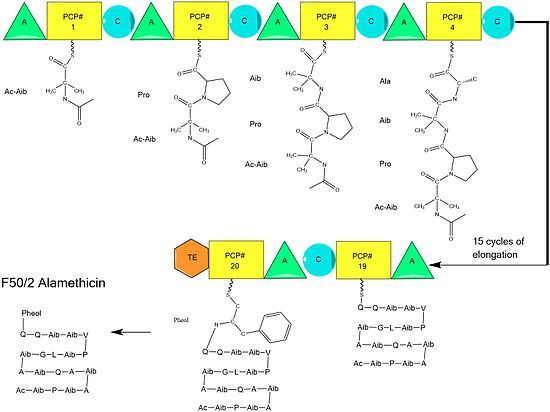
Biosynthèse
La biosynthèse de l'alaméthicine est supposée être catalysée par l'alaméthicine synthase, une peptide synthase non ribosomique (NRPS) isolée pour la première fois en 1975. Bien qu'il existe plusieurs séquences du peptide alaméthicine acceptées, les preuves suggèrent qu'elles suivent toutes le mécanisme général de la NRPS avec de petites variations au niveau des acides aminés sélectionnés. . Commençant par l' acylation de l'extrémité N terminale du premier acide aminoisobutirique sur l'enzyme ALM synthase par l' acétyl-CoA , elle est suivie de la condensation séquentielle des acides aminés par chaque unité modulaire de la synthétase. Les acides aminés sont initialement adénylés par un domaine « d' adénylylation » (A) avant d'être attachés par une liaison thioester à une protéine porteuse peptidique de type Acyl Carrier Protein . La chaîne en croissance est attachée à l'acide aminé portant PCP par le domaine de "condensation" (C), suivi d'un autre cycle des mêmes réactions par le module suivant.
L'assemblage est complété par l'ajout de phénylalaninol, un substrat inhabituel semblable à un acide aminé. Après l'ajout de phénylalaninol, la chaîne peptidique complète est clivée par le domaine thioestérase, clivant la liaison thioester et laissant un alcool.
Les références
Lectures complémentaires
- Jones, LR; Maddock, sud-ouest ; Besch, HR Jr (1980). "Démasquage de l'effet de l'alaméthicine sur la (Na+,K+)-ATPase, l'adénylate cyclase couplée aux récepteurs bêta-adrénergiques et les activités de protéine kinase dépendante de l'AMPc des vésicules cardiaques du sarcolemme" . J. Biol. Chem . 255 (20) : 9971–9980. doi : 10.1016/S0021-9258 (18) 43488-6 . PMID 6253461 .
- Explorez les structures de l' alamethicine à la banque de données sur les protéines
-
Alamethicine dans Norine
- De "Un modèle de canal ionique voltage-dépendant déduit de la structure cristalline de l'alaméthicine à une résolution de 1,5 A." Fox Jr, RO ; Richards, FM (1982). « Un modèle de canal ionique voltage-dépendant déduit de la structure cristalline de l'alaméthicine à une résolution de 1,5 A ». Nature . 300 (5890) : 325-30. Bibcode : 1982Natur.300..325F . doi : 10.1038/300325a0 . PMID 6292726 . S2CID 4278453 .
- Leitgeb, Balázs; Szekeres, Andras; Manczinger, Lászlo ; Vágvölgyi, Csaba; Kredics, László (2007-06-01). "L'histoire d'Alamethicin : Une revue du Peptaibol le plus largement étudié". Chimie & Biodiversité . 4 (6) : 1027-1051. doi : 10.1002/cbdv.200790095 . ISSN 1612-1880 . PMID 17589875 . S2CID 40886688 .