Trichlorure d'antimoine - Antimony trichloride

|
|||
|
|
|||
| Des noms | |||
|---|---|---|---|
|
Nom IUPAC préféré
Trichlorure d'antimoine |
|||
|
Nom IUPAC systématique
Trichlorostibane |
|||
| Autres noms
Chlorure d'antimoine (III), Beurre d'antimoine, Chlorure d'antimoine, Chlorure de Stibous, Trichlorostibine
|
|||
| Identifiants | |||
|
Modèle 3D ( JSmol )
|
|||
| ChEBI | |||
| ChemSpider | |||
| Carte d'information de l'ECHA |
100.030.031 |
||
| Numéro CE | |||
| KEGG | |||
| Engrener | Antimoine + trichlorure | ||
|
CID PubChem
|
|||
| Numéro RTECS | |||
| UNII | |||
| Numéro ONU | 1733 | ||
|
Tableau de bord CompTox ( EPA )
|
|||
|
|||
|
|||
| Propriétés | |||
| Cl 3 Sb | |||
| Masse molaire | 228,11 g·mol -1 | ||
| Apparence | Solide incolore, très hygroscopique | ||
| Odeur | Fort, piquant | ||
| Densité | 3,14 g / cm 3 (25 ° C) 2,51 g / cm 3 (150 ° C) |
||
| Point de fusion | 73,4 °C (164,1 °F; 346,5 K) | ||
| Point d'ébullition | 223,5 °C (434,3 °F; 496,6 K) | ||
| 601,1 g/100 ml (0 °C) 985,1 g/100 ml (25 °C) 1,357 kg/100 ml (40 °C) |
|||
| Solubilité | Soluble dans acétone , éthanol , CH 2 Cl 2 , phényles , éther , dioxane , CS 2 , CCl 4 , CHCl 3 , cyclohexane , oxychlorure de sélénium(IV) Insoluble dans pyridine , quinoléine , bases organiques |
||
| Solubilité dans l'acide acétique | 143,9 g/100 g (0 °C) 205,8 g/100 g (10 °C) 440,5 g/100 g (25 °C) 693,7 g/100 g (45 °C) |
||
| Solubilité dans l' acétone | 537,6 g/100 g (18 °C) | ||
| Solubilité dans le chlorure de benzoyle | 139,2 g/100 g (15 °C) 169,5 g/100 g (25 °C) 2,76 kg/100 g (70 °C) |
||
| Solubilité dans l'acide chlorhydrique | 20 °C : 8,954 g/g (4,63 % p/p) 8,576 g/g (14,4 % p/p) 7,898 g/g (36,7 % p/p) |
||
| Solubilité dans p-Cymène | 69,5 g/100 g (-3,5 °C) 85,5 g/100 g (10 °C) 150 g/100 g (30 °C) 2,17 kg/100 g (70 °C) |
||
| La pression de vapeur | 13,33 Pa (18,1 °C) 0,15 kPa (50 °C) 2,6 kPa (100 °C) |
||
| -86,7·10 -6 cm 3 /mol | |||
|
Indice de réfraction ( n D )
|
1,46 | ||
| Structure | |||
| orthorhombique | |||
| 3,93D (20 °C) | |||
| Thermochimie | |||
|
Capacité calorifique ( C )
|
183,3 J/mol·K | ||
|
Entropie molaire standard ( S |
110,5 J/mol·K | ||
|
Std enthalpie de
formation (Δ f H ⦵ 298 ) |
-381.2 kJ/mol | ||
|
Énergie libre de Gibbs (Δ f G ˚)
|
-322,5 kJ/mol | ||
| Dangers | |||
| Fiche de données de sécurité | ICSC 1224 | ||
| Pictogrammes SGH |
 
|
||
| Mention d'avertissement SGH | Danger | ||
| H314 , H411 | |||
| P273 , P280 , P305+351+338 , P310 | |||
| NFPA 704 (diamant de feu) | |||
| point de rupture | Ininflammable | ||
| Dose ou concentration létale (LD, LC) : | |||
|
DL 50 ( dose médiane )
|
525 mg/kg (orale, rat) | ||
| NIOSH (limites d'exposition pour la santé aux États-Unis) : | |||
|
PEL (Autorisé)
|
TWA 0,5 mg/m 3 (en Sb) | ||
|
REL (recommandé)
|
TWA 0,5 mg/m 3 (en Sb) | ||
| Composés apparentés | |||
|
Autres anions
|
Trifluorure d' antimoine Tribromure d' antimoine Triiodure d'antimoine |
||
|
Autres cations
|
Trichlorure d'azote Trichlorure de phosphore Trichlorure d' arsenic Chlorure de bismuth |
||
|
Sauf indication contraire, les données sont données pour les matériaux dans leur état standard (à 25 °C [77 °F], 100 kPa). |
|||
|
|
|||
| Références de l'infobox | |||
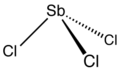
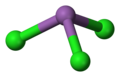
Le trichlorure d'antimoine est le composé chimique de formule SbCl 3 . C'est un solide incolore doux avec une odeur piquante et était connu des alchimistes comme beurre d'antimoine .
Préparation
Le trichlorure d'antimoine est préparé par réaction du chlore avec de l' antimoine , du tribromure d' antimoine , du trioxyde d' antimoine ou du trisulfure d'antimoine . Il peut également être fabriqué en traitant le trioxyde d'antimoine avec de l'acide chlorhydrique concentré .
Réactions
SbCl 3 est facilement hydrolysé et les échantillons de SbCl 3 doivent être protégés de l'humidité. Avec une quantité limitée d'eau, il forme de l'oxychlorure d'antimoine libérant du chlorure d'hydrogène :
- SbCl 3 + H 2 O → SbOCl + 2 HCl
Avec plus d'eau, il forme Sb
4O
5Cl
2qui en chauffant à 460° sous argon se transforme en Sb
8O
11Cl
12.
SbCl 3 forme facilement des complexes avec les halogénures, mais les stoechiométries ne sont pas un bon guide pour la composition, par exemple le (C
5H
5NH)SbCl
4contient un anion en chaîne avec des octaèdres Sb III déformés . De même le sel (C
4H
9NH
3)
2SbCl
5contient un anion polymère de composition [SbCl2−
5]
mavec octaèdre déformé Sb III .
Avec les ligands donneurs d'azote, L, des complexes avec une paire isolée stéréochimiquement active sont formés, par exemple LS-trigonal bipyramidal LSbCl 3 et Ψ-octaédrique L
2SbCl
3.
SbCl 3 n'est qu'une base de Lewis faible, cependant certains complexes sont connus par exemple les complexes carbonylés , Fe(CO)
3(SbCl
3)
2et Ni(CO)
3SbCl
3.
Structure
En phase gazeuse, SbCl 3 est pyramidal avec un angle Cl-Sb-Cl de 97,2° et une longueur de liaison de 233 pm. Dans SbCl 3 chaque Sb a trois atomes Cl à 234 pm montrant la persistance de l' unité moléculaire SbCl 3 , cependant il y a cinq autres atomes Cl voisins, deux à 346 pm, un à 361 pm et deux à 374 pm. Ces huit atomes peuvent être considérés comme formant un prisme trigonal bicapuchonné. Ces distances peuvent être contrastées avec BiCl 3 qui a trois voisins proches à 250 pm, avec deux à 324 pm et trois à une moyenne de 336 pm. Le point à noter ici est que les huit voisins proches de Bi sont plus proches que les huit voisins les plus proches de Sb, démontrant la tendance de Bi à adopter des nombres de coordination plus élevés.
Les usages
SbCl 3 est un réactif de détection de la vitamine A et des caroténoïdes apparentés dans le test de Carr-Price . Le trichlorure d'antimoine réagit avec le caroténoïde pour former un complexe bleu mesurable par colorimétrie .
Le trichlorure d'antimoine a également été utilisé comme adultérant pour renforcer l' effet louche de l' absinthe . Il a été utilisé dans le passé pour dissoudre et retirer les talons de corne des veaux sans avoir à les couper.
Il est également utilisé comme catalyseur pour les réactions de polymérisation, d'hydrocraquage et de chloration ; comme mordant ; et dans la production d'autres sels d'antimoine. Sa solution est utilisée comme réactif analytique pour le chloral, les aromatiques et la vitamine A . Il a une utilisation très potentielle en tant que catalyseur acide de Lewis dans la transformation organique synthétique.
Une solution de trichlorure d'antimoine dans du sulfure d'hydrogène liquide est un bon conducteur, bien que ses applications soient limitées par la très basse température ou la pression élevée requise pour que le sulfure d'hydrogène soit liquide.
Références dans la culture populaire
Dans l'épisode 12 de la troisième saison de la populaire émission britannique All Creatures Great and Small (adapté du chapitre six du livre All Things Wise and Wonderful ), plusieurs veaux sont morts à la suite d'un épisode de gastro - entérite non spécifique , dont la cause a ensuite été déterminée à être l'ingestion de trichlorure d'antimoine présent dans une solution utilisée pour dissoudre leurs talons de corne.