Trisulfure d'arsenic - Arsenic trisulfide

|
|
|
|
|
|
|
| Noms | |
|---|---|
|
Nom IUPAC préféré
Trisulfure d'arsenic |
|
| Autres noms
Sulfure d'arsenic (III)
Orpiment |
|
| Identifiants | |
|
Modèle 3D ( JSmol )
|
|
| ChemSpider | |
| Carte d'information de l'ECHA |
100.013.744 |
| Numéro CE | |
|
CID PubChem
|
|
| Numéro RTECS | |
| UNII | |
|
Tableau de bord CompTox ( EPA )
|
|
|
|
|
|
| Propriétés | |
| Comme 2 S 3 | |
| Masse molaire | 246.02 g·mol −1 |
| Apparence | Cristaux oranges |
| Densité | 3,43 g cm -3 |
| Point de fusion | 310 °C (590 °F; 583 K) |
| Point d'ébullition | 707 °C (1 305 °F ; 980 K) |
| -70,0·10 -6 cm 3 /mol | |
| Structure | |
| P2 1 / n ( n ° 11) | |
|
a = 1147,5(5) pm, b = 957,7(4) pm, c = 425,6(2) pm
= 90°, = 90,68(8)°, = 90°
|
|
| pyramidale (As) | |
| Dangers | |
| Pictogrammes SGH |
 
|
| Mention d'avertissement SGH | Danger |
| H300 , H331 , H400 , H411 | |
| NFPA 704 (diamant de feu) | |
| NIOSH (limites d'exposition pour la santé aux États-Unis) : | |
|
PEL (Autorisé)
|
[1910.1018] VME 0,010 mg/m 3 |
|
REL (recommandé)
|
Ca C 0,002 mg/m 3 [15 minutes] |
|
IDLH (Danger immédiat)
|
Ca [5 mg/m 3 (en As)] |
| Composés apparentés | |
|
Autres anions
|
Trioxyde d' arsenic Triséléniure d' arsenic Tellurure d'arsenic |
|
Autres cations
|
Trisulfure de phosphore Trisulfure d' antimoine Sulfure de bismuth |
|
Composés apparentés
|
Tétrasulfure tétraarsenique |
|
Sauf indication contraire, les données sont données pour les matériaux dans leur état standard (à 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Références de l'infobox | |
Le trisulfure d'arsenic est le composé inorganique de formule As 2 S 3 . C'est un solide jaune foncé insoluble dans l'eau. Il se produit également sous forme d' orpiment minéral (latin : auripigment), qui a été utilisé comme pigment appelé jaune du roi. Il est produit dans l'analyse des composés de l'arsenic. Il s'agit d'un semi-conducteur intrinsèque de type p du groupe V/VI et qui présente des propriétés de changement de phase photo-induit. L'autre principal sulfure d'arsenic est l'As 4 S 4 , un solide rouge-orange connu sous le nom de réalgar minéral .
Structure
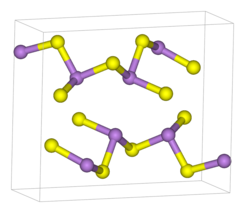
As 2 S 3 se présente à la fois sous forme cristalline et amorphe. Les deux formes présentent des structures polymères constituées de centres pyramidaux trigonaux As(III) liés par des centres sulfurés. Les centres sulfurés sont doublement coordonnés à deux atomes d'arsenic. Sous la forme cristalline, le composé adopte une structure de feuille ébouriffée. La liaison entre les feuilles se compose des forces de van der Waals . La forme cristalline se trouve généralement dans les échantillons géologiques. L'As 2 S 3 amorphe ne possède pas de structure en couches mais est plus fortement réticulé. Comme les autres verres, il n'y a pas d'ordre à moyenne ou longue portée, mais la première sphère de coordination est bien définie. As 2 S 3 est un bon formateur de verre et présente une large région de formation de verre dans son diagramme de phase.
Propriétés
C'est un semi - conducteur , avec une bande interdite directe de 2,7 eV. La large bande interdite le rend transparent à l' infrarouge entre 620 nm et 11 µm.
Synthèse
Des éléments
L'As 2 S 3 amorphe est obtenu par fusion des éléments à 390 °C. Un refroidissement rapide de la masse fondue réactionnelle donne un verre. La réaction peut être représentée par l'équation chimique :
- 2 Comme + 3 S → Comme 2 S 3
Précipitations aqueuses
L'As 2 S 3 se forme lorsque des solutions aqueuses contenant de l'As(III) sont traitées avec de l'H 2 S. L'arsenic était dans le passé analysé et dosé par cette réaction, ce qui conduit à la précipitation d'As 2 S 3 , qui est ensuite pesé. Comme 2 S 3 peut même être précipité dans HCl 6M. Comme 2 S 3 est si insoluble qu'il n'est pas toxique.
Réactions
Lors du chauffage sous vide, l'As 2 S 3 polymère « se fissure » pour donner un mélange d'espèces moléculaires, y compris l'As 4 S 6 moléculaire . As 4 S 6 adopte la géométrie de l' adamantane , comme celle observée pour P 4 O 6 et As 4 O 6 . Lorsqu'un film de ce matériau est exposé à une source d'énergie externe telle que l'énergie thermique (via un recuit thermique), un rayonnement électromagnétique (c'est-à-dire des lampes UV, des lasers, des faisceaux d'électrons)), As 4 S 6 polymérise :
- 2/n (Comme 2 S 3 ) n Comme 4 S 6
As 2 S 3 se dissout de manière caractéristique lors du traitement avec des solutions aqueuses contenant des ions sulfure . L'espèce d'arsenic dissous est le trianion pyramidal AsS3−
3:
- Comme 2 S 3 + 6 NaSH → 2 AsS3−
3 + 3 H 2 S
As 2 S 3 est l'anhydride de l'acide thioarseneux hypothétique, As(SH) 3 . Lors du traitement avec des ions polysulfure , As 2 S 3 se dissout pour donner une variété d'espèces contenant à la fois des liaisons SS et As-S. Un dérivé est S 7 As-S − , un cycle qui contient un centre sulfuré exocyclique attaché à l'atome As. Comme 2 S 3 se dissout également dans des solutions fortement alcalines pour donner un mélange d'AsS3−
3et AsO3−
3.
La "torréfaction" As 2 S 3 dans l'air donne des dérivés volatils et toxiques, cette transformation étant l'un des dangers liés au raffinage des minerais de métaux lourds :
- 2 As 2 S 3 + 9 O 2 → As 4 O 6 + 6 SO 2
Usages contemporains
En tant que résine photosensible inorganique
En raison de son indice de réfraction élevé de 2,45 et de sa grande dureté Knoop par rapport aux résines photosensibles organiques , As 2 S 3 a été étudié pour la fabrication de cristaux photoniques avec une bande interdite entièrement photonique. Les progrès des techniques de structuration au laser, telles que l'écriture laser directe tridimensionnelle (3-D DLW) et la chimie chimique de gravure humide , ont permis d'utiliser ce matériau comme résine photosensible pour fabriquer des nanostructures 3-D.
As 2 S 3 a été étudié pour une utilisation en tant que matériau photorésistant à haute résolution depuis le début des années 1970, en utilisant des agents de gravure aqueux. Bien que ces agents de gravure aqueux aient permis de fabriquer des structures 2-D à faible rapport d'aspect, ils ne permettent pas la gravure de structures à rapport d'aspect élevé avec une périodicité 3-D. Certains réactifs organiques, utilisés dans les solvants organiques, permettent la sélectivité de gravure élevée requise pour produire des structures à rapport d'aspect élevé avec une périodicité 3-D.
Applications médicales
As 2 S 3 et As 4 S 4 ont été étudiés comme traitements de la leucémie aiguë promyélocytaire (LPA).
Pour lunettes IR
Le trisulfure d'arsenic fabriqué sous forme amorphe est utilisé comme verre chalcogénure pour l' optique infrarouge . Il est transparent entre 620 nm et 11 µm. Le verre au trisulfure d'arsenic est plus résistant à l'oxydation que le trisulfure d'arsenic cristallin, ce qui minimise les problèmes de toxicité. Il peut également être utilisé comme matériau acousto-optique .
Le trisulfure d'arsenic a été utilisé pour le nez conique à huit côtés distinctif sur le chercheur infrarouge du missile de Havilland Firestreak .
Rôle dans l'art ancien
Les anciens Égyptiens auraient utilisé l'orpiment, naturel ou synthétique, comme pigment dans l'art et les cosmétiques.
Divers
Le trisulfure d'arsenic est également utilisé comme agent tannant . Il était autrefois utilisé avec un colorant indigo pour la production de bleu crayon, ce qui permettait d'ajouter des teintes bleu foncé au tissu au crayon ou au pinceau.
La précipitation du trisulfure d'arsenic est utilisée comme test analytique pour la présence de bactéries dissimilatrices réduisant l'arsenic (DARB).
Sécurité
Comme 2 S 3 est si insoluble que sa toxicité est faible. Les échantillons vieillis peuvent contenir des quantités substantielles d'oxydes d'arsenic, qui sont solubles et donc hautement toxiques.
Occurrence naturelle
L'orpiment se trouve dans les environnements volcaniques, souvent avec d'autres sulfures d'arsenic, principalement du réalgar . On le trouve parfois dans des veines hydrothermales à basse température, avec d'autres minéraux sulfurés et sulfosels.
Les références
Lectures complémentaires
- « L'arsenic et les composés de l'arsenic », Évaluations globales de la cancérogénicité : une mise à jour des monographies du CIRC, volumes 1 à 42 (PDF) , Monographies du CIRC sur l'évaluation des risques cancérogènes pour l'homme Supplément 7, Lyon, France : Centre international de recherche sur le cancer, 1987 , p. 100–6, ISBN 92-832-1411-0. "Arsenic in Drinking Water", Some Drinking-water Disinfectants and Contaminants, y compris l'arsenic (PDF) , IARC Monographs on the Evaluation of Carcinogenic Risks to Humans 84, Lyon, France : Centre international de recherche sur le cancer, 2004, pp. 39– 267, ISBN 92-832-1284-3.
- « Composés d'arsenic, inorganiques », Rapport sur les agents cancérigènes, onzième édition (PDF), US Department of Health and Human Services, Public Health Service, National Toxicology Program, 2005.

