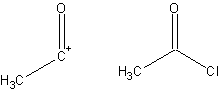Analyse rétrosynthétique - Retrosynthetic analysis
L'analyse rétrosynthétique est une technique de résolution des problèmes de planification de synthèses organiques . Ceci est réalisé en transformant une molécule cible en structures précurseurs plus simples indépendamment de toute réactivité/interaction potentielle avec les réactifs. Chaque matériau précurseur est examiné en utilisant la même méthode. Cette procédure est répétée jusqu'à ce que des structures simples ou disponibles dans le commerce soient atteintes. Ces composés plus simples/disponibles dans le commerce peuvent être utilisés pour former une synthèse de la molécule cible. EJ Corey a formalisé ce concept dans son livre The Logic of Chemical Synthesis .
La puissance de l'analyse rétrosynthétique devient évidente dans la conception d'une synthèse. Le but de l'analyse rétrosynthétique est une simplification structurelle. Souvent, une synthèse aura plus d'une voie de synthèse possible. La rétrosynthèse est bien adaptée pour découvrir différentes voies de synthèse et les comparer de manière logique et directe. Une base de données peut être consultée à chaque étape de l'analyse, afin de déterminer si une composante existe déjà dans la littérature. Dans ce cas, aucune autre exploration de ce composé ne serait nécessaire. Si ce composé existe, il peut être un point de départ pour d'autres étapes développées pour atteindre une synthèse.
Définitions
- Coupure
- Une étape de rétrosynthèse impliquant la rupture d'une liaison pour former deux (ou plus) synthons .
- Rétron
- Une sous-structure moléculaire minimale qui permet certaines transformations.
- Arbre rétrosynthétique
- Un graphe orienté acyclique de plusieurs (ou toutes) rétrosynthèses possibles d'une même cible.
- Synthon
- Fragment d'un composé qui aide à la formation d'une synthèse, dérivé de cette molécule cible. Un synthon et l' équivalent synthétique correspondant disponible dans le commerce sont indiqués ci-dessous :
- Cible
- Le composé final souhaité.
- Transformer
- L'inverse d'une réaction synthétique ; la formation de matières premières à partir d'un seul produit.
Exemple
Un exemple permettra de comprendre facilement le concept d'analyse rétrosynthétique.
Lors de la planification de la synthèse de l'acide phénylacétique , deux synthons sont identifiés. Un groupe nucléophile "-COOH" et un groupe électrophile "PhCH 2 + ". Bien entendu, les deux synthons n'existent pas en soi ; des équivalents synthétiques correspondant aux synthons sont mis à réagir pour produire le produit souhaité. Dans ce cas, l' anion cyanure est l'équivalent synthétique du synthon - COOH, tandis que le bromure de benzyle est l'équivalent synthétique du synthon benzylique.
La synthèse d'acide phénylacétique déterminée par analyse rétrosynthétique est donc :
- PhCH 2 Br + NaCN → PhCH 2 CN + NaBr
- PhCH 2 CN + 2 H 2 O → PhCH 2 COOH + NH 3
En effet, l'acide phénylacétique a été synthétisé à partir du cyanure de benzyle , lui-même préparé par la réaction analogue du chlorure de benzyle avec le cyanure de sodium .
Stratégies
Stratégies de groupe fonctionnel
La manipulation des groupes fonctionnels peut conduire à des réductions significatives de la complexité moléculaire.
Stratégies stéréochimiques
De nombreuses cibles chimiques ont des exigences stéréochimiques distinctes . Les transformations stéréochimiques (telles que le réarrangement de Claisen et la réaction de Mitsunobu ) peuvent supprimer ou transférer la chiralité souhaitée, simplifiant ainsi la cible.
Stratégies structure-objectif
Diriger une synthèse vers un intermédiaire souhaitable peut considérablement réduire l'objectif de l'analyse. Cela permet des techniques de recherche bidirectionnelle.
Stratégies basées sur la transformation
L'application des transformations à l'analyse rétrosynthétique peut conduire à de puissantes réductions de la complexité moléculaire. Malheureusement, de puissants rétrons basés sur des transformations sont rarement présents dans les molécules complexes, et des étapes de synthèse supplémentaires sont souvent nécessaires pour établir leur présence.
Stratégies topologiques
L'identification d'une ou plusieurs déconnexions de liaisons clés peut conduire à l'identification de sous-structures clés ou à des transformations de réarrangement difficiles à identifier afin d'identifier les structures clés.
- Les déconnexions qui préservent les structures en anneau sont encouragées.
- Les déconnexions qui créent des anneaux de plus de 7 membres sont déconseillées.
- La déconnexion implique la créativité.
Voir également
Les références
Liens externes
- Centre d'informatique moléculaire et biomoléculaire
- Présentation sur ARChem Route Designer, ACS, Philadelphie, septembre 2008 pour plus d'informations sur ARChem voir les pages SimBioSys .
- Manifold, Logiciel disponible gratuitement pour les utilisateurs académiques développé par PostEra
- Outil de planification de la rétrosynthèse : ICSynth par InfoChem
- Spaya, Logiciel en libre accès proposé par Iktos