Acide hypofluoreux - Hypofluorous acid
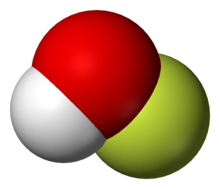
 Structure en phase gazeuse
|
|
|
|
| Des noms | |
|---|---|
|
Nom IUPAC
Acide hypofluoreux
|
|
| Autres noms
Hypofluorite un atome d' hydrogène un
atome d' hydrogène fluorate (-I) Fluoric (-I) de l' acide hydrogène monofluoroxygenate (0) hydroxyle fluorure |
|
| Identifiants | |
|
Modèle 3D ( JSmol )
|
|
| ChemSpider | |
|
PubChem CID
|
|
|
Tableau de bord CompTox ( EPA )
|
|
|
|
|
|
| Propriétés | |
| HOF | |
| Masse molaire | 36,0057 g mol -1 |
| Apparence | liquide jaune pâle au-dessus de -117 ° C solide blanc en dessous de -117 ° C |
| Point de fusion | −117 ° C (−179 ° F; 156 K) |
| Point d'ébullition |
se décompose à 0 ° C |
| Structure | |
| C s | |
| Dangers | |
| Principaux dangers | comburant puissant, corrosif |
| NFPA 704 (diamant de feu) | |
| Composés apparentés | |
|
Autres cations
|
hypofluorite de lithium |
|
Composés apparentés
|
acide hypochloreux nitroxyl hydrogène cyanure formaldéhyde |
|
Sauf indication contraire, les données sont données pour les matériaux dans leur état standard (à 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Références Infobox | |
L'acide hypofluoreux , de formule chimique H O F , est le seul oxyacide connu du fluor et le seul oxoacide connu dans lequel l'atome principal tire des électrons de l' oxygène pour créer un état d'oxydation négatif. L'état d'oxydation de l'oxygène dans les hypofluorites est de 0. C'est aussi le seul acide hypohaleux qui peut être isolé sous forme solide . Le HOF est un intermédiaire dans l' oxydation de l' eau par le fluor , qui produit du fluorure d'hydrogène , du difluorure d'oxygène , du peroxyde d'hydrogène , de l' ozone et de l' oxygène . HOF est explosif à température ambiante, formant HF et O 2 :
- 2 HOF → 2 HF + O 2
Il a été isolé sous forme pure en faisant passer du gaz F 2 sur de la glace à -40 ° C, en collectant le gaz HOF et en le condensant:
- F 2 + H 2 O → HOF + HF
Le composé a été caractérisé en phase solide par cristallographie aux rayons X sous la forme d'une molécule courbée avec un angle de 101 °. Les longueurs de liaison O – F et O – H sont respectivement de 144,2 et 96,4 picomètres . Le cadre solide est constitué de chaînes avec des liaisons O – H ··· O. La structure a également été analysée en phase gazeuse, un état dans lequel l'angle de liaison H – O – F est légèrement plus étroit (97,2 °).
L'acide hypofluoreux dans l'acétonitrile (généré in situ par passage du fluor gazeux à travers l' acétonitrile «humide» ) est communément appelé réactif de Rozen .
Hypofluorites
Les hypofluorites sont formellement des dérivés de OF - , qui est la base conjuguée de l'acide hypofluoreux. Un exemple est l'hypofluorite de trifluorométhyle (CF 3 OF).
Voir également
- L'acide hypochloreux , un composé apparenté qui est plus important sur le plan technologique mais qui n'a pas été obtenu sous forme pure.

