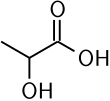
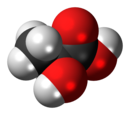
Acide lactique -Lactic acid
|
|
|||
| Des noms | |||
|---|---|---|---|
|
Nom IUPAC préféré
Acide 2-hydroxypropanoïque |
|||
| Autres noms
Acide lactique Acide du
lait |
|||
| Identifiants | |||
|
Modèle 3D ( JSmol )
|
|||
| 3DMet | |||
| 1720251 | |||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| Carte d'information de l'ECHA | 100.000.017 | ||
| Numéro CE | |||
| Numéro E | E270 (conservateurs) | ||
| 362717 | |||
| KEGG | |||
|
CID PubChem
|
|||
| Numéro RTECS | |||
| UNII | |||
| Numéro ONU | 3265 | ||
|
Tableau de bord CompTox ( EPA )
|
|||
|
|||
|
|||
| Propriétés | |||
| C3H6O3 _ _ _ _ _ | |||
| Masse molaire | 90,078 g · mol -1 | ||
| Point de fusion | 18 ° C (64 ° F; 291 K) | ||
| Point d'ébullition | 122 ° C (252 ° F; 395 K) à 15 mm Hg | ||
| Miscible | |||
| Acidité (p K a ) | 3.86, 15.1 | ||
| Thermochimie | |||
|
Enthalpie de
combustion standard (Δ c H ⦵ 298 ) |
1361,9 kJ/mol, 325,5 kcal/mol, 15,1 kJ/g, 3,61 kcal/g | ||
| Pharmacologie | |||
| G01AD01 ( OMS ) QP53AG02 ( OMS ) | |||
| Dangers | |||
| Étiquetage SGH : | |||

|
|||
| H315 , H318 | |||
| P280 , P305+P351+P338 | |||
| Composés apparentés | |||
|
Autres anions
|
Lactate | ||
|
Acides carboxyliques apparentés
|
Acide acétique Acide glycolique Acide propionique Acide 3-hydroxypropanoïque Acide malonique Acide butyrique Acide hydroxybutyrique |
||
|
Composés apparentés
|
1-Propanol 2-Propanol Propionaldéhyde Acroléine Lactate de sodium Lactate d'éthyle |
||
|
Sauf indication contraire, les données sont données pour les matériaux dans leur état standard (à 25 °C [77 °F], 100 kPa).
|
|||
L'acide lactique est un acide organique . Il a une formule moléculaire CH 3 CH(OH)COOH. Il est blanc à l'état solide et il est miscible à l'eau. Lorsqu'il est à l'état dissous, il forme une solution incolore. La production comprend à la fois la synthèse artificielle et les sources naturelles. L'acide lactique est un acide alpha-hydroxylé (AHA) en raison de la présence d'un groupe hydroxyle adjacent au groupe carboxyle . Il est utilisé comme intermédiaire de synthèse dans de nombreuses industries de synthèse organique et dans diverses industries biochimiques . La base conjuguée de l'acide lactique est appelée lactate .
En solution, il peut s'ioniser par perte d'un proton pour produire l' ion lactate CH
3CH(OH)CO−
2. Comparé à l'acide acétique , son p K a est inférieur de 1 unité, ce qui signifie que l'acide lactique est dix fois plus acide que l'acide acétique. Cette acidité plus élevée est la conséquence de la liaison hydrogène intramoléculaire entre l'α-hydroxyle et le groupe carboxylate.
L'acide lactique est chiral , composé de deux énantiomères . L'un est connu sous le nom d' acide L -lactique, d'acide ( S )-lactique ou d'acide (+)-lactique, et l'autre, son image miroir, est l'acide D -lactique, l'acide ( R )-lactique ou l'acide (-)- acide lactique. Un mélange des deux en quantités égales est appelé acide DL -lactique, ou acide lactique racémique . L'acide lactique est hygroscopique . L'acide DL -lactique est miscible à l'eau et à l'éthanol au-dessus de son point de fusion, qui est d'environ 16 à 18 °C. L'acide D -lactique et l'acide L -lactique ont un point de fusion plus élevé. L'acide lactique produit par la fermentation du lait est souvent racémique, bien que certaines espèces de bactéries produisent uniquement de l'acide D -lactique. D'autre part, l'acide lactique produit par la respiration anaérobie dans les muscles des animaux possède l'énantiomère ( L ) et est parfois appelé acide "sarcolactique", du grec "sarx" pour la chair.
Chez les animaux, le L -lactate est constamment produit à partir du pyruvate via l' enzyme lactate déshydrogénase (LDH) dans un processus de fermentation pendant le métabolisme normal et l' exercice . Sa concentration n'augmente pas tant que le taux de production de lactate ne dépasse pas le taux d'élimination du lactate, qui est régi par un certain nombre de facteurs, notamment les transporteurs de monocarboxylate , la concentration et l'isoforme de LDH et la capacité oxydative des tissus. La concentration de lactate sanguin est généralement de 1 à 2 mM au repos, mais peut atteindre plus de 20 mM lors d'un effort intense et atteindre 25 mM par la suite. En plus d'autres rôles biologiques, l'acide L -lactique est le principal agoniste endogène du récepteur 1 de l'acide hydroxycarboxylique (HCA 1 ), qui est un récepteur couplé aux protéines G couplé à G i/o ( GPCR ).
Dans l'industrie, la fermentation de l'acide lactique est réalisée par des bactéries lactiques , qui convertissent les glucides simples tels que le glucose , le saccharose ou le galactose en acide lactique. Ces bactéries peuvent aussi se développer dans la bouche ; l' acide qu'ils produisent est responsable de la carie dentaire connue sous le nom de carie . En médecine , le lactate est l'un des principaux composants de la solution lactate de Ringer et de la solution de Hartmann . Ces fluides intraveineux sont constitués de cations sodium et potassium ainsi que d' anions lactate et chlorure en solution avec de l' eau distillée , généralement à des concentrations isotoniques avec le sang humain . Il est le plus souvent utilisé pour la réanimation liquidienne après une perte de sang due à un traumatisme , une intervention chirurgicale ou des brûlures .
Histoire
Le chimiste suédois Carl Wilhelm Scheele a été le premier à isoler l'acide lactique en 1780 du lait aigre . Le nom reflète la forme lactée dérivée du mot latin lac , qui signifie lait. En 1808, Jöns Jacob Berzelius a découvert que l'acide lactique (en fait le L -lactate) est également produit dans les muscles pendant l'effort. Sa structure a été établie par Johannes Wislicenus en 1873.
En 1856, le rôle de Lactobacillus dans la synthèse de l'acide lactique est découvert par Louis Pasteur . Cette voie a été utilisée commercialement par la pharmacie allemande Boehringer Ingelheim en 1895.
En 2006, la production mondiale d'acide lactique a atteint 275 000 tonnes avec une croissance annuelle moyenne de 10 %.
Production
L'acide lactique est produit industriellement par fermentation bactérienne d' hydrates de carbone , ou par synthèse chimique à partir d' acétaldéhyde . En 2009, l'acide lactique était produit majoritairement (70 à 90 %) par fermentation. La production d'acide lactique racémique constitué d'un mélange 1:1 de stéréoisomères D et L , ou de mélanges contenant jusqu'à 99,9 % d'acide L -lactique, est possible par fermentation microbienne. La production à l'échelle industrielle d' acide D -lactique par fermentation est possible, mais beaucoup plus difficile.
Production fermentaire
Les produits laitiers fermentés sont obtenus industriellement par fermentation de lait ou de lactosérum par des bactéries Lactobacillus : Lactobacillus acidophilus , Lactobacillus casei , Lactobacillus delbrueckii subsp. bulgaricus ( Lactobacillus bulgaricus ), Lactobacillus helveticus , Lactococcus lactis et Streptococcus salivarius subsp. thermophilus ( Streptococcus thermophilus ).
En tant que matière de départ pour la production industrielle d'acide lactique, presque toutes les sources de glucides contenant des sucres en C5 et C6 peuvent être utilisées . Le saccharose pur, le glucose provenant de l'amidon, le sucre brut et le jus de betterave sont fréquemment utilisés. Les bactéries productrices d'acide lactique peuvent être divisées en deux classes : les bactéries homofermentaires comme Lactobacillus casei et Lactococcus lactis , produisant deux moles de lactate à partir d'une mole de glucose, et les espèces hétérofermentaires produisant une mole de lactate à partir d'une mole de glucose ainsi que du dioxyde de carbone et acide acétique / éthanol .
Fabrication chimique
L'acide lactique racémique est synthétisé industriellement en faisant réagir de l'acétaldéhyde avec du cyanure d'hydrogène et en hydrolysant le lactonitrile résultant . Lorsque l' hydrolyse est effectuée par l'acide chlorhydrique , le chlorure d'ammonium se forme comme sous-produit ; la société japonaise Musashino est l'un des derniers grands fabricants d'acide lactique par cette voie. La synthèse d'acides lactiques racémiques et énantiopurs est également possible à partir d'autres matières premières ( acétate de vinyle , glycérol , etc.) en appliquant des procédures catalytiques.
La biologie
Biologie moléculaire
L'acide L -lactique est le principal agoniste endogène du récepteur 1 de l'acide hydroxycarboxylique (HCA 1 ), un récepteur couplé à la protéine G couplé i /o ( GPCR ).
Exercice et lactation
Pendant les exercices de puissance tels que le sprint , lorsque le taux de demande d'énergie est élevé, le glucose est décomposé et oxydé en pyruvate , et le lactate est alors produit à partir du pyruvate plus rapidement que le corps ne peut le traiter, ce qui entraîne une augmentation des concentrations de lactate. La production de lactate est bénéfique pour la régénération du NAD + (le pyruvate est réduit en lactate tandis que le NADH est oxydé en NAD + ), qui est utilisé dans l'oxydation du glycéraldéhyde 3-phosphate lors de la production de pyruvate à partir du glucose, ce qui garantit que la production d'énergie est maintenu et l'exercice peut continuer. Pendant un exercice intense, la chaîne respiratoire ne peut pas suivre la quantité d'ions hydrogène qui se rejoignent pour former le NADH, et ne peut pas régénérer le NAD + assez rapidement.
Le lactate ainsi obtenu peut être utilisé de deux manières :
-
Oxydation en pyruvate par des cellules musculaires , des cellules cardiaques et des cellules cérébrales
bien oxygénées
- Le pyruvate est ensuite directement utilisé pour alimenter le cycle de Krebs
- Conversion en glucose par gluconéogenèse dans le foie et remise en circulation ; voir cycle Cori
- Si les concentrations de glucose dans le sang sont élevées, le glucose peut être utilisé pour constituer les réserves de glycogène du foie .
Cependant, le lactate se forme continuellement au repos et à toutes les intensités d'exercice. Avec l'utilisation de traceurs isotopiques stables, George Brooks et ses collègues, de l'Université de Californie à Berkeley, ont observé que le lactate servait de carburant métabolique produit et éliminé par oxydation dans les muscles au repos et en exercice. Certaines causes en sont le métabolisme dans les globules rouges dépourvus de mitochondries et les limitations résultant de l'activité enzymatique qui se produit dans les fibres musculaires ayant une capacité glycolytique élevée.
En 2004, Robergs et al. a soutenu que l'acidose lactique pendant l'exercice est une "construction" ou un mythe, soulignant qu'une partie du H + provient de l'hydrolyse de l'ATP (ATP 4− + H 2 O → ADP 3− + HPO2−
4+ H + ), et que réduire le pyruvate en lactate (pyruvate − + NADH + H + → lactate − + NAD + ) consomme en réalité H + . Lindinger et al . ont rétorqué qu'ils avaient ignoré les facteurs responsables de l'augmentation de [H + ]. Après tout, la production de lactate − à partir d'une molécule neutre doit augmenter [H + ] pour maintenir l'électroneutralité. Le point de l'article de Robergs, cependant, était que le lactate − est produit à partir de pyruvate − , qui a la même charge. C'est le pyruvate − production à partir de glucose neutre qui génère H + :
| C 6 H 12 O 6 + 2 NAD + + 2 ADP 3− + 2 HPO2− 4 |
→ | 2 CH 3COCO− 2+ 2 H + + 2 NADH + 2 ATP 4− + 2 H 2 O |
|
| La production ultérieure de lactate − absorbe ces protons : | |||
| 2 CH 3COCO− 2+ 2 H + + 2 NADH |
→ | 2 CH 3CH(OH)CO− 2+ 2 NAD + |
|
| Globalement: | |||
| C 6 H 12 O 6 + 2 NAD + + 2 ADP 3− + 2 HPO2− 4 |
→ | 2 CH 3COCO− 2+ 2 H + + 2 NADH + 2 ATP 4− + 2 H 2 O |
|
| → | 2 CH 3CH(OH)CO− 2+ 2 NAD + + 2 ATP 4− + 2 H 2 O |
||
Bien que la réaction glucose → 2 lactate − + 2 H + libère deux H + lorsqu'elle est vue seule, les H + sont absorbés dans la production d'ATP. En revanche, l'acidité absorbée est libérée lors de l'hydrolyse ultérieure de l'ATP : ATP 4− + H 2 O → ADP 3− + HPO2−
4+H + . Ainsi, une fois l'utilisation de l'ATP incluse, la réaction globale est
- C 6 H 12 O 6 → 2 CH
3COCO−
2+ 2H +
La génération de CO 2 pendant la respiration provoque également une augmentation de [H + ].
Source d'énergie du tissu neural
Bien que le glucose soit généralement supposé être la principale source d'énergie des tissus vivants, quelques rapports indiquent que c'est le lactate, et non le glucose, qui est préférentiellement métabolisé par les neurones du cerveau de plusieurs espèces de mammifères (les plus notables étant les souris , rats et humains ). Selon l' hypothèse de la navette lactate , les cellules gliales sont responsables de la transformation du glucose en lactate et de l'apport de lactate aux neurones. En raison de cette activité métabolique locale des cellules gliales, le liquide extracellulaire entourant immédiatement les neurones diffère fortement en composition du sang ou du liquide céphalo-rachidien , étant beaucoup plus riche en lactate, comme cela a été constaté dans les études de microdialyse .
Métabolisme du développement cérébral
Certaines preuves suggèrent que le lactate est important aux premiers stades du développement pour le métabolisme cérébral chez les sujets prénatals et postnatals précoces , le lactate à ces stades ayant des concentrations plus élevées dans les liquides corporels et étant utilisé par le cerveau de préférence au glucose. Il a également été émis l'hypothèse que le lactate pourrait exercer une forte action sur les réseaux GABAergiques dans le cerveau en développement , les rendant plus inhibiteurs qu'on ne le supposait auparavant, agissant soit par un meilleur support des métabolites, soit par des altérations des niveaux de pH intracellulaires de base , soit les deux.
Des études sur des tranches de cerveau de souris montrent que le β-hydroxybutyrate , le lactate et le pyruvate agissent comme des substrats d'énergie oxydative, provoquant une augmentation de la phase d'oxydation du NAD(P)H, que le glucose était insuffisant comme vecteur d'énergie lors d'une activité synaptique intense et, enfin , que le lactate peut être un substrat énergétique efficace capable de soutenir et d'améliorer le métabolisme énergétique aérobie du cerveau in vitro . L'étude "fournit de nouvelles données sur les transitoires de fluorescence NAD(P)H biphasiques, une réponse physiologique importante à l'activation neurale qui a été reproduite dans de nombreuses études et dont on pense qu'elle provient principalement des changements de concentration induits par l'activité dans les pools cellulaires de NADH".
Le lactate peut également servir de source d'énergie importante pour d'autres organes, notamment le cœur et le foie. Pendant l'activité physique, jusqu'à 60 % du taux de renouvellement de l'énergie du muscle cardiaque provient de l'oxydation du lactate.
Test sanguin

Des tests sanguins pour le lactate sont effectués pour déterminer l'état de l' homéostasie acido-basique dans le corps. Le prélèvement sanguin à cet effet est souvent artériel (même s'il est plus difficile que la ponction veineuse ), car les taux de lactate diffèrent sensiblement entre artériel et veineux, et le niveau artériel est plus représentatif à cet effet.
| Limite inférieure | Limite supérieure | Unité | |
|---|---|---|---|
| Veineux | 4.5 | 19.8 | mg/dL |
| 0,5 | 2.2 | mmol/L | |
| Artériel | 4.5 | 14.4 | mg/dL |
| 0,5 | 1.6 | mmol/L |
Pendant l'accouchement , les taux de lactate chez le fœtus peuvent être quantifiés par des tests sanguins sur le cuir chevelu fœtal .
Précurseur polymère
Deux molécules d'acide lactique peuvent être déshydratées en lactone lactide . En présence de catalyseurs , le lactide polymérise en polylactide atactique ou syndiotactique (PLA), qui sont des polyesters biodégradables . Le PLA est un exemple de plastique qui n'est pas issu de la pétrochimie .
Applications pharmaceutiques et cosmétiques
L'acide lactique est également utilisé dans la technologie pharmaceutique pour produire des lactates solubles dans l'eau à partir d'ingrédients actifs autrement insolubles. Il trouve également une utilisation dans les préparations topiques et les cosmétiques pour ajuster l'acidité et pour ses propriétés désinfectantes et kératolytiques .
nourriture
L'acide lactique se trouve principalement dans les produits laitiers aigres , tels que le kumis , le laban , le yaourt , le kéfir et certains fromages cottage . La caséine du lait fermenté est coagulée (caillée) par l'acide lactique. L'acide lactique est également responsable de la saveur aigre du pain au levain .
Dans les listes d' informations nutritionnelles, l'acide lactique peut être inclus sous le terme «glucides» (ou «glucides par différence») car cela inclut souvent tout autre chose que l'eau, les protéines, les graisses, les cendres et l'éthanol. Si tel est le cas, l' énergie alimentaire calculée peut utiliser les 4 kilocalories standard (17 kJ) par gramme qui sont souvent utilisées pour tous les glucides. Mais dans certains cas, l'acide lactique est ignoré dans le calcul. La densité énergétique de l'acide lactique est de 362 kilocalories (1 510 kJ) pour 100 g.
Certaines bières ( bière aigre ) contiennent volontairement de l'acide lactique, l'un de ces types étant les lambics belges . Le plus souvent, cela est produit naturellement par diverses souches de bactéries. Ces bactéries fermentent les sucres en acides, contrairement à la levure qui fermente le sucre en éthanol. Après avoir refroidi le moût , les levures et les bactéries peuvent "tomber" dans les fermenteurs ouverts. Les brasseurs de styles de bière plus courants veilleraient à ce qu'aucune de ces bactéries ne soit autorisée à pénétrer dans le fermenteur. Parmi les autres styles de bière acidulée, citons la Berliner Weisse , la Flanders Red et la Wild Ale américaine .
En vinification, un processus bactérien, naturel ou contrôlé, est souvent utilisé pour convertir l'acide malique naturellement présent en acide lactique, pour réduire la netteté et pour d'autres raisons liées au goût. Cette fermentation malolactique est réalisée par des bactéries lactiques .
Bien qu'il ne soit normalement pas présent en quantités importantes dans les fruits, l'acide lactique est le principal acide organique des fruits d' akébie , représentant 2,12 % du jus.
En tant qu'additif alimentaire, son utilisation est approuvée dans l'UE, aux États-Unis, en Australie et en Nouvelle-Zélande ; il est répertorié par son numéro SIN 270 ou sous le numéro E E270. L'acide lactique est utilisé comme conservateur alimentaire, agent de salaison et agent aromatisant. C'est un ingrédient des aliments transformés et il est utilisé comme décontaminant lors de la transformation de la viande. L'acide lactique est produit commercialement par fermentation d'hydrates de carbone tels que le glucose, le saccharose ou le lactose, ou par synthèse chimique. Les sources de glucides comprennent le maïs, les betteraves et le sucre de canne.
Falsification
L'acide lactique a toujours été utilisé pour aider à l'effacement des encres des papiers officiels à modifier lors de la falsification .
Produits de nettoyage
L'acide lactique est utilisé dans certains nettoyants liquides comme agent détartrant pour éliminer les dépôts d'eau dure tels que le carbonate de calcium , formant le lactate, le lactate de calcium . En raison de son acidité élevée, ces dépôts sont éliminés très rapidement, en particulier lorsque de l'eau bouillante est utilisée, comme dans les bouilloires. Il gagne également en popularité dans les détergents antibactériens pour la vaisselle et les savons pour les mains en remplacement du Triclosan .
Voir également
- Acide hydroxybutyrique
- Acides dans le vin
- Cycle alanine
- Plastique biodégradable
- Caries dentaires
- MCT1 , un transporteur de lactate
- Acide thiolactique
Références
Liens externes
- Le plastique de maïs à la rescousse Archivé le 21 novembre 2013 sur la Wayback Machine
- Acide lactique : informations et ressources
- L'acide lactique n'est pas l'ennemi des muscles, c'est du carburant
- Fitzgerald M (26 janvier 2010). "Les mythes de l'acide lactique" . Concurrent en cours d'exécution . Archivé de l'original le 25 août 2018.