Lactone - Lactone
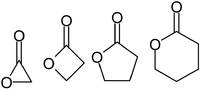
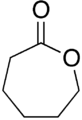
Les lactones sont des esters carboxyliques cycliques , contenant une structure 1-oxacycloalcan-2-one ( -C(=O)-O- ), ou des analogues ayant une insaturation ou des hétéroatomes remplaçant un ou plusieurs atomes de carbone du cycle.
Les lactones sont formées par estérification intramoléculaire des acides hydroxycarboxyliques correspondants, qui a lieu spontanément lorsque le cycle formé est à cinq ou six chaînons. Les lactones à cycles à trois ou quatre chaînons (α-lactones et β-lactones) sont très réactives, ce qui rend leur isolement difficile. Des méthodes spéciales sont normalement requises pour la synthèse en laboratoire des lactones à petits cycles ainsi que celles qui contiennent des cycles de plus de six chaînons.
Nomenclature
Les lactones sont généralement nommées en fonction de la molécule d'acide précurseur ( acéto = 2 atomes de carbone, propio = 3, butyro = 4, valero = 5, capro = 6, etc.), avec un suffixe -lactone et un préfixe de lettre grecque qui spécifie le nombre d'atomes de carbone dans l'hétérocycle, c'est-à-dire la distance entre les groupes -OH et -COOH pertinents le long dudit squelette. Le premier atome de carbone après le carbone dans le groupe -COOH sur le composé parent est étiqueté second, le second sera étiqueté , et ainsi de suite. Par conséquent, les préfixes indiquent également la taille du cycle lactone : -lactone = cycle à 3 chaînons, β-lactone = à 4 chaînons, γ-lactone = à 5 chaînons, etc.Les lactones macrocycliques sont appelées macrolactones .
L'autre suffixe utilisé pour désigner une lactone est -olide , utilisé dans les noms de classes de substances comme buténolide , macrolide , cardénolide ou bufadienolide .
Pour obtenir les noms IUPAC préférés , les lactones sont nommées pseudocétones hétérocycliques en ajoutant le suffixe « one », « dione », « thione », etc. et les préfixes multiplicatifs appropriés au nom de l'hydrure parent hétérocyclique.
Étymologie
Le nom "lactone" a été inventé en 1844 par le chimiste français Théophile-Jules Pelouze , qui l'a d'abord obtenu comme dérivé de l'acide lactique. Le nom lactone dérive du composé cyclique appelé lactide , qui est formé à partir de la déshydratation de l'acide 2-hydroxypropanoïque ( acide lactique ) CH 3 -CH(OH)-COOH. L'acide lactique, à son tour, tire son nom de son isolement originel du lait caillé (latin : lac, lactis). Une déshydratation interne au sein de la même molécule d'acide lactique aurait produit de l' alpha-propiolactone , une lactone avec un cycle à 3 chaînons.
En 1880, le chimiste allemand Wilhelm Rudolph Fittig étendit le nom de « lactone » à tous les esters carboxyliques intramoléculaires.
Sources naturelles
Les lactones naturelles sont principalement des γ- et γ-lactones saturées et insaturées, et dans une moindre mesure des lactones macrocycliques. Les - et -lactones sont des esters intramoléculaires des acides gras hydroxylés correspondants. Ils contribuent à l'arôme des fruits, du beurre, du fromage et d'autres aliments. Le cyclopentadécanolide est responsable de l'odeur musquée de l' huile de racine d'angélique . Parmi les lactones bicycliques naturelles, les phtalides sont responsables des odeurs des huiles de céleri et de livèche , et la coumarine de l' aspérule . Les lactones sont présentes dans le bois de chêne et contribuent au profil aromatique des bières vieillies en fût .
Des cycles lactone se produisent généralement comme blocs de construction dans la nature, par exemple dans de l' acide ascorbique , kawaïne , nepetalactone , gluconolactone , hormones ( spironolactone , mévalonolactone ), des enzymes ( lactonase ), neurotransmetteurs ( butyrolactone , avermectines ), des antibiotiques ( macrolides comme l' érythromycine ; amphotéricine B ) , médicaments anticancéreux ( vernolépine , épothilones ), phytoestrogènes ( lactones d' acide résorcylique , glycosides cardiaques ).
La synthèse
De nombreuses méthodes de synthèse d'esters peuvent également être appliquées à celle des lactones. Dans une synthèse industrielle d' oxandrolone, l'étape clé de formation de lactone est une réaction organique - estérification .
Dans halolactonisation , un alcène est attaqué par un halogène via une addition électrophile avec l'intermédiaire cationique capturé intramoléculairement par un acide carboxylique adjacent (Voir aussi iodolactamisation ).
Des méthodes spécifiques comprennent estérification Yamaguchi , Shiina macrolactonisation , Corey-Nicolaou macrolactonisation , l' oxydation Baeyer-Villiger et l' abstraction nucléophile .
Les gamma-lactones y-octalactone , γ-nonalactone , γ-décalactone , γ-undécalactone peut être préparé avec un bon rendement dans un procédé en une étape par addition radicalaire de primaires alcools gras à l' acide acrylique , à l' aide de di-tert-butyl peroxyde comme un catalyseur.
Réactions
La structure la plus stable pour les lactones sont les -lactones à 5 chaînons et les δ-lactones à 6 chaînons car, comme dans tous les cycles organiques, les cycles à 5 et 6 chaînons minimisent la déformation des angles de liaison . Les γ-lactones sont si stables qu'en présence d'acides dilués à température ambiante, les 4-hydroxy acides (R-CH(OH)-(CH 2 ) 2 -COOH) subissent immédiatement une estérification spontanée et une cyclisation en lactone. Les β-lactones existent, mais ne peuvent être fabriquées que par des méthodes spéciales. Les α-lactones peuvent être détectées en tant qu'espèces transitoires dans des expériences de spectrométrie de masse .
Les réactions des lactones sont similaires à celles des esters, comme illustré par la gamma-lactone dans les sections suivantes :
Hydrolyse
Le chauffage d'une lactone avec une base ( hydroxyde de sodium ) hydrolyse la lactone en son composé parent, le composé bifonctionnel à chaîne droite. Comme les esters à chaîne droite, la réaction d'hydrolyse-condensation des lactones est une réaction réversible , avec un équilibre . Cependant, la constante d'équilibre de la réaction d'hydrolyse de la lactone est inférieure à celle de l'ester linéaire c'est-à-dire que les produits (hydroxyacides) sont moins favorisés dans le cas des lactones. En effet, bien que les enthalpies de l'hydrolyse des esters et des lactones soient à peu près les mêmes, l' entropie de l'hydrolyse des lactones est inférieure à l'entropie des esters à chaîne droite. Les esters à chaîne droite donnent deux produits lors de l'hydrolyse, ce qui rend le changement d'entropie plus favorable que dans le cas des lactones qui ne donnent qu'un seul produit.
Réduction
Les lactones peuvent être réduites en diols en utilisant de l'hydrure de lithium et d'aluminium dans de l'éther sec. La réaction de réduction rompra d'abord la liaison ester de la lactone, puis réduira le groupe aldéhyde (-CHO) en groupe alcool (-OH). Par exemple, les gamma-lactones seront réduites en butane-1,4-diol, (CH 2 (OH)-(CH 2 ) 2 -CH 2 (OH).
Aminolyse
Les lactones réagissent également avec l'ammoniac éthanolique, qui rompra d'abord la liaison ester puis réagira avec le groupe acide -COOH, en raison des propriétés basiques de l'ammoniac, pour former un groupe difonctionnel, c'est-à-dire alcool et amide. Les gamma-lactones réagiront pour donner CH 2 (OH)-(CH 2 ) 2 -CO-NH 2 .
Polymérisation
Les lactones forment facilement des polyesters selon la formule et il a été démontré qu'elles s'oligomérisent également sans catalyseur :
Réaction de Michel
Les lactones sesquiterpéniques , présentes dans de nombreuses plantes, peuvent réagir avec d'autres molécules via une réaction de Michael .
Les usages
Saveurs et parfums
Les lactones contribuent de manière significative à la saveur des fruits et des produits laitiers non fermentés et fermentés, et sont donc utilisées comme arômes et parfums. Quelques exemples sont la γ-décalactone (4-décanolide), qui a une saveur de pêche caractéristique ; δ-décalactone (5-décanolide), qui a une saveur crémeuse de noix de coco/pêche; la γ-dodécalactone (4-dodécanolide), qui a également une saveur de noix de coco/fruitée, une description qui correspond également à la γ-octalactone (4-octanolide), bien qu'elle ait également un caractère herbacé ; γ-nonalactone , qui a une saveur intense de noix de coco de cette série, bien qu'elle ne se trouve pas dans la noix de coco, et γ-undécalactone .
Les lactones macrocycliques ( cyclopentadécanolide , 15-pentadec-11/12-énolide ) ont des odeurs similaires aux cétones macrocycliques d'origine animale ( muscone , civétone ), mais elles peuvent être préparées plus facilement, par exemple, par dépolymérisation des polyesters linéaires correspondants . Le remplacement d'une unité méthylène par l'oxygène affecte à peine l'odeur de ces composés, et des oxalactones avec des cycles de 15 à 17 chaînons sont produits en plus du cyclopentadécanolide (par exemple, 12-oxa-16-hexadécanolide ).
Chimie prébiotique
Il a été démontré que les lactones prébiotiques plausibles, telles que la -caprolactone et la -valérolactone, s'oligomérisent sans l'utilisation de catalyseurs formant des oligomères qui peuvent avoir été pertinents à l' origine de la vie .
Plastiques
La polycaprolactone est un plastique important.
Exemples
γ-butyrolactone (GBL)
- Macrolides
- Kavalactones
dilactones
- Acide ellagique (acide hexahydroxydiphénique dilactone)
- L'acide flavogallonique dilactone peut être trouvé dans les graines de Rhynchosia volubilis et dans Shorea laeviforia
- Lactide
- L'acide tergallique dilactone peut être trouvé dans les graines de Rhynchosia volubilis
- L'acide valonéique dilactone peut être isolé du bois de cœur de Shorea laeviforia
- Brassylate d'éthylène (Musk T), un musc synthétique largement utilisé
Voir également
- Lactame , un amide cyclique
- Lactim , un imide cyclique
- Lactide , un diester cyclique
- Halolactonisation
- Phtaléine