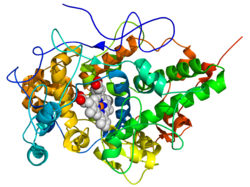
Lactoperoxydase - Lactoperoxidase
La lactoperoxydase est une enzyme peroxydase sécrétée par les glandes mammaires, salivaires et autres muqueuses, y compris les poumons, les bronches et le nez, qui fonctionne comme une première ligne de défense naturelle contre les agents antibactériens et antiviraux. La lactoperoxydase est un membre de la famille des enzymes hème peroxydase . Chez l'homme, la lactoperoxydase est codée par le gène LPO .
La lactoperoxydase catalyse l'oxydation de plusieurs substrats inorganiques et organiques par le peroxyde d'hydrogène . Ces substrats comprennent le bromure et l' iodure et, par conséquent, la lactoperoxydase peut être classée comme une haloperoxydase . Un autre substrat important est le thiocyanate . Les produits oxydés produits par l'action de cette enzyme ont des activités bactéricides et antivirales puissantes et non spécifiques , y compris la destruction du virus de la grippe. La lactoperoxydase avec ses substrats ioniques inorganiques, le peroxyde d'hydrogène et ses produits oxydés est connue sous le nom de système lactoperoxydase . Par conséquent, la LPO est considérée comme une défense très importante contre les bactéries invasives et les agents viraux tels que la grippe et le virus SARS-CoV-2 lorsqu'une quantité suffisante d'iode est fournie.
Le système lactoperoxydase joue un rôle important dans le système immunitaire inné en tuant les bactéries dans le lait et les sécrétions des muqueuses (les revêtements d'origine principalement endodermique, recouverts d'épithélium, qui sont impliqués dans l'absorption et la sécrétion), d'où l'augmentation du système lactoperoxydase peut avoir des applications thérapeutiques. En outre, l'ajout ou l'augmentation du système de lactoperoxydase a des applications potentielles dans le contrôle des bactéries dans les produits alimentaires et de soins de santé destinés aux consommateurs. Le système lactoperoxydase n'attaque pas l'ADN et n'est pas mutagène. Cependant, dans certaines conditions, le système lactoperoxydase peut contribuer au stress oxydatif. De plus, la lactoperoxydase peut contribuer à l'initiation du cancer du sein , grâce à sa capacité à oxyder les hormones œstrogéniques produisant des intermédiaires radicaux libres .
Structure
La structure de la lactoperoxydase se compose principalement d' hélices alpha et de deux courts brins bêta antiparallèles . La lactoperoxydase appartient à la famille des hèmes peroxydases des enzymes de mammifères qui comprend également la myéloperoxydase (MPO), la peroxydase éosinophile (EPO), la peroxydase thyroïdienne (TPO) et la prostaglandine H synthase (PGHS). Un cofacteur hémique est lié près du centre de la protéine.
Fonction
La lactoperoxydase catalyse l'oxydation au peroxyde d'hydrogène (H 2 O 2 ) de plusieurs molécules acceptrices :
- accepteur réduit + H 2 O 2 → accepteur oxydé + H 2 O
Des exemples spécifiques incluent :
- thiocyanate (SCN − ) → hypothiocyanite (OSCN − )
- bromure (Br − ) → hypobromite (BrO − )
- iodure (I − ) → hypoiodite (IO − )
La source du peroxyde d'hydrogène (H 2 O 2 ) est généralement la réaction du glucose avec l' oxygène en présence de l'enzyme glucose oxydase ( EC 1.1.3.4 ) qui a également lieu dans la salive . Le glucose, à son tour, peut être formé à partir de l' amidon en présence de l'enzyme salivaire amyloglucosidase ( EC 3.2.1.3 ).
Ces intermédiaires oxydés à durée de vie relativement courte ont des effets bactéricides puissants , c'est pourquoi la lactoperoxydase fait partie du système de défense antimicrobien dans les tissus qui expriment la lactoperoxydase. Le système lactoperoxydase est efficace pour tuer une gamme de micro-organismes aérobies et certains micro-organismes anaérobies . Recherche (1984) : « L'effet des mélanges lactoperoxydase-thiocyanate-peroxyde d'hydrogène sur les bactéries dépend des conditions expérimentales. Si les bactéries sont cultivées après l'exposition à la lactoperoxydase-thiocyanate-peroxyde d'hydrogène sur une gélose nutritive dans des conditions aérobies, elles peuvent ne pas , alors qu'ils poussent facilement sur gélose au sang dans des conditions anaérobies." Dans sa capacité antimicrobienne, la lactoperoxydase semble agir en synergie avec la lactoferrine et le lysozyme .
Applications
La lactoperoxydase est un agent antimicrobien et antiviral efficace. Par conséquent, des applications de la lactoperoxydase sont trouvées dans la conservation des aliments, des cosmétiques et des solutions ophtalmiques. De plus, la lactoperoxydase a trouvé une application dans le traitement dentaire et des plaies. Enfin, la lactoperoxydase peut trouver une application en tant qu'agents anti-tumoraux et antiviraux. La lactoperoxydase a été utilisée avec de l'iode radioactif pour marquer sélectivement les surfaces membranaires.
Les produits laitiers
La lactoperoxydase est un agent antimicrobien efficace et est utilisée comme agent antibactérien pour réduire la microflore bactérienne dans le lait et les produits laitiers. L'activation du système lactoperoxydase par addition de peroxyde d'hydrogène et de thiocyanate prolonge la durée de conservation du lait cru réfrigéré. Il est assez résistant à la chaleur et est utilisé comme indicateur de surpasteurisation du lait.
Soins bucco-dentaires
Un système de lactoperoxydase est revendiqué comme étant approprié pour le traitement de la gingivite et de la paradentose . La lactoperoxydase a été utilisée dans un dentifrice ou un bain de bouche pour réduire les bactéries buccales et par conséquent l'acide produit par ces bactéries.
Produits de beauté
Une combinaison de lactoperoxydase, de glucose, de glucose oxydase (GOD), d'iodure et de thiocyanate serait efficace pour la conservation des produits cosmétiques.
Cancer
Des conjugués d'anticorps de glucose oxydase et de lactoperoxydase se sont avérés efficaces pour tuer les cellules tumorales in vitro. De plus, les macrophages exposés à la lactoperoxydase sont stimulés pour tuer les cellules cancéreuses.
Signification clinique
Système immunitaire inné
Les activités antibactériennes et antivirales de la lactoperoxydase jouent un rôle important dans le système de défense immunitaire des mammifères ; le système lactoperoxydase est considéré comme la première ligne de défense contre les bactéries et les agents viraux en suspension dans l'air. Il est important de noter que la lactoperoxydase est également extrudée dans les poumons, les bronches et le mucus nasal.
L'hypothiocyanite est l'un des intermédiaires réactifs produits par l'activité de la lactoperoxydase sur le thiocyanate et le peroxyde d'hydrogène produits par les protéines double oxydase 2 , également connues sous le nom de Duox2. La sécrétion de thiocyanate chez les patients atteints de mucoviscidose est diminuée, ce qui entraîne une production réduite d'hypothiocyanite antimicrobien et contribue par conséquent à un risque accru d'infection des voies respiratoires.
Infections virales
L'acide hypoiodique (HOI) généré par la peroxydase, l'hypoiodite et l'hypothiocyanite détruisent tous le virus de l' herpès simplex et le virus de l'immunodéficience humaine . L'hypothiocyanite et les produits ioniques hypoiodate sont des oxydants antiviraux très puissants et surtout non spécifiques qui sont mortels, même à de faibles concentrations, pour le virus de la grippe. L'activité antivirale de la lactoperoxydase est renforcée avec des concentrations croissantes d'ions iodure. Cette enzyme s'est avérée efficace contre un virus à ARN hautement dangereux et résistant (poliovirus) et un virus à ADN à longue durée de vie (vaccin).
Infections bactériennes
Il a été démontré que le système duox2-lactoperoxydase offre une protection contre plusieurs dizaines de bactéries et de mycoplasmes, y compris des variétés du Staphylococcus cliniquement important et de nombreux types de Streptococcus . Le système lactoperoxydase inhibe efficacement le Helicobacter pylori commun dans le tampon ; cependant, dans la salive humaine entière, il semble avoir un effet plus faible contre ce microbe. Il a été montré que la lactoperoxydase en présence de thiocyanure peut catalyser les effets bactéricides et cytotoxiques du peroxyde d'hydrogène dans des conditions spécifiques lorsque le peroxyde d'hydrogène est présent en excès de thiocyanure. La combinaison de lactoperoxydase, de peroxyde d'hydrogène et de thiocyanure est beaucoup plus efficace que le peroxyde d'hydrogène seul pour inhiber le métabolisme et la croissance des bactéries.
Cancer du sein
L'oxydation de l' estradiol par la lactoperoxydase est une source possible de stress oxydatif dans le cancer du sein . La capacité de la lactoperoxydase à propager une réaction en chaîne conduisant à une consommation d'oxygène et à une accumulation intracellulaire de peroxyde d'hydrogène pourrait expliquer les lésions de la base de l'ADN induites par les radicaux hydroxyles récemment signalées dans les tissus du cancer du sein féminin. La lactoperoxydase pourrait être impliquée dans la carcinogenèse mammaire, en raison de sa capacité à interagir avec les hormones œstrogéniques et à les oxyder à travers deux étapes de réaction à un électron. La lactoperoxydase réagit avec le cycle A phénolique des œstrogènes pour produire des radicaux libres réactifs . De plus, la lactoperoxydase peut activer les amines aromatiques et hétérocycliques cancérigènes et augmenter les niveaux de liaison des produits activés à l'ADN, ce qui suggère un rôle potentiel de l'activation catalysée par la lactoperoxydase des cancérogènes dans la causalité du cancer du sein.
Soins bucco-dentaires
Au cours des dernières décennies, plusieurs études cliniques décrivant l'efficacité clinique du système lactoperoxydase dans une variété de produits d'hygiène bucco-dentaire (dentifrices, bains de bouche) ont été publiées. Après avoir montré indirectement, en mesurant les paramètres expérimentaux de la gingivite et des caries , que les bains de bouche contenant de l'amyloglucosidase (γ- amylase ) et de la glucose oxydase activent le système lactoperoxydase, le mécanisme protecteur des enzymes dans les produits d'hygiène bucco-dentaire a été partiellement élucidé. Des enzymes telles que le lysozyme , la lactoperoxydase et la glucose oxydase sont transférées des dentifrices à la pellicule . Étant des composants de la pellicule, ces enzymes sont catalytiquement très actives. Aussi, dans le cadre des dentifrices, le système lactoperoxydase a une influence bénéfique pour éviter les caries de la petite enfance en réduisant le nombre de colonies formées par la microflore cariogène tout en augmentant la concentration en thiocyanate. Chez les patients atteints de xérostomie , les dentifrices avec le système lactoperoxydase sont apparemment supérieurs aux dentifrices contenant du fluor en ce qui concerne la formation de plaque et la gingivite. D'autres études sont nécessaires pour examiner plus avant les mécanismes de protection.
L'application de la lactoperoxydase n'est pas limitée aux caries, à la gingivite et à la parodontite . Une combinaison de lysozyme et de lactoperoxydase peut être appliquée pour soutenir le traitement du syndrome de la bouche brûlante ( glosodynie ). En association avec la lactoferrine, la lactoperoxydase combat l' halitose ; en combinaison avec la lactoferrine et le lysozyme, la lactoperoxydase aide à améliorer les symptômes de la xérostomie. De plus, les gels contenant de la lactoperoxydase aident à améliorer les symptômes du cancer de la bouche lorsque la production de salive est compromise en raison de l'irradiation. Dans ce cas, la flore bactérienne buccale est également influencée favorablement.
Voir également
Les références
Lectures complémentaires
- Galijasevic S, Saed GM, Diamond MP, Abu-Soud HM (septembre 2004). « Constante de vitesse de dissociation élevée du complexe ferreux-dioxy lié à l'activité de type catalase dans la lactoperoxydase » . Le Journal de Chimie Biologique . 279 (38) : 39465–70. doi : 10.1074/jbc.M406003200 . PMID 15258136 . S2CID 30280587 .
- Ekstrand B (1994). « Lactoperoxydase et lactoferrine ». Dans Beuchat LR, Dillon VM, Board RG (éd.). Systèmes antimicrobiens naturels et conservation des aliments . Oxon : CAB International. ISBN 978-0-85198-878-8.
- Kussendrager KD, van Hooijdonk AC (novembre 2000). "Lactoperoxydase : propriétés physico-chimiques, occurrence, mécanisme d'action et applications" . Le Journal britannique de la nutrition . 84 (Suppl. 1) : S19-25. doi : 10.1017/S0007114500002208 . PMID 11242442 .
- Thomas EL, Pera KA, Smith KW, Chwang AK (février 1983). "Inhibition de Streptococcus mutans par le système antimicrobien lactoperoxydase" . Infection et immunité . 39 (2) : 767–78. doi : 10.1128/IAI.39.2.767-778.1983 . PMC 348016 . PMID 6832819 .
- Korhonen H, Meriläinen V, Antila M, Kouvalainen K (1980). "[Facteurs antimicrobiens dans le lait et résistance aux infections chez les nourrissons]". Duodécim ; Laaketieteellinen Aikakauskirja (en finnois). 96 (3) : 184-99. PMID 7192622 .
- Oram JD, Reiter B (août 1966). "L'inhibition des streptocoques par la lactoperoxydase, le thiocyanate et le peroxyde d'hydrogène. L'effet du système inhibiteur sur les souches sensibles et résistantes des streptocoques du groupe N" . Le Journal Biochimique . 100 (2) : 373-81. doi : 10.1042/bj1000373 . PMC 1265145 . PMID 4290983 .
- Oram JD, Reiter B (août 1966). "L'inhibition des streptocoques par la lactoperoxydase, le thiocyanate et le peroxyde d'hydrogène. L'oxydation du thiocyanate et la nature du composé inhibiteur" . Le Journal Biochimique . 100 (2) : 382-8. doi : 10.1042/bj1000382 . PMC 1265146 . PMID 5338806 .
- Hannuksela S, Tenovuo J, Roger V, Lenander-Lumikari M, Ekstrand J (1994). « Le fluorure inhibe les systèmes de peroxydase antimicrobienne dans la salive entière humaine ». Recherche sur les caries . 28 (6) : 429–34. doi : 10.1159/000262016 . PMID 7850846 .
- Aune TM, Thomas EL (mars 1978). « L'oxydation des protéines sulfhydryles par les produits de l'oxydation catalysée par la peroxydase de l'ion thiocyanate ». Biochimie . 17 (6) : 1005-10. doi : 10.1021/bi00599a010 . PMID 204336 .
- Ekstrand B, Mullan WM, Waterhouse A (juin 1985). « Inhibition du système antibactérien Lactoperoxydase-Thiocyanate-Peroxyde d'hydrogène par le lait traité thermiquement ». Journal de la protection des aliments . 48 (6) : 494-498. doi : 10.4315/0362-028X-48.6.494 . PMID 30943594 .
- Reiter B, Härnulv G (septembre 1984). "Système antibactérien de lactoperoxydase : occurrence naturelle, fonctions biologiques et applications pratiques". Journal de la protection des aliments . 47 (9) : 724-732. doi : 10.4315/0362-028X-47.9.724 . PMID 30934451 .
Liens externes
- Lactoperoxydase à la National Library of Medicine Medical Subject Headings (MeSH) des États-Unis