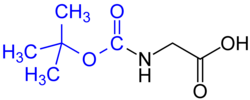
Groupe protecteur - Protecting group

Un groupe protecteur ou un groupe protecteur est introduit dans une molécule par modification chimique d'un groupe fonctionnel pour obtenir une chimiosélectivité dans une réaction chimique ultérieure. Il joue un rôle important dans la synthèse organique en plusieurs étapes .
Dans de nombreuses préparations de composés organiques délicats, certaines parties spécifiques de leurs molécules ne peuvent pas survivre aux réactifs ou aux environnements chimiques requis. Ensuite, ces parties, ou groupes, doivent être protégés . Par exemple, l'hydrure de lithium et d'aluminium est un réactif hautement réactif mais utile capable de réduire les esters en alcools . Il réagira toujours avec les groupes carbonyle , et cela ne peut être découragé par aucun moyen. Lorsqu'une réduction d'un ester est requise en présence d'un carbonyle, l'attaque de l'hydrure sur le carbonyle doit être évitée. Par exemple, le carbonyle est transformé en un acétal , qui ne réagit pas avec les hydrures. L'acétal est alors appelé groupe protecteur pour le carbonyle. Une fois l'étape impliquant l'hydrure terminée, l'acétal est éliminé (en le faisant réagir avec un acide aqueux), restituant le carbonyle d'origine. Cette étape est appelée déprotection .
Les groupes protecteurs sont plus couramment utilisés dans les travaux de laboratoire à petite échelle et le développement initial que dans les processus de production industrielle, car leur utilisation ajoute des étapes supplémentaires et des coûts matériels au processus. Cependant, la disponibilité d'un bloc de construction chiral bon marché peut surmonter ces coûts supplémentaires (par exemple, l'acide shikimique pour l' oseltamivir ).
Groupes protecteurs communs
Groupes de protection contre l'alcool
Protection des alcools :
- Acétyle (Ac) - Éliminé par un acide ou une base (voir groupe acétoxy ).
- Benzoyle (Bz) - Éliminé par un acide ou une base, plus stable que le groupe Ac.
- Benzyle (Bn) – Éliminé par hydrogénolyse . Le groupe Bn est largement utilisé dans la chimie des sucres et des nucléosides.
- Éther -méthoxyéthoxyméthylique (MEM) – Éliminé par l'acide.
- Diméthoxytrityle, [bis-(4-méthoxyphényl)phénylméthyl] (DMT) – Éliminé par un acide faible. Le groupe DMT est largement utilisé pour la protection du groupe 5'-hydroxy dans les nucléosides, en particulier dans la synthèse d'oligonucléotides .
- Éther méthoxyméthylique (MOM) – Éliminé par l'acide.
- Méthoxytrityle [(4-méthoxyphényl)diphénylméthyl] (MMT) – Éliminé par acide et hydrogénolyse.
- Éther p- méthoxybenzylique (PMB) – Éliminé par acide, hydrogénolyse ou oxydation – généralement avec le DDQ .
- p -Éther méthoxyphénylique (PMP) – Éliminé par oxydation.
- Éther méthylthiométhylique – Éliminé par l'acide.
- Pivaloyl (Piv) – Éliminé par des agents acides, basiques ou réducteurs. Il est sensiblement plus stable que les autres groupes protecteurs d'acyle.
- Tétrahydropyranyle (THP) – Éliminé par l'acide.
- Tétrahydrofurane (THF) – Éliminé par l'acide.
- Trityl (triphénylméthyle, Tr) – Éliminé par acide et hydrogénolyse.
- Éther de silyle (les plus populaires incluent le triméthylsilyle (TMS), tert- butyldiméthylsilyle (TBDMS ou TBS),tri- iso -propylsilyloxymethyl (TOM), et les éthers triisopropylsilyle (TIPS)) - éliminé par l' acide ou le fluorure ionique. (tels que NaF, TBAF ( fluorure de tétra- n- butylammonium , HF-Py ou HF-NEt 3 )). Les groupes TBDMS et TOM sont utilisés pour la protection de la fonction 2'-hydroxy dans les nucléosides, en particulier dans la synthèse d'oligonucléotides .
- Ethers méthyliques – Le clivage se fait par TMSI dans du dichlorométhane ou de l'acétonitrile ou du chloroforme. Une méthode alternative pour cliver les éthers méthyliques est le BBr 3 dans le DCM
- Ethoxyethyl ethers (EE) - Clivage plus trivial que les éthers simples, par exemple l'acide chlorhydrique 1N
Groupes protecteurs d'amine
Protection des amines :
- Groupe carbobenzyloxy (Cbz) – Éliminé par hydrogénolyse
- Groupe p- méthoxybenzyl carbonyle (Moz ou MeOZ) – Éliminé par hydrogénolyse , plus labile que Cbz
- Groupe tert- butyloxycarbonyle (BOC) (commun dans la synthèse de peptides en phase solide ) – Éliminé par un acide fort concentré (tel que HCl ou CF 3 COOH), ou par chauffage à >80 °C.
- Groupe 9-Fluorénylméthyloxycarbonyle ( Fmoc ) (commun dans la synthèse peptidique en phase solide ) - Supprimé par une base, telle que la pipéridine
- Acétyle (Ac)Le groupe est commun dans la synthèse d'oligonucléotides pour la protection de N4 dans la cytosine et de N6 dans les bases nucléiques adénine et est éliminé par traitement avec une base, le plus souvent, avec de l' ammoniaque ou de la méthylamine aqueux ou gazeux . Ac est trop stable pour être facilement éliminé des amides aliphatiques.
- Benzoyle (Bz)Le groupe est commun dans la synthèse d'oligonucléotides pour la protection de N4 dans la cytosine et de N6 dans les bases nucléiques d' adénine et est éliminé par traitement avec une base, le plus souvent avec de l'ammoniaque ou de la méthylamine aqueux ou gazeux. Bz est trop stable pour être facilement éliminé des amides aliphatiques.
- Groupe benzyle (Bn) - Éliminé par hydrogénolyse
- Groupe carbamate – Éliminé par un chauffage acide et doux.
- p -Méthoxybenzyle (PMB) – Éliminé par hydrogénolyse , plus labile que le benzyle
- 3,4- Diméthoxybenzyl (DMPM) – Éliminé par hydrogénolyse , plus labile que le p- méthoxybenzyl
- Groupe p- méthoxyphényle (PMP) – Éliminé par le nitrate d'ammonium et de cérium(IV) (CAN)
- Groupe Tosyl (Ts) - Éliminé par l'acide concentré (HBr, H 2 SO 4 ) et les agents réducteurs puissants ( sodium dans l' ammoniac liquide ou naphtaléniure de sodium )
- Groupe Troc (chloroformiate de trichloroéthyle) - Supprimé par insertion de Zn en présence d'acide acétique
- Autres groupes sulfonamides (Nosyl et Nps) - Éliminés par l' iodure de samarium , le thiophénol ou d'autres nucléophiles thiols mous, ou l'hydrure de tributylétain
Groupes protecteurs carbonyle
Protection des groupes carbonyle :
- Acétals et cétals – Éliminés par l'acide. Normalement, le clivage des acétals acycliques est plus facile que celui des acétals cycliques.
- Acylals – Supprimés par les acides de Lewis .
- Dithianes – Éliminés par des sels métalliques ou des agents oxydants.
Groupes protecteurs d'acide carboxylique
Protection des acides carboxyliques :
- Esters méthyliques – Éliminés par un acide ou une base.
- Esters benzyliques – Éliminés par hydrogénolyse.
- tert -Esters butyliques – Éliminés par l'acide, la base et certains réducteurs.
- Esters de phénols 2,6-disubstitués (par exemple 2,6-diméthylphénol , 2,6-diisopropylphénol , 2,6-di- tert -butylphénol ) – Éliminés à température ambiante par méthanolyse catalysée par DBU dans des conditions de haute pression.
- Esters de silyle – Éliminés par les réactifs acides, basiques et organométalliques .
- Orthoesters - Supprimés par un acide aqueux doux pour former un ester, qui est éliminé en fonction des propriétés de l'ester.
- Oxazoline - Éliminé par un acide fort chaud (pH < 1, T > 100 °C) ou un alcali (pH > 12, T > 100 °C), mais pas par exemple LiAlH 4 , les réactifs organolithiens ou les réactifs Grignard (organomagnésiens)
Groupes protecteurs de phosphate
- 2-cyanoéthyle– enlevé par une base douce. Le groupe est largement utilisé dans la synthèse d'oligonucléotides .
- Méthyle (Me)– éliminé par les nucléophiles forts ec . thiophénole/THÉ.
Groupes protecteurs d'alcyne terminaux
- Alcools propargyliques dans la réaction de Favorskii ,
- Groupes silyles, en particulier dans la protection de l' acétylène lui-même.
Autre
Protection orthogonale

La protection orthogonale est une stratégie permettant la déprotection spécifique d'un groupe protecteur dans une structure multiprotégée sans affecter les autres. Par exemple, l'acide aminé tyrosine pourrait être protégé sous la forme d'un ester benzylique sur le groupe carboxyle, d'un carbamate de fluorénylméthylèneoxy sur le groupe amine et d'un éther tert- butylique sur le groupe phénol. L'ester benzylique peut être éliminé par hydrogénolyse, le groupe fluorénylméthylénoxy (Fmoc) par des bases (telles que la pipéridine) et l' éther tert- butylique phénolique clivé avec des acides (par exemple avec de l'acide trifluoroacétique).
Un exemple courant pour cette application, la synthèse Fmoc-peptide, dans laquelle les peptides sont cultivés en solution et sur phase solide, est très importante. Les groupes protecteurs dans la synthèse en phase solide en ce qui concerne les conditions de réaction telles que le temps de réaction, la température et les réactifs peuvent être standardisés de sorte qu'ils soient effectués par une machine, tandis que des rendements bien supérieurs à 99% peuvent être atteints. Sinon, la séparation du mélange résultant de produits de réaction est pratiquement impossible.
La technique a été introduite dans le domaine de la synthèse peptidique par Robert Bruce Merrifield en 1977. Comme preuve de concept, la déprotection orthogonale est démontrée dans une transestérification photochimique par le triméthylsilyldiazométhane utilisant l' effet isotopique cinétique :
En raison de cet effet, le rendement quantique pour la déprotection du groupe ester du côté droit est réduit et il reste intact. De manière significative, en plaçant les atomes de deutérium à côté du groupe ester du côté gauche ou en changeant la longueur d'onde à 254 nm, l'autre monoarène est obtenu.
Critique
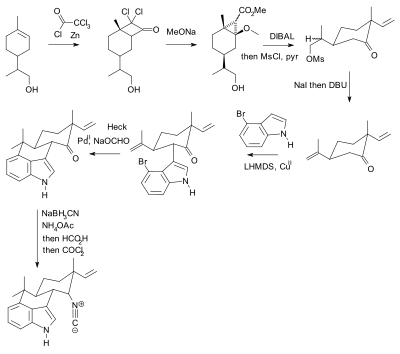
L'utilisation de groupes protecteurs est omniprésente mais non sans critique. En termes pratiques, leur utilisation ajoute deux étapes (séquence de protection-déprotection) à une synthèse, l'une ou les deux pouvant considérablement réduire le rendement chimique . Surtout, la complexité accrue empêche l'utilisation de la synthèse totale synthétique dans la découverte de médicaments . En revanche, la synthèse biomimétique n'emploie pas de groupes protecteurs. Comme alternative, Baran a présenté une nouvelle synthèse sans groupe protecteur du composé hapalindole U. La synthèse précédemment publiée selon Baran, contenait 20 étapes avec plusieurs manipulations de groupe protecteur (deux confirmées) :
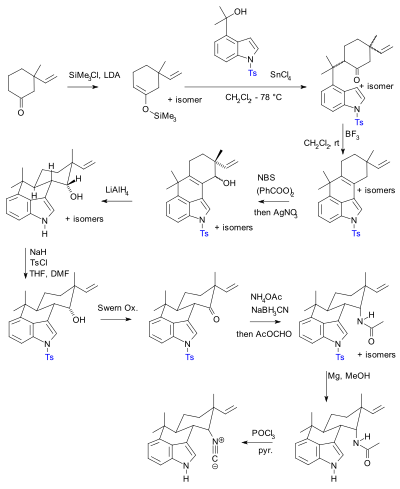
Hideaki Muratake est la synthèse 1990 en utilisant tosyle groupes protecteurs (en bleu).
|
Applications industrielles
Bien que l'utilisation de groupes protecteurs ne soit pas préférée dans les synthèses industrielles, ils sont toujours utilisés dans des contextes industriels, par exemple :
- Synthèse de l'oseltamivir (Tamiflu, un médicament antiviral) par Roche
- Sucralose (édulcorant)
Les références
Liens externes
- Introduction du groupe protecteur et mécanisme de déprotection
- Notes d'étude de premier cycle sur ce sujet, du professeur Rizzo.
- Un autre ensemble de notes d'étude sous forme de tutoriel, avec des conseils et des commentaires, des Profs. Grossman et Cammers.
- Une critique par le professeur Kocienski.
- Un site utilisateur extrait du texte classique de Greene et Wuts concernant la stabilité de quelques groupes clés, à partir des tableaux détaillés de cette référence.
- Protection du groupe contre organic-reaction.com