Réglementation - Regelation
La régulation est le phénomène de fonte de la glace sous pression et de regel lorsque la pression est réduite. Nous pouvons démontrer la régélation en enroulant un fil fin autour d'un bloc de glace, auquel est attaché un poids lourd. La pression exercée sur la glace la fait fondre lentement localement, permettant au fil de traverser tout le bloc. La piste du fil se remplira dès que la pression sera relâchée, de sorte que le bloc de glace restera solide même après le passage complet du fil. Cette expérience est possible pour la glace à -10 °C ou moins, et bien qu'essentiellement valable, les détails du processus par lequel le fil traverse la glace sont complexes. Le phénomène fonctionne mieux avec des matériaux à haute conductivité thermique tels que le cuivre, car la chaleur latente de fusion de la face supérieure doit être transférée vers la face inférieure pour fournir la chaleur latente de fusion. En bref, le phénomène dans lequel la glace se transforme en liquide en raison de la pression appliquée, puis se reconvertit en glace une fois la pression supprimée s'appelle la regélation.
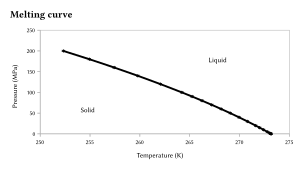
La Régélation a été découverte par Michael Faraday . Il ne se produit que pour des substances telles que la glace, qui ont la propriété de se dilater lors de la congélation, car les points de fusion de ces substances diminuent avec l'augmentation de la pression extérieure. Le point de fusion de la glace chute de 0,0072 °C pour chaque atm de pression supplémentaire appliqué. Par exemple, une pression de 500 atmosphères est nécessaire pour que la glace fonde à -4 °C.
Fonte superficielle
Pour une glace cristalline normale bien en dessous de son point de fusion, il y aura une certaine relaxation des atomes près de la surface. Des simulations de glace près de son point de fusion montrent qu'il y a une fusion significative des couches de surface plutôt qu'une relaxation symétrique des positions des atomes. La résonance magnétique nucléaire a fourni la preuve d'une couche liquide à la surface de la glace. En 1998, en utilisant la microscopie à force atomique , Astrid Döppenschmidt et Hans-Jürgen Butt ont mesuré l'épaisseur de la couche liquide sur la glace à environ 32 nm à -1 °C et 11 nm à -10 °C.
La fusion de surface peut expliquer ce qui suit :
- Faible coefficient de friction de la glace, tel qu'expérimenté par les patineurs.
- Facilité de compactage de la glace
- Haute adhérence des surfaces glacées
Exemples de régélation
Un glacier peut exercer une pression suffisante sur sa surface inférieure pour abaisser le point de fusion de sa glace. La fonte de la glace à la base du glacier lui permet de passer d'une altitude plus élevée à une altitude plus basse. L'eau liquide peut s'écouler de la base d'un glacier à des altitudes inférieures lorsque la température de l'air est supérieure au point de congélation de l'eau.
Idées fausses
Le patinage sur glace est donné comme exemple de régélation; cependant, la pression requise est bien supérieure au poids d'un patineur. De plus, la regelation n'explique pas comment on peut patiner à des températures inférieures à zéro (0°C).
Le compactage et la création de boules de neige est un autre exemple de textes anciens. Ici, la pression requise est bien supérieure à la pression qui peut être appliquée à la main. Un contre-exemple est que les voitures ne font pas fondre la neige lorsqu'elles roulent dessus.
Derniers progrès
Une peau ultrasolide , élastique, hydrophobe, thermiquement plus stable recouvre à la fois l'eau et la glace. Les peaux d'eau et de glace sont caractérisées par des phonons d'étirement HO identiques de 3450 cm^-1. Ni le cas des formes liquides sur la glace ni la couche de glace ne recouvrent l'eau, mais la peau supersolide glisse la glace et durcit la peau de l'eau
Relaxation de la liaison hydrogène (O:HO) sous compression. La compression raccourcit et raidit la non-liaison O:H et allonge et adoucit simultanément la liaison covalente HO et l'effet de pression négative à l'opposé
Le point de fusion est proportionnel à l'énergie de cohésion de la liaison covalente. Par conséquent, la compression abaisse la Tm.
Lectures complémentaires
- Y. Huang, X. Zhang, Z. Ma, Y. Zhou, W. Zheng, J. Zhou et CQ Sun, Dynamique de relaxation des liaisons hydrogène : résoudre les mystères de la glace d'eau. Coordination Chemistry Reviews 2015. 285 : 109-165.
- CQ Sun, Relaxation de la liaison chimique. Série Springer en Physique Chimique 108. Vol. 108. 2014 Heidelberg, 807 pages ISBN 978-981-4585-20-0 .