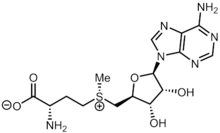
S -Adénosyl méthionine - S-Adenosyl methionine
|
|||
|
|
|||
| Noms | |||
|---|---|---|---|
|
Nom IUPAC préféré
(2 S )-2-Amino-4-[( S )-{[(2 S ,3 S ,4 R ,5 R )-5-(4-amino-9 H -purin-9-yl)-3 ,4-dihydroxyoxolan-2-yl]méthyl}méthylsulfaniumyl]butanoate |
|||
| Autres noms
S- Adénosyl- L- méthionine; Même; SAMe, AdoMet , Heparab (Inde), adéméthionine
|
|||
| Identifiants | |||
|
Modèle 3D ( JSmol )
|
|||
| ChEMBL | |||
| ChemSpider | |||
| Carte d'information de l'ECHA |
100.045.391 |
||
| KEGG | |||
| Engrener | S-Adénosylméthionine | ||
|
CID PubChem
|
|||
| UNII | |||
|
Tableau de bord CompTox ( EPA )
|
|||
|
|||
|
|||
| Propriétés | |||
| C 15 H 22 N 6 O 5 S | |||
| Masse molaire | 398,44 g·mol -1 | ||
| Pharmacologie | |||
| A16AA02 ( OMS ) | |||
|
Sauf indication contraire, les données sont données pour les matériaux dans leur état standard (à 25 °C [77 °F], 100 kPa). |
|||
|
|
|||
| Références de l'infobox | |||
La S- adénosyl méthionine ( SAM-e ) est un cosubstrat communimpliqué dans les transferts de groupes méthyle , la transsulfuration et l'aminopropylation. Bien que cesréactions anaboliques se produisent dans tout le corps, la plupart des SAM-e sont produites et consommées dans le foie. Plus de 40 transferts de méthyle de SAM-e sont connus vers divers substrats tels que les acides nucléiques , les protéines , les lipides et les métabolites secondaires . Il est fabriqué à partir d' adénosine triphosphate (ATP) et de méthionine par la méthionine adénosyltransférase . SAM-e a été découvert pour la première fois par Giulio Cantoni en 1952.
Chez les bactéries, SAM-e est lié par le riboswitch SAM , qui régule les gènes impliqués dans la biosynthèse de la méthionine ou de la cystéine . Dans les cellules eucaryotes, SAM-e sert de régulateur à divers processus, notamment la méthylation de l'ADN, de l'ARNt et de l'ARNr ; réponse immunitaire; métabolisme des acides aminés; transsulfuration ; et plus. Chez les plantes, la SAM-e est cruciale pour la biosynthèse de l' éthylène , une hormone végétale importante et une molécule de signalisation.
Chimiquement, c'est une bétaïne sulfonium qui sert de source de groupe méthyle électrophile ou de source de radical 5'-désoxyadénosyle.
Biochimie
Cycle SAM-e
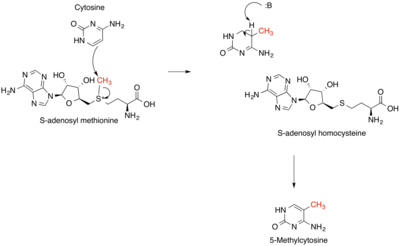
Les réactions qui produisent, consomment et régénèrent SAM-e sont appelées le cycle SAM-e. Dans la première étape de ce cycle, les méthylases dépendantes de la SAM (EC 2.1.1) qui utilisent la SAM-e comme substrat produisent la S- adénosyl homocystéine en tant que produit. La S- Adénosyl homocystéine est un puissant régulateur négatif de presque toutes les méthylases SAM dépendantes malgré leur diversité biologique. Ceci est hydrolysé à l' homocystéine et l' adénosine par S -adenosylhomocysteine hydrolase EC 3.3.1.1 et l'homocystéine recyclé vers la méthionine par le transfert d'un groupe méthyle à partir de 5-méthyltétrahydrofolate , par l' une des deux classes de synthases de methionine (c. -à- cobalamine - dépendante ( EC 2.1.1.13 ) ou indépendant de la cobalamine ( EC 2.1.1.14 )). Cette méthionine peut ensuite être reconvertie en SAM-e, complétant ainsi le cycle. Dans l'étape limitante du cycle SAM, la MTHFR (méthylènetétrahydrofolate réductase) réduit de manière irréversible le 5,10-méthylènetétrahydrofolate en 5-méthyltétrahydrofolate.
Enzymes radicales SAM-e
Un grand nombre d'enzymes contenant des amas fer-soufre clivent SAM-e de manière réductrice pour produire un radical 5'-désoxyadénosyle 5' en tant qu'intermédiaire, et sont appelées enzymes SAM radicales . La plupart des enzymes ayant cette capacité partagent une région d'homologie de séquence qui inclut le motif CxxxCxxC ou un variant proche. L'intermédiaire radical permet aux enzymes d'effectuer une grande variété de réactions chimiques inhabituelles. Des exemples d'enzymes SAM radicales comprennent la lyase de photoproduit de spores , les activases de pyruvate formiate lyase et de sulfatases anaérobies, la lysine 2,3-aminomutase et diverses enzymes de biosynthèse de cofacteur, de modification de peptide, de formation de clusters de métalloprotéines , de modification d' ARNt , de métabolisme lipidique, etc. Les enzymes SAM-e utilisent un deuxième SAM-e comme donneur de méthyle. Les enzymes SAM radicales sont beaucoup plus abondantes dans les bactéries anaérobies que dans les organismes aérobies. Ils peuvent être trouvés dans tous les domaines de la vie et sont largement inexplorés. Une étude bioinformatique récente a conclu que cette famille d'enzymes comprend au moins 114 000 séquences comprenant 65 réactions uniques.
Biosynthèse des polyamines
Un autre rôle majeur de SAM-e est dans la biosynthèse des polyamines . Ici, SAM-e est décarboxylée par l' adénosylméthionine décarboxylase ( EC 4.1.1.50 ) pour former la S- adénosylméthioninamine . Ce composé donne alors son groupement n-propylamine dans la biosynthèse de polyamines telles que la spermidine et la spermine à partir de la putrescine .
SAM-e est nécessaire à la croissance et à la réparation cellulaires. Il est également impliqué dans la biosynthèse de plusieurs hormones et neurotransmetteurs qui affectent l'humeur, comme l' épinéphrine . Les méthyltransférases sont également responsables de l'ajout de groupes méthyle aux hydroxyles 2' des premier et deuxième nucléotides à côté de la coiffe 5' dans l'ARN messager .
Utilisations thérapeutiques
En 2012, les preuves n'étaient pas concluantes quant à savoir si SAM pouvait atténuer la douleur de l' arthrose ; les essais cliniques qui avaient été menés étaient trop petits pour généraliser.
Le cycle SAM-e est étroitement lié au foie depuis 1947, car les personnes atteintes de cirrhose alcoolique du foie accumuleraient de grandes quantités de méthionine dans leur sang. Alors que plusieurs sources de données issues de tests de laboratoire sur des cellules et des modèles animaux suggèrent que la SAM pourrait être utile pour traiter diverses maladies du foie , en 2012, la SAM n'avait été étudiée dans aucun grand essai clinique randomisé contrôlé par placebo qui permettrait d'évaluer son efficacité. et la sécurité.
Dépression
Une revue Cochrane de 2016 a conclu que pour le trouble dépressif majeur , « étant donné l'absence de preuves de haute qualité et l'incapacité de tirer des conclusions fermes sur la base de ces preuves, l'utilisation de la SAMe pour le traitement de la dépression chez les adultes devrait être étudiée plus avant. »
Une revue systématique de 2020 n'a trouvé aucun résultat statistiquement différent comparant la SAMe et d'autres antidépresseurs couramment utilisés (imipramine ou escitalopram).
Pharmacocinétique
La SAM orale atteint des concentrations plasmatiques maximales trois à cinq heures après l'ingestion d'un comprimé entérosoluble (400 à 1 000 mg). La demi-vie est d'environ 100 minutes.
Effets indésirables
Des troubles gastro-intestinaux, une dyspepsie et une anxiété peuvent survenir avec la consommation de SAM. Les effets à long terme sont inconnus. SAM est un agent alkylant faible de l'ADN .
Un autre effet secondaire rapporté de SAM est l' insomnie ; par conséquent, le supplément est souvent pris le matin. D'autres rapports d'effets secondaires légers incluent le manque d'appétit, la constipation, les nausées, la bouche sèche, la transpiration et l'anxiété/la nervosité, mais dans les études contrôlées par placebo, ces effets secondaires se produisent à peu près à la même incidence dans les groupes placebo.
Il a récemment été démontré que SAM-e joue un rôle dans la régulation épigénétique . La méthylation de l'ADN est un régulateur clé de la modification épigénétique au cours du développement et de la différenciation des cellules de mammifères. Dans les modèles murins, des niveaux excessifs de SAM-e ont été impliqués dans des schémas de méthylation erronés associés à la neuropathie diabétique. SAM-e sert de donneur de méthyle dans la méthylation de la cytosine, qui est un processus de régulation épigénétique clé. En raison de cet impact sur la régulation épigénétique, SAM-e a été testé comme traitement anticancéreux. La prolifération des cellules cancéreuses dépend de faibles niveaux de méthylation de l'ADN. Il a été démontré que l'addition in vitro reméthyle les séquences promotrices et diminue la production de proto-oncogènes.
Des déficiences en enzymes SAM-e radicales ont été associées à diverses maladies, notamment les cardiopathies congénitales , la sclérose latérale amyotrophique et une susceptibilité virale accrue.
Interactions et contre-indications
La prise de SAM en même temps que certains médicaments peut augmenter le risque de syndrome sérotoninergique , une maladie potentiellement dangereuse causée par un excès de sérotonine. Ces médicaments comprennent le dextrométhorphane (Robitussin), la mépéridine (Demerol), la pentazocine (Talwin) et le tramadol (Ultram).
SAM peut également interagir avec des médicaments antidépresseurs - y compris le tryptophane et Hypericum perforatum (millepertuis) - augmentant le potentiel de syndrome sérotoninergique ou d'autres effets secondaires, et peut réduire l'efficacité de la lévodopa pour la maladie de Parkinson.
Les personnes atteintes de trouble bipolaire ne devraient pas utiliser la MAS car elle augmente le risque d'épisodes maniaques.
Disponibilité dans différents pays
Aux États-Unis et au Canada , SAM est vendu comme complément alimentaire sous le nom commercial SAM-e (également orthographié SAME ou SAMe ; prononcé « Sammy » ;) il a été introduit aux États-Unis en 1999, après le supplément diététique Santé et Éducation. La loi a été adoptée en 1994.
Il a été introduit comme médicament d'ordonnance en Italie en 1979, en Espagne en 1985 et en Allemagne en 1989; à partir de 2012, il a été commercialisé comme médicament d'ordonnance en Russie, en Inde, en Chine, en Italie, en Allemagne, au Vietnam et au Mexique.
Voir également
- ADN méthyltransférase
- riboswitch SAM-I
- Riboswitch SAM-II
- riboswitch SAM-III
- riboswitch SAM-IV
- riboswitch SAM-V
- Riboswitch SAM-VI
- Liste des antidépresseurs expérimentaux
Les références
Liens externes
- Numéro EINECS 249-946-8
- Shippy, R Andrew; Mendez, Douglas; Jones, Kristina; Cergnul, Irène ; Karpiak, Stephen E (2004). " S- Adenosylmethionine (SAM-e) pour le traitement de la dépression chez les personnes vivant avec le VIH/SIDA" . BMC Psychiatrie . 4 : 38. doi : 10.1186/1471-244X-4-38 . PMC 535560 . PMID 15538952 .