Iodure de thallium (I) - Thallium(I) iodide
|
|
| Noms | |
|---|---|
| Autres noms
Monoïodure de thallium Iodure thalleux |
|
| Identifiants | |
|
Modèle 3D ( JSmol )
|
|
| ChemSpider | |
| Carte Info ECHA |
100.029.272 |
|
PubChem CID
|
|
| UNII | |
|
Tableau de bord CompTox ( EPA )
|
|
|
|
|
|
| Propriétés | |
| TlI | |
| Masse molaire | 331,287 g / mol |
| Apparence | cristaux jaunes |
| Densité | 7,1 g / cm 3 |
| Point de fusion | 441,7 ° C (827,1 ° F; 714,8 K) |
| Point d'ébullition | 824 ° C (1 515 ° F; 1 097 K) |
| 0,085 g / L (25 ° C) | |
| Solubilité | insoluble dans l' alcool |
| −82,2 · 10 −6 cm 3 / mol | |
| Dangers | |
|
Classification UE (DSD) (obsolète)
|
Très toxique ( T + ) Dangereux pour l'environnement ( N ) |
| Phrases R (obsolètes) | R26 / 28 , R33 , R51 / 53 |
| Phrases S (obsolètes) | (S1 / 2) , S13 , S28 , S45 , S61 |
| point de rupture | Ininflammable |
| Composés apparentés | |
|
Autres anions
|
Fluorure de thallium (I) Chlorure de thallium (I) Bromure de thallium (I) |
|
Autres cations
|
Iodure de gallium (I) Iodure d' indium (I) |
|
Composés apparentés
|
Iodure de mercure (II) Iodure de plomb (II) |
|
Sauf indication contraire, les données sont données pour les matériaux dans leur état standard (à 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Références Infobox | |
L'iodure de thallium (I) est un composé chimique de formule TlI . Il est inhabituel d'être l'un des rares iodures métalliques insolubles dans l'eau , avec AgI , CuI , SnI 2 , SnI 4 , PbI 2 et HgI 2 .
Chimie
TlI peut être formé en solution aqueuse par métathèse de tout sel de thallium soluble avec un ion iodure. Il est également formé comme sous-produit de l'iodation de phénols favorisée par le thallium avec de l'acétate de thallium (I).
Les tentatives faites pour oxyder TlI de thallium (III) iodure sûr, étant donné que l' oxydation produit le thallium (I) triiodure , Tl + I 3 - .
Propriétés physiques
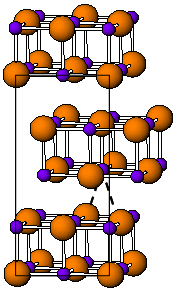
La forme à température ambiante de TlI est jaune et a une structure orthorhombique qui peut être considérée comme une structure NaCl déformée. On pense que la structure déformée est causée par des interactions thallium-thallium favorables, la distance Tl-Tl la plus proche étant de 383 pm. À 175 ° C, la forme jaune se transforme en une forme CsCl rouge . Cette transition de phase s'accompagne d'environ deux ordres de grandeur de saut de conductivité électrique. La structure CsI peut être stabilisée jusqu'à la température ambiante en dopant TlI avec d'autres halogénures tels que RbI, CsI, KI, AgI, TlBr et TlCl. Ainsi, la présence d'impuretés pourrait être responsable de la coexistence des phases cubique et orthorombique TlI aux conditions ambiantes. Sous haute pression, 160 kbar, TlI devient un conducteur métallique. Les films TlI nanométriques minces cultivés sur des substrats LiF, NaCl ou KBr présentent la structure cubique de sel de roche .
Applications
De l'iodure de thallium (I) est ajouté aux lampes à arc au mercure pour améliorer leurs performances. La lumière produite se trouve principalement dans la partie bleu-vert du spectre de la lumière visible la moins absorbée par l'eau, elle a donc été utilisée pour l'éclairage sous-marin. L'iodure de thallium (I) est également utilisé à l'état de traces avec NaI ou CsI pour produire des scintillateurs utilisés dans les détecteurs de rayonnement.
Occurrence naturelle
L'iodure de thallium (I) naturel n'a été trouvé que récemment, sous la forme d'un polymorphe orthorhombique appelé nataliyamalikite. Il est d'origine fumarolique.
Sécurité
Comme tous les composés du thallium, l'iodure de thallium (I) est hautement toxique.
Les références
Sources citées
- Haynes, William M., éd. (2011). CRC Handbook of Chemistry and Physics (92e éd.). Boca Raton, Floride: CRC Press . ISBN 1439855110 .
