Aggrecan - Aggrecan
L'aggrécan (ACAN) , également connu sous le nom de protéine centrale protéoglycane spécifique du cartilage (CSPCP) ou protéoglycane sulfate de chondroïtine 1 , est une protéine codée chez l'homme par le gène ACAN . Ce gène appartient à la famille des lectican ( chondroïtine sulfate protéoglycane ). La protéine codée fait partie intégrante de la matrice extracellulaire dans le tissu cartilagineux et résiste à la compression dans le cartilage .
Aggrecan est un protéoglycane , ou une protéine modifiée avec de gros glucides ; la forme humaine de la protéine a une longueur de 2316 acides aminés et peut être exprimée en plusieurs isoformes en raison d' un épissage alternatif .
Structure
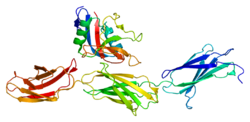
L'aggrécan est un protéoglycane de haut poids moléculaire (1x10 6 <M <3x10 6 ). Il présente une structure de brosse à bouteilles, dans laquelle les chaînes de sulfate de chondroïtine et de sulfate de kératane glycosaminoglycane (GAG) sont attachées à un noyau protéique étendu.
Aggrecan a une masse moléculaire> 2 500 k Da . La protéine de base (~ 300 kDa) a environ 100 chaînes GAG qui lui sont attachées.
Aggrecan se compose de deux domaines structuraux globulaires (G1 et G2) à l' extrémité N-terminale et d'un domaine globulaire (G3) à l' extrémité C-terminale , séparés par un grand domaine étendu (CS) fortement modifié avec des GAG . (N-G1-G2-CS-G3-C) Les deux principaux fragments modificateurs sont eux-mêmes disposés en régions distinctes, une région de sulfate de chondroïtine et une région de sulfate de kératane .
Les trois domaines globulaires, G1, G2 et G3 sont impliqués dans l'agrégation, la liaison de l' hyaluronane , l'adhésion cellulaire et l' apoptose des chondrocytes .
Avec le collagène de type II , l'aggrécan forme un composant structurel majeur du cartilage , en particulier le cartilage articulaire .
La famille des agrécanes comprend d'autres membres importants tels que le versican , également appelé PG-M, le neurocan , le brevican et le récepteur de HA de surface cellulaire CD44 . Ce sont des protéoglycanes modulaires contenant des combinaisons de motifs structurels, tels que des domaines de type EGF , des domaines de reconnaissance des glucides (CRD), des domaines de type protéine de liaison au complément (CBP), des replis d'immunoglobuline et des répétitions en tandem de protéoglycane.
Fonction
Aggrecan est un composant essentiel pour la structure du cartilage et la fonction des articulations.
Fonctionnellement, le domaine G1 interagit avec l'acide hyaluronique et la protéine de liaison, formant des complexes ternaires stables dans la matrice extracellulaire. G2 est homologue aux répétitions en tandem de G1 et de la protéine de liaison et est impliquée dans le traitement du produit. G3 constitue l'extrémité carboxyle de la protéine centrale. Il améliore la modification des glycosaminoglycanes et la sécrétion du produit. Aggrecan joue un rôle important dans la médiation des interactions chondrocytes-chondrocytes et chondrocytes-matrice grâce à sa capacité à se lier à l'hyaluronane.
Aggrecan fournit au disque intervertébral et au cartilage la capacité de résister aux charges de compression. Les concentrations élevées localisées d'aggrécane fournissent les propriétés osmotiques nécessaires à la fonction normale des tissus, les GAG produisant la pression de gonflement qui s'oppose aux charges de compression sur le tissu. Cette capacité fonctionnelle dépend de la présence d'une concentration élevée de GAG / aggrécane dans la matrice extracellulaire tissulaire. Dans le disque, les concentrations d'agrécanes atteignent leur maximum dans la vingtaine et diminuent par la suite, les produits de dégradation des agrécanes s'accumulant lentement au cours des décennies suivantes. Cela rend les disques plus rigides et moins résistants avec l'âge.
Aggrecan joue également un rôle important dans l'organisation des espaces extracellulaires entre les neurones du cerveau . Par des interactions avec la protéine de liaison et les ténascines , l'aggrécan se lie à l' hyaluronane , formant de grands complexes agrégés à la surface cellulaire .
Signification clinique
La synthèse et la dégradation de l'aggrécan sont étudiées pour leurs rôles dans la détérioration du cartilage lors de lésions articulaires, de maladies et de vieillissement.
Le domaine de liaison entre les domaines globulaires N-terminaux, appelé domaine interglobulaire, est très sensible à la protéolyse . Une telle dégradation a été associée au développement de l' arthrite . Les protéases capables de dégrader les aggrécanes sont appelées aggrécanases et font partie de la famille des protéines ADAM (A Disintegrin And Metalloprotease ).
La maladie dégénérative des articulations est une des principales sources de morbidité ayant un impact social et économique significatif. L'arthrose se caractérise par une lente détérioration progressive du cartilage articulaire et une fibrose de la synoviale et de la capsule articulaire . Le cartilage articulaire contient jusqu'à 10% de protéoglycane en poids, dont la majeure partie est de l'aggrécane, et sa perte est un signe précoce de la maladie.
Références
Lectures complémentaires
- Watanabe H, Yamada Y, Kimata K (1998). "Les rôles d'aggrecan, un grand protéoglycane de sulfate de chondroïtine, dans la structure et la fonction de cartilage". J. Biochem . 124 (4): 687–93. doi : 10.1093 / oxfordjournals.jbchem.a022166 . PMID 9756610 .
- Fosang AJ, Neame PJ, Last K, Hardingham TE, Murphy G, Hamilton JA (1992). "Le domaine interglobulaire de l'aggrécan de cartilage est clivé par la POMPE, les gélatinases et la cathepsine B". J. Biol. Chem . 267 (27): 19470–4. PMID 1326552 .
- Sandy JD, Flannery CR, Neame PJ, Lohmander LS (1992). "La structure des fragments d'agrécane dans le liquide synovial humain. Preuve de l'implication dans l'arthrose d'une nouvelle protéinase qui clive la liaison Glu 373-Ala 374 du domaine interglobulaire" . J. Clin. Investissez . 89 (5): 1512–6. doi : 10.1172 / JCI115742 . PMC 443022 . PMID 1569188 .
- Baldwin CT, Reginato AM, Prockop DJ (1989). "Un nouveau domaine de facteur de croissance épidermique semblable dans la protéine de noyau humain pour le grand protéoglycane spécifique de cartilage. Preuve d'épissage alternatif du domaine". J. Biol. Chem . 264 (27): 15747–50. PMID 2789216 .
- Kimata K, Barrach HJ, Brown KS, Pennypacker JP (1981). "Absence de protéine de noyau de protéoglycane dans le cartilage de la souris cmd / cmd (déficit de matrice de cartilage)". J. Biol. Chem . 256 (13): 6961–8. PMID 7240256 .
- Glumoff V, Savontaus M, Vehanen J, Vuorio E (1994). "Analyse de l'expression des gènes d'aggrécan et de ténascine dans les tissus squelettiques de souris par hybridation nordique et in situ en utilisant des sondes d'ADNc spécifiques d'espèces". Biochim. Biophys. Acta . 1219 (3): 613–22. doi : 10.1016 / 0167-4781 (94) 90220-8 . PMID 7524681 .
- Ilic MZ, Mok MT, Williamson OD, Campbell MA, Hughes CE, Handley CJ (1995). "Catabolisme d'aggrecan par des cultures d'explants de cartilage articulaire humain en présence d'acide rétinoïque". Cambre. Biochem. Biophys . 322 (1): 22–30. doi : 10.1006 / abbi.1995.1431 . PMID 7574678 .
- Valhmu WB, Palmer GD, Rivers PA, Ebara S, Cheng JF, Fischer S, Ratcliffe A (1995). "Structure du gène d'aggrécan humain: organisation d'exon-intron et association avec les domaines protéiques" . Biochem. J . 309. 309 (2): 535–42. doi : 10.1042 / bj3090535 . PMC 1135764 . PMID 7626017 .
- Barry FP, Neame PJ, Sasse J, Pearson D (1994). "Variation de longueur dans le domaine de sulfate de kératane d'aggrécan mammifère". Matrix Biol . 14 (4): 323–8. doi : 10.1016 / 0945-053X (94) 90198-8 . PMID 7827755 .
- Fosang AJ, Last K, Neame PJ, Murphy G, Knäuper V, Tschesche H, Hughes CE, Caterson B, Hardingham TE (1994). "La collagénase neutrophile (MMP-8) clive au site d'aggrécanase E373-A374 dans le domaine interglobulaire de l'aggrécan de cartilage" . Biochem. J . 304. 304 (2): 347–51. doi : 10.1042 / bj3040347 . PMC 1137499 . PMID 7998967 .
- Fosang AJ, Last K, Knäuper V, Neame PJ, Murphy G, Hardingham TE, Tschesche H, Hamilton JA (1993). "Les collagénases fibroblastes et neutrophiles clivent en deux sites dans le domaine interglobulaire de l'aggrécane du cartilage" . Biochem. J . 295. 295 (1): 273–6. doi : 10.1042 / bj2950273 . PMC 1134849 . PMID 8216228 .
- Korenberg JR, Chen XN, Doege K, Grover J, Roughley PJ (1993). "Attribution du gène humain d'aggrécan (AGC1) à 15q26 en utilisant l'analyse d'hybridation in situ par fluorescence". Génomique . 16 (2): 546–8. doi : 10.1006 / geno.1993.1228 . PMID 8314595 .
- Dudhia J, Davidson CM, Wells TM, Vynios DH, Hardingham TE, Bayliss MT (1996). "Changements liés à l'âge dans le contenu de la région C-terminale d'aggrécan dans le cartilage articulaire humain" . Biochem. J . 313. 313 (3): 933–40. doi : 10.1042 / bj3130933 . PMC 1217001 . PMID 8611178 .
- Fülöp C, Cs-Szabó G, Glant TT (1996). "Épissage alternatif spécifique d'espèce du domaine 1 de facteur de croissance épidermique semblable d'aggrecan de cartilage" . Biochem. J . 319. 319 (3): 935–40. doi : 10.1042 / bj3190935 . PMC 1217878 . PMID 8921002 .
- Kirschfink M, Blase L, Engelmann S, Schwartz-Albiez R (1997). "Le protéoglycane de sulfate de chondroïtine sécrété des lignées de cellules B humaines se lie à la protéine de complément C1q et inhibe la formation complexe de C1". J. Immunol . 158 (3): 1324–31. PMID 9013976 .
- Parkar AA, Kahmann JD, Howat SL, Bayliss MT, Day AJ (1998). "TSG-6 interagit avec l'hyaluronane et l'aggrécane d'une manière dépendant du pH via un élément fonctionnel commun: implications pour sa régulation dans le cartilage enflammé" . FEBS Lett . 428 (3): 171–6. doi : 10.1016 / S0014-5793 (98) 00523-7 . PMID 9654129 .
- Fosang AJ, Last K, Fujii Y, Seiki M, Okada Y (1998). "Le type de membrane 1 MMP (MMP-14) clive à trois sites dans le domaine interglobulaire d'agrécane" . FEBS Lett . 430 (3): 186–90. doi : 10.1016 / S0014-5793 (98) 00667-X . PMID 9688535 .
- "Aggrecan" . Centre d'apprentissage . Société Sigma-Aldrich . Récupéré le 24/10/2011 .
Liens externes
- Aggrecan à la US National Library of Medicine Medical Subject Headings (MeSH)
- Emplacement du génome humain ACAN et page de détails du gène ACAN dans le navigateur de génomes UCSC .
- Vue d'ensemble de toutes les informations structurelles disponibles dans le PDB pour UniProt : P16112 (Human Aggrecan core protein) au PDBe-KB .
- Vue d'ensemble de toutes les informations structurelles disponibles dans le PDB pour UniProt : P07897 (Rat Aggrecan core protein) au PDBe-KB .