Acétate de béryllium basique - Basic beryllium acetate

|
|
| Noms | |
|---|---|
|
Nom IUPAC systématique
Hexa-μ-acétato(O,O')-μ4-oxo-tétrabéryllium(II) |
|
| Autres noms
Oxyacétate de
béryllium Acétate d'oxyde de béryllium Acétate de béryllium basique |
|
| Identifiants | |
|
Modèle 3D ( JSmol )
|
|
| ChemSpider | |
| Carte d'information de l'ECHA |
100.038.881 |
| Numéro CE | |
|
CID PubChem
|
|
| UNII | |
|
Tableau de bord CompTox ( EPA )
|
|
|
|
| Propriétés | |
|
C 12H 18Être 4O 13 |
|
| Masse molaire | 406,3122 g/mol |
| Apparence | incolore |
| Point de fusion | 285 °C (545 °F; 558 K) |
| Point d'ébullition | 330 °C (626 °F; 603 K) |
| Solubilité dans le chloroforme | soluble |
| Dangers | |
| Principaux dangers | très toxique |
| NIOSH (limites d'exposition pour la santé aux États-Unis) : | |
|
PEL (Autorisé)
|
TWA 0,002 mg/m 3 C 0,005 mg/m 3 (30 minutes), avec un pic maximum de 0,025 mg/m 3 (en Be) |
|
REL (recommandé)
|
Ca C 0,0005 mg/m 3 (en Be) |
|
IDLH (Danger immédiat)
|
Ca [4 mg/m 3 (en Be)] |
|
Sauf indication contraire, les données sont données pour les matériaux dans leur état standard (à 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Références de l'infobox | |
L'acétate de béryllium basique est le composé chimique de formule Be 4 O(O 2 CCH 3 ) 6 . Ce composé adopte une structure distinctive, mais il n'a pas d'applications et n'a été que peu étudié. C'est un solide incolore soluble dans les solvants organiques.
Préparation
Il peut être préparé en traitant du carbonate de béryllium basique avec de l'acide acétique chaud .
- 2 être
2CO
3(OH)
2+ 6 AcOH → être
4O(AcO)
6+ 5H
2O + 2 CO
2
L'acétate de béryllium basique est insoluble dans l'eau mais soluble dans le chloroforme , ce qui est cohérent avec son caractère non polaire. Il fond et se sublime sous vide sans se décomposer.
Structure
Les « acétates basiques » se composent d'un ensemble de centres métalliques liés à un ion oxyde central et d'une collection de ligands acétate . L'acétate de béryllium basique a un noyau tétraédrique Be 4 O 6+ avec des acétates (CH 3 CO 2 − ) couvrant chacune des paires de centres Be 2+ . Il se compose d' anneaux de Be 2 O 3 C à six chaînons imbriqués . La structure est importante pour sa stabilité considérable (le composé est distillable à 330 °C).
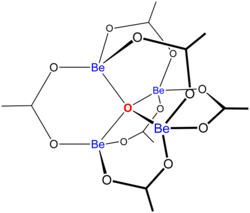
Les usages
La solubilité du sel dans les solvants organiques (chloroforme) est utile pour extraire et purifier les fractions riches en béryllium à de nombreuses fins. Les monocristaux basiques d'acétate de béryllium peuvent facilement être cultivés et sont utiles pour aligner les diffractomètres à rayons X et également comme référence en cristallographie des protéines.
Voir également
Les références
- ^ A b c NIOSH Pocket Guide de dangers des produits chimiques. "#0054" . Institut national pour la sécurité et la santé au travail (NIOSH).
- ^ Moeller, T. (1950). "Dérivés de base de béryllium d'acides organiques". Dans Audrieth, LF (éd.). Synthèses inorganiques, tome 3 . Synthèses inorganiques. John Wiley & Fils . p. 4-9. doi : 10.1002/9780470132340.ch2 . ISBN 978-0-470-13234-0.
- ^ Bragg, WH (1923). "Structure cristalline de l'acétate de béryllium basique" . Nature . 111 (2 790): 532. bibcode : 1923Natur.111..532B . doi : 10.1038/111532a0 .
- ^ Pauling, L. ; Sherman, J. (1934). "La structure du groupe carboxyle. II. La structure cristalline de l'acétate de béryllium basique" (PDF) . Actes de l'Académie nationale des sciences . 20 (6) : 340-5. Bibcode : 1934PNAS ... 20..340P . doi : 10.1073/pnas.20.6.340 . PMC 1076415 . PMID 16587899 .
