Téréphtalate de diméthyle - Dimethyl terephthalate

|
|
| Noms | |
|---|---|
|
Nom IUPAC préféré
Diméthylbenzène-1,4-dicarboxylate |
|
| Autres noms
Téréphtalate de diméthyle
1,4-benzènedicarboxylique acide diméthyl ester diméthylique 4-phtalate de diméthyle p phtalate de di-Me téréphtalate de méthyle 4-carbomethoxybenzoate méthyl-p- (méthoxycarbonyl) benzoate de méthyle téréphtalate, di- ester de l' acide téréphtalique de diméthyle |
|
| Identifiants | |
|
Modèle 3D ( JSmol )
|
|
| Abréviations | DMT |
| 1107185 | |
| ChEBI | |
| ChemSpider | |
| Carte d'information de l'ECHA |
100.004.011 |
| Numéro CE | |
| Engrener | Diméthyl+4-phtalate |
|
CID PubChem
|
|
| Numéro RTECS | |
| UNII | |
|
Tableau de bord CompTox ( EPA )
|
|
|
|
|
|
| Propriétés | |
| C 10 H 10 O 4 | |
| Masse molaire | 194,186 g·mol -1 |
| Apparence | solide blanc |
| Densité | 1,2 g/cm 3 , ? |
| Point de fusion | 142 °C (288 °F; 415 K) |
| Point d'ébullition | 288 °C (550 °F; 561 K) |
| Acidité (p K a ) | -7,21 |
| Basicité (p K b ) | -6,60 |
|
Sauf indication contraire, les données sont données pour les matériaux dans leur état standard (à 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Références de l'infobox | |
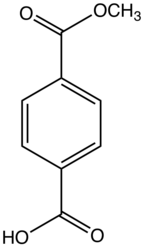
Le téréphtalate de diméthyle (DMT) est un composé organique de formule C 6 H 4 (COOCH 3 ) 2 . C'est le diester formé d' acide téréphtalique et de méthanol . C'est un solide blanc qui fond pour donner un liquide incolore distillable.
Production
Le téréphtalate de diméthyle (DMT) a été produit de plusieurs manières. Classiquement, et toujours d'intérêt commercial, est l'estérification directe de l'acide téréphtalique. En variante, il peut être préparé par oxydation alternée et méthyl- estérification étapes à partir de p-xylène par l' intermédiaire d'un groupe méthyle p -toluate (PT).
Téréphtalate de diméthyle (DMT) (procédé Witten)
Le procédé de production de DMT à partir de p- xylène (PX) et de méthanol consiste en un processus en plusieurs étapes impliquant à la fois l'oxydation et l'estérification. Un mélange de p-xylène (PX) et de p- toluate de méthyle est oxydé à l'air en présence d'un catalyseur au cobalt et au manganèse. Le mélange acide résultant de l'oxydation est estérifié avec du méthanol pour donner un mélange d'esters. Le mélange d'esters bruts est distillé pour éliminer tous les chaudières lourdes et les résidus produits ; les esters plus légers sont recyclés vers la section d'oxydation. Le DMT brut est ensuite envoyé à la section de cristallisation pour éliminer les isomères du DMT, les acides résiduels et les aldéhydes aromatiques.
L'oxydation du p-toluate de méthyle suivie d'une estérification donne également du téréphtalate de diméthyle (DMT) comme le montre la réaction ci-dessous :
Production de téréphtalate de diméthyle (DMT) par estérification directe
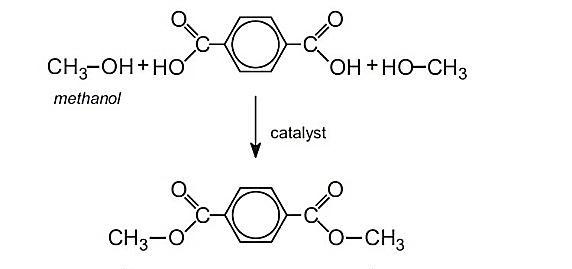
Si de l'acide téréphtalique hautement impur est disponible, le DMT peut être fabriqué dans un processus séparé par estérification avec du méthanol en téréphtalate de diméthyle, qui est ensuite purifié par distillation :
- C 8 H 6 O 4 + 2CH 3 OH → C 10 H 10 O 4 + 2 H 2 O
en présence d'o-xylène à 250–300 °C.
Utilisation
Le DMT est utilisé dans la production de polyesters , dont le polyéthylène téréphtalate (PET), le polytriméthylène téréphtalate (PTT) et le polybutylène téréphtalate (PBT). Il se compose de benzène substitué par des groupes carboxyméthyle (CO 2 CH 3 ) aux positions 1 et 4. Le DMT étant volatil, il constitue un intermédiaire dans certains schémas de recyclage du PET, par exemple à partir de bouteilles en plastique .
L'hydrogénation du DMT donne le diol cyclohexanediméthanol , qui est un monomère utile.
Les références
- ^ A b c Richard J. Sheehan "acide téréphtalique, téréphtalate de diméthyle et l' acide isophthalique" dans l' Encyclopédie Ullmann de chimie industrielle, Wiley-VCH, Weinheim, 2005. doi : 10.1002 / 14356007.a26_193
- ^ "Téréphtalate de diméthyle (DMT)" . 2013-05-02.
Liens externes
- Fournisseur : Teijin Limited https://web.archive.org/web/20150503041344/http://www.teijin.com/products/chemicals/dmt/
- http://www.inchem.org/documents/icsc/icsc/eics0262.htm
- Carte internationale de sécurité chimique 0262
- Bibliothèque nationale de médecine des États-Unis : Banque de données sur les substances dangereuses – Diméthyl+téréphtalate