ELMO1 - ELMO1
Engloutissement et motilité cellulaire La protéine 1 est une protéine qui, chez l'homme, est codée par le gène ELMO1 . ELMO1 est situé sur le chromosome numéro sept chez l'homme et sur le chromosome numéro treize chez la souris.
Structure
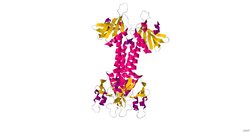
La protéine d'engloutissement humain et de motilité cellulaire 1, ELMO1, a une longueur de 720 résidus. La protéine contient les trois domaines suivants :
- Domaine Armadillo N-terminal (résidus 82-262)
- central ELMO ( E ngulfment et Cel l Mo tilité) domaine (301-492)
- Domaine d'homologie pleckstrine C-terminal (résidus 527-674)
ELMO1 a également un motif pro-riche à l'extrémité C-terminale. L'analyse de structure secondaire a prédit qu'il existe des régions alpha-hélicoïdales à la fois aux extrémités N et C.
La structure du domaine d'homologie de la pleckstrine d'ELMO1 a été déterminée par cristallographie aux rayons X.
Fonction
La protéine codée par ce gène interagit avec le dédicateur de la protéine cyto-kinésie 1 pour favoriser la phagocytose et effectuer des changements de forme cellulaire. La similitude avec une protéine de C. elegans suggère que cette protéine peut fonctionner dans l'apoptose et dans la migration cellulaire. L'épissage alternatif de ce gène résulte en de multiples variantes de transcrits codant pour différentes isoformes.
Interactions
Il a été démontré que ELMO1 interagit avec Dock180 et HCK . ELMO1 interagit directement avec le domaine SH3 de HCK. L'association entre ELMO1 et HCK dépend des interactions de la polyproline.
Lorsque ELMO1 est complexé avec DOCK180, les processus biologiques dépendants de Rac GTPase sont activés. Le domaine pH d'ELMO1 fonctionne en trans pour stabiliser DOCK180 et le rendre résistant à la dégradation. Lorsque ELMO1 se lie à DOCK180, il soulage l'inhibition stérique de DOCK180 qui active alors la Rac GTPase. Le motif pro-riche de l'extrémité C sur ELMO1 est essentiel pour la liaison d'ELMO1 au domaine SH3 à l'extrémité N de DOCK180. Le complexe ELMO1 et DOCK180 agit comme un régulateur de Rac lors du développement d'une cellule et de la migration cellulaire. La mutation des deux sites d'interaction pour DOCK180 sur ELMO1 entraînera la perturbation du complexe ELMO1-DOCK180. ELMO1 complexé avec DOCK180 et CrkII conduit à une efficacité maximale de la phagocytose dans la cellule. Ce complexe de molécules se produit en amont de Rac lors de la phagocytose.
Les références
Lectures complémentaires
- Ohara O, Nagase T, Ishikawa K, et al. (1997). "Construction et caractérisation de bibliothèques d'ADNc de cerveau humain adaptées à l'analyse de clones d'ADNc codant pour des protéines relativement grandes" . ADN Res . 4 (1) : 53-9. doi : 10.1093/dnares/4.1.53 . PMID 9179496 .
- Wiemann S, Weil B, Wellenreuther R, et al. (2001). « Vers un catalogue de gènes et de protéines humains : séquençage et analyse de 500 nouveaux ADNc humains complets codant des protéines » . Génome Res . 11 (3) : 422–35. doi : 10.1101/gr.GR1547R . PMC 311072 . PMID 11230166 .
- Scott MP, Zappacosta F, Kim EY, et al. (2002). "Identification de nouveaux ligands du domaine SH3 pour la kinase de la famille Src Hck. Protéine du syndrome de Wiskott-Aldrich (WASP), protéine d'interaction WASP (WIP) et ELMO1" . J. Biol. Chem . 277 (31) : 28238-46. doi : 10.1074/jbc.M202783200 . PMID 12029088 .
- Brugnera E, Haney L, Grimsley C, et al. (2002). "L'activité Rac-GEF non conventionnelle est médiée par le complexe Dock180-ELMO". Nat. Cell Biol . 4 (8) : 574–82. doi : 10.1038/ncb824 . PMID 12134158 . S2CID 36363774 .
- Strausberg RL, Feingold EA, Grouse LH, et al. (2003). "Génération et analyse initiale de plus de 15 000 séquences d'ADNc humaines et de souris complètes" . Proc. Natl. Acad. Sci. États-Unis . 99 (26) : 16899–903. doi : 10.1073/pnas.242603899 . PMC 139241 . PMID 12477932 .
- Scherer SW, Cheung J, MacDonald JR, et al. (2003). « Chromosome humain 7 : séquence d'ADN et biologie » . Sciences . 300 (5620) : 767-72. Bibcode : 2003Sci ... 300..767S . doi : 10.1126/science.1083423 . PMC 2882961 . PMID 12690205 .
- Sanui T, Inayoshi A, Noda M, et al. (2003). « DOCK2 régule l'activation de Rac et la réorganisation du cytosquelette par interaction avec ELMO1 ». Du sang . 102 (8) : 2948-50. doi : 10.1182/sang-2003-01-0173 . PMID 12829596 .
- Katoh H, Negishi M (2003). "RhoG active Rac1 par interaction directe avec la protéine de liaison Dock180 Elmo". Nature . 424 (6947) : 461-4. Bibcode : 2003Natur.424..461K . doi : 10.1038/nature01817 . PMID 12879077 . S2CID 4411133 .
- Grimsley CM, Kinchen JM, Tosello-Trampont AC, et al. (2004). "Les protéines Dock180 et ELMO1 coopèrent pour promouvoir la migration cellulaire dépendante de Rac conservée au cours de l'évolution" . J. Biol. Chem . 279 (7) : 6087–97. doi : 10.1074/jbc.M307087200 . PMID 14638695 .
- Wang X, Wu YC, Fadok VA, et al. (2003). « Engloutissement des cadavres cellulaires médié par le récepteur de la phosphatidylsérine de C. elegans via CED-5 et CED-12 ». Sciences . 302 (5650) : 1563–6. Bibcode : 2003Sci ... 302.1563W . doi : 10.1126/science.1087641 . PMID 14645848 . S2CID 25672278 .
- Ota T, Suzuki Y, Nishikawa T, et al. (2004). "Séquençage complet et caractérisation de 21 243 ADNc humains de pleine longueur" . Nat. Genet . 36 (1) : 40-5. doi : 10.1038/ng1285 . PMID 14702039 .
- Janardhan A, Swigut T, Hill B et al. (2006). "HIV-1 Nef lie le complexe DOCK2-ELMO1 pour activer rac et inhiber la chimiotaxie des lymphocytes" . PLOS Biol . 2 (1) : E6. doi : 10.1371/journal.pbio.0020006 . PMC 314466 . PMID 14737186 .
- Lu M, Kinchen JM, Rossman KL, et al. (2004). "Le domaine PH des fonctions ELMO en trans pour réguler l'activation de Rac via Dock180". Nat. Structurer. Mol. Biol . 11 (8) : 756-762. doi : 10.1038/nsmb800 . PMID 15247908 . S2CID 125990 .
- Gerhard DS, Wagner L, Feingold EA, et al. (2004). « Le statut, la qualité et l'expansion du projet d'ADNc complet du NIH : la collection de gènes de mammifères (MGC) » . Génome Res . 14 (10B) : 2121–7. doi : 10.1101/gr.2596504 . PMC 528928 . PMID 15489334 .
- deBakker CD, Haney LB, Kinchen JM, et al. (2005). "La phagocytose des cellules apoptotiques est régulée par un module de signalisation UNC-73/TRIO-MIG-2/RhoG et des répétitions tatou de CED-12/ELMO" . Cour. Biol . 14 (24) : 2208–16. doi : 10.1016/j.cub.2004.12.029 . PMID 15620647 . S2CID 1269946 .
- Akakura S, Kar B, Singh S, et al. (2005). « Le domaine SH3 C-terminal de CrkII régule l'assemblage et la fonction du DOCK180/ELMO Rac-GEF ». J. Cell. Physiol . 204 (1) : 344-51. doi : 10.1002/jcp.20288 . PMID 15700267 . S2CID 29767556 .
- Lu M, Kinchen JM, Rossman KL, et al. (2005). "Un modèle d'inhibition stérique pour la régulation de l'échange de nucléotides via la famille Dock180 de GEF" . Cour. Biol . 15 (4) : 371-7. doi : 10.1016/j.cub.2005.01.050 . PMID 15723800 . S2CID 14267018 .
- Shimazaki A, Kawamura Y, Kanazawa A, et al. (2005). "Les variations génétiques du gène codant pour ELMO1 sont associées à une susceptibilité à la néphropathie diabétique" . Diabète . 54 (4) : 1171–8. doi : 10.2337/diabetes.54.4.1171 . PMID 15793258 .
- Yokoyama N, deBakker CD, Zappacosta F, et al. (2005). "Identification des résidus de tyrosine sur ELMO1 qui sont phosphorylés par la kinase Hck de la famille Src" . Biochimie . 44 (24) : 8841-9. doi : 10.1021/bi0500832 . PMC 2441568 . PMID 15952790 .