Disulfite - Disulfite

|
|
| Des noms | |
|---|---|
|
Nom IUPAC
disulfite
|
|
|
Nom IUPAC systématique
pentaoxido-1 κ 3 O ,2 κ 2 O -disulfate(S—S)(2−) |
|
| Autres noms
pyrosulfite d' ions métabisulfite |
|
| Identifiants | |
|
Modèle 3D ( JSmol )
|
|
| ChemSpider | |
|
CID PubChem
|
|
| UNII | |
|
Tableau de bord CompTox ( EPA )
|
|
|
|
|
|
| Propriétés | |
|
S 2O2− 5 |
|
| Acide conjugué | Acide disulfureux |
|
Sauf indication contraire, les données sont données pour les matériaux dans leur état standard (à 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Références de l'infobox | |
Un disulfite , communément appelé métabisulfite ou pyrosulfite , est un composé chimique contenant l' ion S
2O2−
5. C'est un dianion incolore qui est principalement commercialisé sous forme de métabisulfite de sodium ou de métabisulfite de potassium . Lorsqu'ils sont dissous dans l'eau, ces sels libèrent le bisulfite HSO−
3ion. Ces sels agissent de manière équivalente au bisulfite de sodium ou au bisulfite de potassium .
Structure
Contrairement au disulfate ( S
2O2−
7), ion disulfite ( S
2O2−
5) a une structure asymétrique avec une liaison SS. L'état d'oxydation de l'atome de soufre lié à 3 atomes d'oxygène est de +5 tandis que le nombre d'oxydation des autres atomes de soufre est de +3.
L'anion est constitué d'un groupe SO 2 lié à un groupe SO 3 , la charge négative étant plus localisée à l' extrémité SO 3 . La longueur de la liaison S–S est de 2,22 et les distances S–O « thionate » et « thionite » sont respectivement de 1,46 et 1,50 .
Production
Les sels d'ion disulfite sont produits par déshydratation de sels d' ion bisulfite ( HSO−
3). Lorsque les solutions de bisulfite de sodium ou de bisulfite de potassium sont évaporées, il en résulte du métabisulfite de sodium et du métabisulfite de potassium .
Bien que l'équilibre se situe loin à gauche, l'évaporation d'un sel bisulfite produira une quantité substantielle de disulfite.
Le disulfite est la base conjuguée de l'acide disulfureux ( acide pyrosulfureux), qui provient de l'acide sulfureux conformément à la réaction de déshydratation ci-dessus :
- 2 H 2 SO 3 → 2 HSO−
3+ 2 H + → H 2 S 2 O 5 + H 2 O
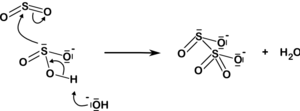
L'ion disulfite résulte également de l'ajout de dioxyde de soufre à l' ion sulfite :
|
ASS− 3 3+ H + SO 3 2− + SO 2 S 2O2− 5 |
Utiliser
Les sels disulfites sont utilisés pour la conservation des aliments et des boissons .
Exemples de disulfites
- Le métabisulfite de sodium ( E223 ) et le métabisulfite de potassium (E224) sont utilisés comme conservateur et antioxydant dans les aliments. Les sulfites sont impliqués dans les réactions asthmatiques et peuvent également provoquer des symptômes chez les personnes non asthmatiques, à savoir dermatite , urticaire , bouffées vasomotrices , hypotension , douleurs abdominales et diarrhée , et même anaphylaxie potentiellement mortelle .