Hérédité non mendélienne - Non-Mendelian inheritance
L'hérédité non mendélienne est tout modèle d'hérédité dans lequel les traits ne se séparent pas conformément aux lois de Mendel . Ces lois décrivent l'hérédité de traits liés à des gènes uniques sur les chromosomes du noyau. Dans l'hérédité mendélienne , chaque parent contribue à l'un des deux allèles possibles pour un trait. Si les génotypes des deux parents d'un croisement génétique sont connus, les lois de Mendel peuvent être utilisées pour déterminer la distribution des phénotypes attendue pour la population de la progéniture. Il existe plusieurs situations dans lesquelles les proportions de phénotypes observés dans la descendance ne correspondent pas aux valeurs prédites.
L'hérédité non mendélienne joue un rôle dans plusieurs processus pathologiques.
Les types
Dominance incomplète
En cas d'hérédité intermédiaire due à une dominance incomplète , le principe de dominance découvert par Mendel ne s'applique pas. Néanmoins, le principe d'uniformité fonctionne, car tous les descendants de la génération F 1 ont le même génotype et le même phénotype. Le principe de ségrégation des gènes de Mendel s'applique également, car dans la génération F 2 apparaissent des individus homozygotes avec les phénotypes de la génération P. L'hérédité intermédiaire a été examinée pour la première fois par Carl Correns dans Mirabilis jalapa qu'il a utilisé pour d'autres expériences génétiques. Antirrhinum majus présente également une transmission intermédiaire de la pigmentation des fleurs.
Co-dominance
En cas de co-dominance , les traits génétiques des deux allèles différents du même gène-locus sont clairement exprimés dans le phénotype. Par exemple, chez certaines variétés de poulet, l'allèle des plumes noires est co-dominant avec l'allèle des plumes blanches. Les poulets hétérozygotes ont une couleur décrite comme « erminette », tachetée de plumes noires et blanches apparaissant séparément. De nombreux gènes humains, dont un pour une protéine qui contrôle le taux de cholestérol dans le sang, présentent également une co-dominance. Les personnes atteintes de la forme hétérozygote de ce gène produisent deux formes différentes de la protéine, chacune ayant un effet différent sur le taux de cholestérol.
Lien génétique
Lorsque les gènes sont situés sur le même chromosome et qu'aucun croisement n'a eu lieu avant la ségrégation des chromosomes dans les gamètes , les traits génétiques seront hérités en lien, en raison de la liaison génétique . Ces cas constituent une exception à la règle mendélienne de l'assortiment indépendant.
Allèles multiples
Dans l'hérédité mendélienne, les gènes n'ont que deux allèles, tels que a et A . Mendel a consciemment choisi des paires de traits génétiques, représentés par deux allèles pour ses expériences d'héritage. Dans la nature, de tels gènes existent souvent sous plusieurs formes différentes et on dit donc qu'ils ont de multiples allèles . Un individu, bien sûr, ne possède généralement que deux copies de chaque gène, mais de nombreux allèles différents sont souvent trouvés au sein d'une population. La couleur du pelage d'un lapin est déterminée par un seul gène qui possède au moins quatre allèles différents. Ils affichent un modèle de hiérarchie de dominance qui peut produire quatre couleurs de pelage. Dans les gènes des couleurs du pelage du chien, il y a quatre allèles sur le locus Agouti. L'allèle "aw" est dominant sur les allèles "at" et "a" mais récessif sous "Ay".
De nombreux autres gènes ont plusieurs allèles, y compris les gènes humains du groupe sanguin ABO .
Épistase


Si un ou plusieurs gènes ne peuvent pas être exprimés à cause d'un autre facteur génétique entravant leur expression, cette épistasie peut rendre impossible même pour des allèles dominants sur certains autres gènes-loci d'avoir un effet sur le phénotype. Un exemple dans la génétique du pelage du chien est l'homozygotie avec l'allèle "e e" sur le locus d'extension, ce qui rend impossible la production d'un autre pigment que la phéomélanine. Bien que l'allèle "e" soit un allèle récessif sur le locus d'extension lui-même, la présence de deux copies tire parti de la dominance d'autres gènes de couleur de robe. Les chats domestiques ont un gène ayant un effet similaire sur le chromosome X.
Hérédité liée au sexe
Les traits génétiques localisés sur les gonosomes présentent parfois des modèles d'hérédité non mendéliens spécifiques. Les individus peuvent développer un trait récessif dans le phénotype dépendant de leur sexe, par exemple, le daltonisme et l' hémophilie (voir Hérédités gonosomiques ). Comme de nombreux allèles sont dominants ou récessifs, une véritable compréhension des principes de l'hérédité mendélienne est une exigence importante pour également comprendre les modèles d'hérédité plus compliqués des héritages liés au sexe.
Héritage extranucléaire
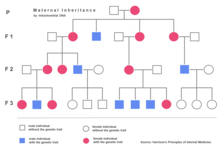
L'hérédité extranucléaire (également connue sous le nom d'hérédité cytoplasmique) est une forme d'hérédité non mendélienne également découverte pour la première fois par Carl Correns en 1908. En travaillant avec Mirabilis jalapa , Correns a observé que la couleur des feuilles ne dépendait que du génotype du parent maternel. Sur la base de ces données, il a déterminé que le trait était transmis par un caractère présent dans le cytoplasme de l' ovule . Des recherches ultérieures menées par Ruth Sager et d'autres ont identifié l'ADN présent dans les chloroplastes comme étant responsable du modèle d'hérédité inhabituel observé. Les travaux sur la souche poky de la moisissure Neurospora crassa commencés par Mary et Hershel Mitchell ont finalement conduit à la découverte de matériel génétique dans les mitochondries, l' ADN mitochondrial .
Selon la théorie des endosymbiotes , les mitochondries et les chloroplastes étaient autrefois des organismes libres qui étaient chacun absorbés par une cellule eucaryote. Au fil du temps, les mitochondries et les chloroplastes ont formé une relation symbiotique avec leurs hôtes eucaryotes. Bien que le transfert d'un certain nombre de gènes de ces organites vers le noyau les empêche de vivre de manière indépendante, chacun possède toujours du matériel génétique sous forme d'ADN double brin.
C'est la transmission de cet ADN organellaire qui est responsable du phénomène d'hérédité extranucléaire. Les chloroplastes et les mitochondries ne sont présents que dans le cytoplasme des gamètes maternels. Les gamètes paternels (les spermatozoïdes par exemple) n'ont pas de mitochondries cytoplasmiques. Ainsi, le phénotype des traits liés aux gènes trouvés dans les chloroplastes ou les mitochondries est déterminé exclusivement par le parent maternel.
Chez l'homme, les maladies mitochondriales sont une classe de maladies, dont beaucoup affectent les muscles et les yeux.
Caractères polygéniques
De nombreux traits sont produits par l'interaction de plusieurs gènes. Les traits contrôlés par deux ou plusieurs gènes sont dits des traits polygéniques . Polygénique signifie que "de nombreux gènes" sont nécessaires pour que l'organisme développe le trait. Par exemple, au moins trois gènes sont impliqués dans la fabrication du pigment brun rougeâtre dans les yeux des mouches des fruits . Les traits polygéniques présentent souvent un large éventail de phénotypes. La grande variété de couleurs de peau chez l'homme est due en partie au fait qu'au moins quatre gènes différents contrôlent probablement ce trait.
Ségrégation non aléatoire
La ségrégation non aléatoire des chromosomes est une déviation de la distribution habituelle des chromosomes pendant la méiose et dans certains cas de mitose.
Conversion de gènes
La conversion génique peut être l'une des principales formes d'hérédité non mendélienne. La conversion génique se produit lors de la réparation de l'ADN via la recombinaison de l' ADN , par laquelle une information de séquence d'ADN est transférée d'une hélice d'ADN (qui reste inchangée) à une autre hélice d'ADN, dont la séquence est altérée. Cela peut se produire comme une réparation de mésappariement entre les brins d'ADN qui sont dérivés de différents parents. Ainsi, la réparation des mésappariements peut convertir un allèle en un autre. Ce phénomène peut être détecté à travers les rapports de descendance non mendéliens, et est fréquemment observé, par exemple, dans les croisements fongiques.
Hérédité infectieuse
Une autre forme d'hérédité non mendélienne est connue sous le nom d'hérédité infectieuse. Les particules infectieuses telles que les virus peuvent infecter les cellules hôtes et continuer à résider dans le cytoplasme de ces cellules. Si la présence de ces particules entraîne un phénotype altéré, alors ce phénotype peut être ultérieurement transmis à la descendance. Étant donné que ce phénotype ne dépend que de la présence de l'envahisseur dans le cytoplasme de la cellule hôte, l'hérédité ne sera déterminée que par le statut infecté du parent maternel. Cela se traduira par une transmission uniparentale du trait, tout comme dans l'hérédité extranucléaire.
L'un des exemples d'hérédité infectieuse les mieux étudiés est le phénomène tueur présenté dans la levure . Deux virus à ARN double brin , désignés L et M, sont responsables de ce phénotype. Le virus L code pour les protéines de capside des deux virus, ainsi qu'une ARN polymérase . Ainsi, le virus M ne peut infecter que les cellules abritant déjà des particules de virus L. L'ARN viral M code pour une toxine qui est sécrétée par la cellule hôte. Il tue les cellules sensibles qui se développent à proximité immédiate de l'hôte. L'ARN viral M rend également la cellule hôte immunisée contre les effets mortels de la toxine. Pour qu'une cellule soit sensible, elle doit donc être soit non infectée, soit héberger uniquement le virus L.
Les virus L et M ne sont pas capables de sortir de leur cellule hôte par des moyens conventionnels. Ils ne peuvent passer d'une cellule à l'autre que lorsque leur hôte s'accouple. Toute la descendance d'un accouplement impliquant une cellule de levure doublement infectée sera également infectée par les virus L et M. Par conséquent, le phénotype tueur sera transmis à toute la descendance.
Des traits héréditaires résultant d'une infection par des particules étrangères ont également été identifiés chez la drosophile . Les mouches de type sauvage récupèrent normalement complètement après avoir été anesthésiées avec du dioxyde de carbone. Certaines lignées de mouches ont été identifiées qui meurent après exposition au composé. Cette sensibilité au dioxyde de carbone est transmise de la mère à sa progéniture. Cette sensibilité est due à une infection par le virus σ (Sigma), un rhabdovirus capable uniquement d'infecter la drosophile .
Bien que ce processus soit généralement associé à des virus, des recherches récentes ont montré que la bactérie Wolbachia est également capable d'insérer son génome dans celui de son hôte.
Empreinte génomique
L'empreinte génomique représente encore un autre exemple d'hérédité non mendélienne. Tout comme dans l'hérédité conventionnelle, les gènes d'un trait donné sont transmis à la descendance des deux parents. Cependant, ces gènes sont marqués épigénétiquement avant la transmission, modifiant leurs niveaux d'expression. Ces empreintes sont créées avant la formation des gamètes et sont effacées lors de la création des cellules de la lignée germinale. Par conséquent, un nouveau modèle d'impression peut être fait à chaque génération.
Les gènes sont imprimés différemment selon l'origine parentale du chromosome qui les contient. Chez la souris, le gène du facteur de croissance analogue à l' insuline 2 subit une empreinte. La protéine codée par ce gène aide à réguler la taille du corps. Les souris possédant deux copies fonctionnelles de ce gène sont plus grosses que celles possédant deux copies mutantes. La taille des souris hétérozygotes à ce locus dépend du parent d'où provient l' allèle de type sauvage . Si l'allèle fonctionnel provient de la mère, la progéniture présentera un nanisme , alors qu'un allèle paternel générera une souris de taille normale. C'est parce que le gène maternel Igf2 est imprimé. L'empreinte entraîne l'inactivation du gène Igf2 sur le chromosome transmis par la mère.
Les empreintes sont formées en raison de la méthylation différentielle des allèles paternels et maternels. Il en résulte une expression différente entre les allèles des deux parents. Les sites présentant une méthylation significative sont associés à de faibles niveaux d' expression génique . Une expression génique plus élevée est trouvée sur les sites non méthylés. Dans ce mode de transmission, le phénotype est déterminé non seulement par l'allèle spécifique transmis à la descendance, mais aussi par le sexe du parent qui l'a transmis.
Mosaïcisme
Les individus qui possèdent des cellules présentant des différences génétiques par rapport aux autres cellules de leur corps sont appelés mosaïques. Ces différences peuvent résulter de mutations qui se produisent dans différents tissus et à différentes périodes de développement. Si une mutation se produit dans les tissus non gamètes, elle est caractérisée comme somatique . Les mutations de la lignée germinale se produisent dans l'ovule ou les spermatozoïdes et peuvent être transmises à la progéniture. Les mutations qui se produisent tôt dans le développement affecteront un plus grand nombre de cellules et peuvent donner lieu à un individu qui peut être identifié comme une mosaïque strictement basée sur le phénotype.
Le mosaïcisme résulte également d'un phénomène connu sous le nom de X-inactivation . Tous les mammifères femelles ont deux chromosomes X . Pour éviter des problèmes de dosage de gènes mortels , l'un de ces chromosomes est inactivé après la fécondation . Ce processus se produit de manière aléatoire pour toutes les cellules du corps de l'organisme. Étant donné que les deux chromosomes X d'une femme donnée différeront presque certainement dans leur modèle spécifique d'allèles, cela entraînera des phénotypes cellulaires différents selon le chromosome qui est réduit au silence. Les chats Calico , qui sont presque tous des femelles, présentent l'une des manifestations les plus couramment observées de ce processus.
Troubles de la répétition des trinucléotides
Les troubles de la répétition des trinucléotides suivent également un modèle d'hérédité non mendélienne. Ces maladies sont toutes causées par l'expansion des répétitions en tandem des microsatellites constituées d'un tronçon de trois nucléotides . Typiquement chez les individus, le nombre d'unités répétées est relativement faible. Avec chaque génération successive, il y a une chance que le nombre de répétitions augmente. Au fur et à mesure que cela se produit, la descendance peut progresser vers la prémutation et finalement le statut affecté. Les personnes dont le nombre de répétitions se situe dans la plage de prémutation ont de bonnes chances d'avoir des enfants affectés. Ceux qui progressent vers le statut affecté présenteront les symptômes de leur maladie particulière. Les principaux troubles de la répétition des trinucléotides comprennent le syndrome de l'X fragile et la maladie de Huntington . Dans le cas du syndrome de l'X fragile, on pense que les symptômes résultent de l'augmentation de la méthylation et de l'expression réduite qui l'accompagne du gène de retard mental de l'X fragile chez les individus avec un nombre suffisant de répétitions.
Voir également
- Entraînement méiotique
- Hypothèse du CRR
- Héritage épigénétique
- Génération de gènes
- Conflit intranomique