Pyran - Pyran
|
|||
|
|
|||
| Des noms | |||
|---|---|---|---|
|
Nom IUPAC
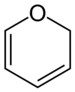
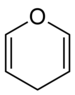
2 H -Pyrane, 4 H -Pyrane
|
|||
| Autres noms
2 H -Oxine, 4 H -Oxine
|
|||
| Identifiants | |||
|
Modèle 3D ( JSmol )
|
|||
| ChemSpider | |||
|
PubChem CID
|
|||
|
Tableau de bord CompTox ( EPA )
|
|||
|
|||
|
|||
| Propriétés | |||
| C 5 H 6 O | |||
| Masse molaire | 82,102 g · mol −1 | ||
| Composés apparentés | |||
|
Composés apparentés
|
Dihydropyran Tétrahydropyrane |
||
|
Sauf indication contraire, les données sont données pour les matériaux dans leur état standard (à 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Références Infobox | |||
En chimie , pyrane , ou oxine , est un cycle hétérocyclique non aromatique à six chaînons , composé de cinq atomes de carbone et d'un atome d' oxygène et contenant deux doubles liaisons . La formule moléculaire est C 5 H 6 O. Il existe deux isomères du pyrane qui diffèrent par l'emplacement des doubles liaisons. Dans le 2 H -pyrane , le carbone saturé est en position 2, tandis que dans le 4 H -pyrane , le carbone saturé est en position 4.
Le 4 H- pyrane a été isolé et caractérisé pour la première fois en 1962 par pyrolyse du 2-acétoxy-3,4-dihydro-2 H -pyrane. Il a été trouvé trop instable, notamment en présence d'air. Le 4 H- pyrane se disproportionnait facilement en dihydropyrane correspondant et en ion pyrylium , qui est facilement hydrolysé en milieu aqueux.
Bien que les pyranes eux-mêmes aient peu d'importance en chimie, nombre de leurs dérivés sont des molécules biologiques importantes, telles que les pyranoflavonoïdes .
Le terme pyrane est également souvent appliqué à l'analogue de cycle saturé, qui est plus correctement appelé tétrahydropyrane (oxane). Dans ce contexte, les monosaccharides contenant un système cyclique à six chaînons sont appelés pyranoses .