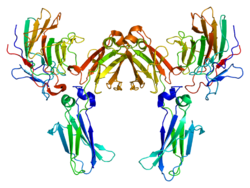TRIM21 - TRIM21
La protéine 21 contenant un motif tripartite , également connue sous le nom d' ubiquitine-protéine ligase E3 TRIM21 , est une protéine qui, chez l'homme, est codée par le gène TRIM21 . Des variantes de transcrits épissés de manière alternative pour ce gène ont été décrites, mais la nature complète d'un seul a été déterminée. Il est exprimé dans la plupart des tissus humains.
Structure
TRIM21 fait partie de la famille des motifs tripartites (TRIM). Le motif TRIM comprend trois domaines de liaison de zinc, d' un domaine à doigt RING , un type-boîte de B 1 et de type boîte B 2 doigts de zinc , et une bobine enroulée région.
Fonction
TRIM21 est un effecteur d'anticorps intracellulaire dans la voie de protéolyse médiée par les anticorps intracellulaires . Il reconnaît le domaine Fc et se lie à l' immunoglobuline G , à l' immunoglobuline A et à l' immunoglobuline M sur des virions non enveloppés marqués d'anticorps qui ont infecté la cellule. Soit par autoubiquitination, soit par ubiquitination d'un cofacteur, il est alors chargé de diriger les virions vers le protéasome . TRIM21 lui-même n'est pas dégradé dans le protéasome contrairement à la capside virale et à l'anticorps lié.
TRIM21 fait partie de la ribonucléoprotéine RoSSA, qui comprend un seul polypeptide et l'une des quatre petites molécules d'ARN. La particule RoSSA se localise à la fois dans le cytoplasme et dans le noyau.
Signification clinique
RoSSA interagit avec les auto-antigènes chez les patients atteints du syndrome de Sjögren et du lupus érythémateux disséminé . De plus, l'incapacité des macrophages à tendance lupique à dégrader les complexes immuns dans le lysosome entraîne la fuite d'auto-anticorps dans le cytosol qui peuvent se lier à TRIM21 et améliorer la signalisation NF-κB.
TRIM21 peut être utilisé pour éliminer des protéines spécifiques avec leurs anticorps correspondants, une méthode connue sous le nom de Trim-Away. Dans cet essai, TRIM21 et les anticorps sont délivrés dans les cellules par électroporation et la protéine ciblée est dégradée en quelques minutes.
Les références
Lectures complémentaires
- Jones SK (juin 1992). "Le rayonnement ultraviolet (UV) induit l'expression de l'antigène Ro/SSA à la surface des cellules par les kératinocytes humains in vitro : un mécanisme possible pour l'induction par UVR des lésions de lupus cutané". Le British Journal of Dermatology . 126 (6) : 546–53. doi : 10.1111/j.1365-2133.1992.tb00098.x . PMID 1610705 . S2CID 24542694 .
- Itoh K, Itoh Y, Frank MB (janvier 1991). "Hétérogénéité des protéines dans les ribonucléoprotéines Ro/SSA humaines. Les auto-antigènes Ro/SSA de 52 et 60 kD sont codés par des gènes séparés" . Le Journal d'Investigation Clinique . 87 (1) : 177-86. doi : 10.1172/JCI114968 . PMC 295020 . PMID 1985094 .
- Chan EK, Hamel JC, Buyon JP, Tan EM (janvier 1991). "Définition moléculaire et motifs de séquence du composant de 52 kD de l'auto-antigène SS-A/Ro humain" . Le Journal d'Investigation Clinique . 87 (1) : 68-76. doi : 10.1172/JCI115003 . PMC 294993 . PMID 1985112 .
- Miyagawa S, Okada N, Inagaki Y, Kitano Y, Ueki H, Sakamoto K, Steinberg ML (mars 1988). « Expression de l'antigène SSA/Ro dans les kératinocytes humains transformés par le virus simien 40 » . Le Journal de la dermatologie d'investigation . 90 (3) : 342-5. doi : 10.1111/1523-1747.ep12456308 . PMID 2450143 .
- Chan EK, Di Donato F, Hamel JC, Tseng CE, Buyon JP (octobre 1995). "52-kD SS-A/Ro: structure génomique et identification d'un transcrit épissé alternativement codant pour un nouvel autoantigène leucine zipper-moins exprimé dans le cœur fœtal et adulte" . Le Journal de la médecine expérimentale . 182 (4) : 983-92. doi : 10.1084/jem.182.4.983 . PMC 2192297 . PMID 7561701 .
- Tsugu H, Horowitz R, Gibson N, Frank MB (décembre 1994). « L'emplacement d'un polymorphisme associé à la maladie et de la structure génomique du locus Ro/SSA humain de 52 kDa (SSA1) ». Génomique . 24 (3) : 541–8. doi : 10.1006/geno.1994.1664 . PMID 7713506 .
- Frank MB, McCubbin VR, Heldermon C (janvier 1995). "Expression et liaison à l'ADN de l'auto-antigène Ro/SSA humain de 52 kDa" . Le Journal Biochimique . 305 (2) : 359-62. doi : 10.1042/bj3050359 . PMC 1136368 . PMID 7832745 .
- Maruyama K, Sugano S (janvier 1994). « Oligo-capping : une méthode simple pour remplacer la structure de la coiffe des ARNm eucaryotes par des oligoribonucléotides ». Gène . 138 (1–2) : 171–4. doi : 10.1016/0378-1119(94)90802-8 . PMID 8125298 .
- Keech CL, Gordon TP, McCluskey J (mai 1996). "Différences structurelles entre les auto-antigènes Ro de 52 kD humains et souris associés à une activité d'auto-anticorps mal conservée à travers les espèces" . Immunologie Clinique et Expérimentale . 104 (2) : 255–63. doi : 10.1046/j.1365-2249.1996.16726.x . PMC 2200432 . PMID 8625517 .
- Igarashi T, Itoh Y, Fukunaga Y, Yamamoto M (1996). « Expression de surface cellulaire induite par le stress et altération antigénique de l'auto-antigène Ro/SSA ». Auto-immunité . 22 (1) : 33-42. doi : 10.3109/08916939508995297 . PMID 8882420 .
- Suzuki Y, Yoshitomo-Nakagawa K, Maruyama K, Suyama A, Sugano S (octobre 1997). « Construction et caractérisation d'une bibliothèque d'ADNc enrichie sur toute la longueur et enrichie en 5' ». Gène . 200 (1–2) : 149–56. doi : 10.1016/S0378-1119 (97) 00411-3 . PMID 9373149 .
- Bepler G, O'briant KC, Kim YC, Schreiber G, Pitterle DM (janvier 1999). « Une carte physique haute résolution de 1,4 Mb et un contig du segment chromosomique 11p15.5 et des gènes dans la région suppressive de métastases LOH11A ». Génomique . 55 (2) : 164-75. doi : 10.1006/geno.1998.5659 . PMID 9933563 .
- Tseng CE, Miranda E, Di Donato F, Boutjdir M, Rashbaum W, Chan EK, Buyon JP (février 1999). « Expression d'ARNm et de protéines de SSA/Ro et SSB/La dans des myocytes cardiaques fœtaux humains cultivés à l'aide d'une nouvelle application de la procédure de Langendorff » . Recherche Pédiatrique . 45 (2) : 260-9. doi : 10.1203/00006450-19902000-00018 . PMID 10022600 .
- Fabini G, Rutjes SA, Zimmermann C, Pruijn GJ, Steiner G (mai 2000). "Analyse de la composition moléculaire des complexes ribonucléoprotéiques Ro. Identification de nouvelles protéines de liaison à l'ARN Y" . Journal Européen de Biochimie . 267 (9) : 2778-89. doi : 10.1046/j.1432-1327.2000.01298.x . PMID 10785401 .
- Kurien BT, Chambers TL, Thomas PY, Frank MB, Scofield RH (mars 2001). "L'auto-anticorps contre la région de fermeture à glissière leucine de 52 kDa Ro/SSA lie 60 kDa Ro/SSA natif : identification d'un épitope tertiaire avec des composants de 60 kDa Ro/SSA et 52 kDa Ro/SSA" . Journal scandinave d'immunologie . 53 (3) : 268–76. doi : 10.1046/j.1365-3083.2001.00870.x . PMID 11251884 . S2CID 7923255 .
- Reymond A, Meroni G, Fantozzi A, Merla G, Cairo S, Luzi L, Riganelli D, Zanaria E, Messali S, Cainarca S, Guffanti A, Minucci S, Pelicci PG, Ballabio A (mai 2001). "La famille de motifs tripartite identifie les compartiments cellulaires" . Le Journal de l'EMBO . 20 (9) : 2140–51. doi : 10.1093/emboj/20.9.2140 . PMC 125245 . PMID 11331580 .
- Di Donato F, Chan EK, Askanase AD, Miranda-Carus M, Buyon JP (septembre 2001). « Interaction entre 52 kDa SSA/Ro et l'enzyme désubiquitinante UnpEL : un indice pour fonctionner ». Le Journal International de Biochimie et de Biologie Cellulaire . 33 (9) : 924-34. doi : 10.1016/S1357-2725(01)00055-3 . PMID 11461834 .
- Fukuda-Kamitani T, Kamitani T (juillet 2002). « Ubiquitination d'autoantigène Ro52 ». Communications de recherche biochimique et biophysique . 295 (4) : 774-8. doi : 10.1016/S0006-291X(02)00750-7 . PMID 12127959 .