Vanadocène - Vanadocene

|
|
| Noms | |
|---|---|
|
Nom IUPAC
Bis (cyclopentadiényl) vanadium
|
|
| Autres noms
Vanadocène
|
|
| Identifiants | |
|
Modèle 3D ( JSmol )
|
|
| Carte Info ECHA |
100.149.756 |
|
PubChem CID
|
|
| UNII | |
|
Tableau de bord CompTox ( EPA )
|
|
|
|
| Propriétés | |
| V (C 5 H 5 ) 2 | |
| Masse molaire | 181,128 g / mol |
| Apparence | Cristal violet |
| Point de fusion | 167 ° C (333 ° F; 440 K) |
|
Sauf indication contraire, les données sont données pour les matériaux dans leur état standard (à 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Références Infobox | |
Le vanadocène , bis (η 5 -cyclopentadiényl) vanadium, est le composé organométallique de formule V (C 5 H 5 ) 2 , communément abrégé Cp 2 V. Il s'agit d'un solide paramagnétique cristallin violet. Le vanadocène a une utilisation pratique relativement limitée, mais il a été largement étudié.
Structure et collage
V (C 5 H 5 ) 2 est un métallocène , une classe de composés organométalliques qui ont typiquement un ion métallique pris en sandwich entre deux cycles cyclopentadiényle. A l'état solide, la molécule a une symétrie D 5d . Le centre du vanadium (II) réside à égale distance entre le centre des deux cycles cyclopentadiényle à un centre cristallographique d'inversion. La distance moyenne des liaisons VC est de 226 pm. Les anneaux Cp du vanadocène sont désordonnés dynamiquement à des températures supérieures à 170 K et ne sont entièrement commandés qu'à 108 K.
Préparation
Le vanadocène a été préparé pour la première fois en 1954 par Birmingham, Fischer et Wilkinson via une réduction du dichlorure de vanadocène avec de l'hydrure d'aluminium, après quoi le vanadocène a été sublimé sous vide à 100 ° C. Une synthèse moderne de vanadocène qui permet une production en plus grandes quantités nécessite de traiter [V 2 Cl 3 (THF) 6 ] 2 [Zn 2 Cl 6 ] avec du cyclopentadiénylsodium .
- 2 [V 2 Cl 3 (THF) 6 ] 2 [Zn 2 Cl 6 ] + 8 NaCp + THF → 4 Cp 2 V
Propriétés
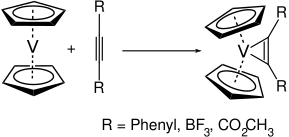
Le vanadocène est une molécule réactive. Comme il ne dispose que de 15 électrons de valence, il réagit facilement avec de nombreux ligands. Avec les alcynes, par exemple, il réagit pour donner les complexes vanadium-cyclopropène correspondants.
Une réaction implique du monoxyde de carbone, conduisant à un dérivé ionique du vanadocène lorsqu'elle est effectuée dans une atmosphère inerte:
- Cp 2 V + V (CO) 6 → [Cp 2 V (CO) 2 ] [V (CO) 6 ]
Le vanadocène est facilement oxydé en monocation lorsqu'il est traité avec un sel de ferrocénium dans le toluène.
- VCp 2 + [FeCp 2 ] BR 4 → [VCp 2 ] BR 4 + FeCp 2 (R = Ph ou 4-C 6 H 4 F)
Ces monocations sont extrêmement sensibles à l'air et ont un potentiel redox de -1,10 V.
Le vanadocène réagit avec des pressions élevées de monoxyde de carbone pour donner CpV (CO) 4 .