Annulène - Annulene

Les annulènes sont des hydrocarbures monocycliques qui contiennent le nombre maximum de doubles liaisons non cumulées (« mancude »). Ils ont la formule générale C n H n (lorsque n est un nombre pair) ou C n H n +1 (lorsque n est un nombre impair). Les conventions de dénomination de l'IUPAC sont que les annulènes avec 7 atomes de carbone ou plus sont appelés [ n ] annulène, où n est le nombre d' atomes de carbone dans leur cycle, bien que parfois les annulènes plus petits soient désignés en utilisant la même notation, et le benzène est parfois appelé simplement annulène.
Les trois premiers annulènes pairs sont le cyclobutadiène , le benzène et le cyclooctatétraène ([8] annulène). Certains annulènes, à savoir le cyclobutadiène, le cyclodécapentaène ([10] annulène), le cyclododécahexaène ([12] annulène) et le cyclotétradécaheptaène ([14] annulène), sont instables, le cyclobutadiène étant extrêmement instable.
Dans les annulynes liées , une double liaison est remplacée par une triple liaison .
Aromaticité
| n | aromaticité |
|---|---|
| 4 | antiaromatique |
| 6 | aromatique |
| 8 | non aromatique |
| dix | non aromatique |
| 12 | faiblement antiaromatique |
| 14 | faiblement aromatique |
| 16 | non aromatique |
| 18 | aromatique |
Les annulènes peuvent être aromatiques (benzène, [6] annulène et [18] annulène), non aromatiques ([8] et [10] annulène) ou anti-aromatiques (cyclobutadiène, [4] annulène). Le cyclobutadiène est le seul annulène avec une antiaromaticité considérable, car la planéité est inévitable. Avec l'annulène [8], la molécule prend une forme de cuve qui lui permet d'éviter la conjugaison de doubles liaisons. [10] L'annulène est de la mauvaise taille pour obtenir une structure plane: dans une conformation plane, déformation cyclique due soit à l' encombrement stérique des hydrogènes internes (lorsque certaines doubles liaisons sont trans ) ou à la distorsion de l'angle de liaison (lorsque les doubles liaisons sont toutes cis ) est inévitable. Ainsi, il ne présente pas d'aromaticité appréciable.
Lorsque l'annulène est suffisamment grand, [18] l'annulène par exemple, il y a suffisamment de place à l'intérieur pour recevoir des atomes d'hydrogène sans distorsion significative des angles de liaison. [18] L'annulène possède plusieurs propriétés qui le qualifient d'aromatique. Cependant, aucun des annulènes plus gros n'est aussi stable que le benzène, car leur réactivité ressemble plus étroitement à un polyène conjugué qu'à un hydrocarbure aromatique.
En général, les espèces d'annulène chargées de la forme [C 4 n +2+ q H 4 n +2+ q ] q ( n = 0, 1, 2, ..., q = 0, ± 1, ± 2, 4 n + 2 + q ≥ 3) sont aromatiques, à condition qu'une conformation plane puisse être obtenue. Par exemple, C 5 H 5 - , C 3 H 3 + et C 8 H 8 2– sont toutes des espèces aromatiques connues.
Galerie
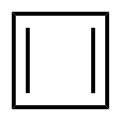
Cyclobutadiène ([4] annulène)
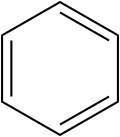
Benzène ([6] annulène)
Cyclooctatétraène ([8] annulène)
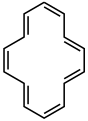
Cyclododécahexaène ([12] annulène)
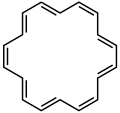
Cyclotétradécaheptaène ([14] annulène)
Cyclooctadécanonaène ([18] annulène)
Voir également
Les références
Liens externes
- NIST Chemistry WebBook - [18] annulène
- Structure de [14] et [18] annulène