Sous-oxyde de bore - Boron suboxide

|
|
| Noms | |
|---|---|
|
Nom IUPAC
Sous-oxyde de bore
|
|
| Autres noms
Monoxyde d'hexabore
|
|
| Identifiants | |
|
Modèle 3D ( JSmol )
|
|
|
|
|
|
| Propriétés | |
| B 6 O | |
| Masse molaire | 80,865 g/mol |
| Apparence | Cristaux jumelés icosaédriques rougeâtres |
| Densité | 2,56 g / cm 3 |
| Point de fusion | 2 000 °C (3 630 °F; 2 270 K) |
| Structure | |
| Rhomboédrique , hR42 | |
| R 3 , n° 166 | |
|
a = 0,53824 nm, b = 0,53824 nm, c = 1,2322 nm
= 90°, = 90°, = 120°
|
|
|
Unités de formule ( Z )
|
6 |
|
Sauf indication contraire, les données sont données pour les matériaux dans leur état standard (à 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Références de l'infobox | |
Le sous-oxyde de bore (formule chimique B 6 O) est un composé solide dont la structure est constituée de huit icosaèdres aux sommets de la maille rhomboédrique . Chaque icosaèdre est composé de douze atomes de bore . Deux atomes d' oxygène sont situés dans les interstices le long de la direction rhomboédrique [111]. En raison de ses courtes longueurs de liaisons interatomiques et de son caractère fortement covalent, le B 6 O présente une gamme de propriétés physiques et chimiques exceptionnelles telles qu'une grande dureté (proche de celle du diborure de rhénium et du nitrure de bore ), une faible densité de masse, une conductivité thermique élevée, une résistance chimique élevée. inertie et excellente résistance à l'usure.
Le B 6 O peut être synthétisé par réduction du B 2 O 3 avec du bore ou par oxydation du bore avec de l'oxyde de zinc ou d'autres oxydants. Ces matériaux de sous-oxyde de bore formés à ou près de la pression ambiante sont généralement pauvres en oxygène et non stoechiométriques (B 6 O x , x < 0,9) et ont une mauvaise cristallinité et une très petite taille de grain (inférieure à 5 µm). Une pression élevée appliquée pendant la synthèse de B 6 O peut augmenter considérablement la cristallinité, la stoechiométrie de l'oxygène et la taille des cristaux des produits. Des mélanges de poudres de bore et de B 2 O 3 étaient généralement utilisés comme matières de départ dans les méthodes rapportées pour la synthèse de B 6 O.
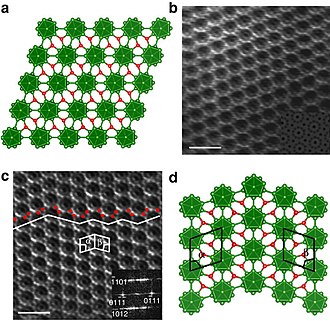
Le sous-oxyde de bore pauvre en oxygène (B 6 O x , x<0,9) pourrait former des particules icosaédriques , qui ne sont ni des monocristaux ni des quasicristaux , mais des groupes jumelés de vingt cristaux tétraédriques .
Le B 6 O de type bore -rhomboédrique a été étudié en raison de sa nature céramique (dureté, point de fusion élevé, stabilité chimique et faible densité) en tant que nouveau matériau structurel. En plus de cela, ces borures ont une liaison unique qui n'est pas facilement accessible par la théorie de valence habituelle. Bien qu'une méthode de spectroscopie d'émission de rayons X ait indiqué une plage de paramètres probable pour le site d'oxygène de B 6 O, la position correcte de l'oxygène est restée en question jusqu'à ce que l' analyse de Rietveld des profils de diffraction des rayons X sur des poudres de B 6 O ait été réalisée avec succès, même s'il s'agissait d'enquêtes préliminaires.
Préparation
Le B 6 O peut être préparé par trois méthodes :
- (1) réaction à l'état solide entre B et B 2 O 3 ,
- (2) réduction de B 2 O 3 et
- (3) oxydation de B . La pression de vapeur élevée de B 2 O 3 à des températures élevées provoquerait l' excès de B composition dans le processus de la réaction à l'état solide entre B et B 2 O 3 .
Dans la réduction de B 2 O 3 , des réducteurs qui peuvent être utilisés comprennent, mais sans s'y limiter, Si et Mg qui restent dans B 6 O sous forme d'impureté dans le processus. Pendant le processus d'oxydation de B , des oxydants tels que ZnO contamineraient B 6 O dans le processus.
Propriétés physiques
B 6 O a une forte nature covalente et est facile à composer à des températures supérieures à 1 973 K. Il a également été rapporté que le sous-oxyde de bore présente une large gamme de propriétés supérieures telles qu'une dureté élevée avec une faible densité, une résistance mécanique élevée, une résistance à l'oxydation jusqu'à hautes températures ainsi que sa grande inertie chimique. Des calculs fonctionnels de densité ab initio préliminaires du premier principe des propriétés structurelles du sous-oxyde de bore (B 6 O) suggèrent que la force de liaison dans B 6 O peut être améliorée par la présence d'un interstitiel à haute électronégativité dans la structure. Les calculs informatiques confirment le raccourcissement des liaisons covalentes, ce qui favoriserait des constantes élastiques et des valeurs de dureté plus élevées.
Applications
Les applications potentielles du B 6 O en tant que revêtement réduisant l'usure pour les outils de coupe à grande vitesse, les abrasifs ou d'autres applications à forte usure, par exemple, ont fait l'objet d'un intérêt intense ces dernières années. Cependant, malgré des efforts de recherche intensifs, des applications commerciales n'ont pas encore été réalisées. Ceci est en partie dû à la faible ténacité à la rupture du matériau pressé à chaud et aux défis pratiques considérables associés à la densification du matériau B 6 O stoechiométrique avec une bonne cristallinité. De plus, de nombreuses propriétés mécaniques du matériau étaient jusqu'à récemment assez mal comprises.
Le bore est également un sous - oxyde prometteur armure de corps matériel, mais son test est encore aux premiers stades et aucun déploiement commercial est connu sous le nom de 2019.