Cancer du poumon EML4-ALK positif - EML4-ALK positive lung cancer
| Cancer du poumon EML4-ALK positif | |
|---|---|
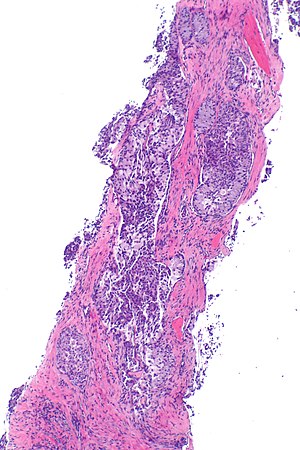 | |
| Micrographie montrant un adénocarcinome pulmonaire ALK positif. Tache H&E . | |
| Spécialité | Oncologie |
Cancer du poumon positif EML4-ALK est un primaire maligne tumeur du poumon dont les cellules contiennent une configuration anormale caractéristique de l' ADN dans lequel la protéine analogue à 4 associée aux microtubules d'échinodermes ( EML4 ) gène est fusionné à la kinase du lymphome anaplasique ( ALK ) gène . Cette fusion anormale de gènes conduit à la production d'une protéine ( EML4-ALK ) qui semble, dans de nombreux cas, favoriser et maintenir le comportement malin des cellules cancéreuses .
Le gène de fusion transformant EML4-ALK a été signalé pour la première fois dans le carcinome pulmonaire non à petites cellules (NSCLC) en 2007.
Signes et symptômes
Les signes et symptômes de cette variante du cancer du poumon semblent imiter ceux du type cellulaire majeur sous-jacent.
Diagnostic
Classification
La plupart des carcinomes pulmonaires contenant la fusion du gène EML4-ALK sont des adénocarcinomes .
Certaines études suggèrent que l' adénocarcinome papillaire et les variantes de l' adénocarcinome à cellules en bague à chevalière sont plus susceptibles de porter ce gène fusionné que d'autres variantes histologiques.
Dépistage
Le dépistage du cancer du poumon ALK positif est désormais une norme de soins aux États-Unis et au Canada. Le dépistage peut être effectué par immunocoloration, FISH ou par séquençage de nouvelle génération (NGS).
Traitement
Le crizotinib est une thérapie ciblée (approuvée par la FDA en 2011), fabriquée par Pfizer et commercialisée sous les marques Xalkori et Crizalk qui cible le gène de fusion EML4/ALK.
Le céritinib est une thérapie ciblée de deuxième génération (approuvée par la FDA en 2014), fabriquée par Novartis et vendue sous le nom de marque Zykadia qui cible également le gène de fusion EML4, mais en tant que médicament de deuxième génération, il a une molécule plus petite qui permet une pénétration supérieure du sang Barrière cérébrale (BHE) par rapport au crizotinib et est plus capable de protéger le système nerveux central (SNC).
Alectinib est une autre thérapie ciblée de deuxième génération et a été approuvé (pour cela) par le Japon en 2014 et par la FDA américaine en 2015., fabriqué par Genentech et commercialisé sous le nom de marque Alecensa.
Brigatinib, une thérapie ciblée de deuxième génération (approuvée par la FDA en 2017), fabriquée par Takeda et commercialisée sous le nom de marque Alunbrig.
L'ensartinib est une thérapie ciblée de deuxième génération (médicament d'essai X-396), fabriqué par XCovery.
Lorlatinib est une thérapie ciblée de troisième génération (en attente de l'approbation de la FDA sous le médicament d'essai PF-6463922), fabriqué par Pfizer.
TPX-0005 est un nouvel essai thérapeutique ciblé de troisième génération.
Pronostic
Le traitement par crizotinib atteint un taux de réponse de 60 % . Cependant, le crizotinib n'a montré aucune amélioration de la survie globale par rapport à la chimiothérapie. Cela peut être dû au fait qu'il y avait un taux de croisement de 70 % avec le crizotinib chez les patients traités initialement par chimiothérapie. De plus, les patients dont le test de fusion EML4/ALK était négatif ont présenté un taux de réponse au crizotinib pouvant atteindre 35 %.
Épidémiologie
Les fusions de gènes EML4-ALK se produisent presque exclusivement dans des carcinomes survenant chez des non-fumeurs. Environ 4 % des carcinomes pulmonaires non à petites cellules impliquent un gène de fusion EML4-ALK tyrosine kinase. 4 à 6 % des adénocarcinomes pulmonaires impliquent le gène de fusion.
La mutation EML4-ALK se produit rarement en association avec des mutations K-RAS ou EGFR .

