Liste des cannabinoïdes AM - List of AM cannabinoids
Alexandros Makriyannis est professeur au Département de chimie médicinale de l'Université Northeastern , où son groupe de recherche a synthétisé de nombreux nouveaux composés ayant une activité cannabinoïde . Certains d'entre eux sont:
| Nom | Classer | K i / nM au CB 1 | K i / nM au CB 2 | Sélectivité | CLogP | Structure | La description |
|---|---|---|---|---|---|---|---|
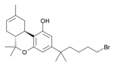
| AM-087 | Dibenzopyran | 0,43 | 6,47 |
|
Un agoniste analgésique CB 1 dérivé de Δ 8 THC substitué par une chaîne latérale en position 3, environ 100 fois plus puissant que le THC. | ||
| AM-251 | Dérivé de pyrazole | 7,5 | 7,08 |

|
Un agoniste inverse du récepteur cannabinoïde CB 1 qui est structurellement lié au SR141716A ( rimonabant ), mais qui a une affinité de liaison plus élevée. | ||
| AM-279 | Une substance de l'annexe I en Alabama. | ||||||
| AM-281 | N - (morpholin-4-yl) -1- (2,4-dichlorophényl) -5- (4-iodophényl) -4-méthyl-1H-pyrazole-3-carboxamide | ||||||
| AM-356 | 17,9 | 868 | 5,55 |

|
Un analogue chiral stable créé synthétiquement de l' anandamide , il agit sur les deux récepteurs cannabinoïdes. | ||
| AM-374 | Fluorure de palmitylsulfonyle | ||||||
| AM-381 | Fluorure de stéarylsulfonyle | ||||||
| AM-404 | 7.02 |

|
Un métabolite actif du paracétamol ( acétaminophène ) et un inhibiteur probable de l'amide hydrolase d'acide gras (FAAH) | ||||
| AM-411 | 6,80 | 52,0 |

|
Un dérivé adamantyl- substitué de Δ 8 THC , c'est un agoniste complet CB 1 puissant et assez sélectif et un agoniste CB 2 modérément puissant . | |||
| AM-630 | 32,1 | CB 2 (165 ×) | 4.19 |

|
Un agoniste inverse puissant et sélectif pour le récepteur cannabinoïde CB 2 et un agoniste partiel faible à CB 1 . | ||
| AM-661 | 1- ( N -méthyl-2-pipéridine) méthyl-2-méthyl-3- (2-iodo) benzoylindole | ||||||
| AM-678 | 9,00 ± 5,00 | 2,94 ± 2,65 | CB 2 | 5,68 |

|
Un autre nom pour JWH-018, c'est un agoniste complet des deux récepteurs cannabinoïdes avec une certaine sélectivité pour CB 2 . | |
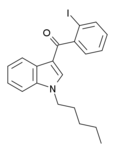
| AM-679 | 13,5 | 49,5 | 6,04 |
|
Un iodobenzoylindole qui agit comme un agoniste modérément puissant pour les deux récepteurs cannabinoïdes. | ||
| AM-694 | 0,08 | 1,44 | CB 1 (18 ×) | 5,54 |
|
Un iodobenzoylindole qui agit comme un agoniste puissant et sélectif du récepteur cannabinoïde CB 1 . | |
| AM-735 | 8,9 | 7.4 | 3-bornyl-Δ8-THC, un agoniste mixte CB 1 / CB 2 . | ||||
| AM-855 | 22,3 | 58,6 | CB 1 | 7,1 |

|
Dérivé analgésique du Δ 8 tétrahydrocannabinol , c'est un agoniste à la fois au CB 1 et au CB 2 avec une sélectivité modérée pour CB 1 . | |
| AM-881 | 5,3 | 95 | Stéréoisomère d'anandamide à substitution chlore. | ||||
| AM-883 | 9,9 | 226 | Stéréoisomère d'anandamide à substitution allyle. | ||||
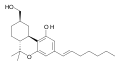
| AM-905 | 1.2 | 5,3 | CB 1 | 4,98 |
|
Un agoniste puissant et raisonnablement sélectif pour le récepteur cannabinoïde CB 1 . | |
| AM-906 | 0,8 | 9,5 | CB 1 | 4,98 |

|
Un agoniste puissant et sélectif dodéciquement pour le récepteur cannabinoïde CB 1 . | |
| AM-919 | 2.2 | 3.4 | CB 1 | 6,21 |

|
Un agoniste puissant à la fois CB 1 et CB 2 avec une sélectivité modérée pour CB 1 . C'est un dérivé du HU-210 et représente une structure hybride entre les familles de cannabinoïdes classiques et non classiques. | |
| AM-926 | 2.2 | 4.3 | CB 1 | Un agoniste puissant à la fois CB 1 et CB 2 avec une sélectivité modérée pour CB 1 . C'est un dérivé du HU-210 et représente une structure hybride entre les familles de cannabinoïdes classiques et non classiques. | |||
| AM-938 | 1.2 | 0,3 | CB 2 (4 ×) | 5,92 |

|
Un agoniste puissant à la fois CB 1 et CB 2 . C'est un dérivé du HU-210 et représente une structure hybride entre les familles de cannabinoïdes classiques et non classiques. | |
| AM-1116 | 7.4 | Un stéréoisomère diméthylé d'anandamide. | |||||
| AM-1172 | Analogue d'endocannabinoïde spécifiquement conçu pour être un inhibiteur puissant et sélectif de l'absorption d'AEA résistant à l'hydrolyse de FAAH. | ||||||
| AM-1220 | 3,88 | 73,4 | CB 1 (19 ×) | 4,73 |

|
Un agoniste analgésique puissant et sélectif de CB 1 (comme racémate ). L'énantiomère (R) a une affinité environ 1000 fois plus élevée pour CB 1 que pour l'énantiomère (S). | |
| AM-1221 | 52,3 | 0,28 | CB 2 (187 ×) |

|
Un agoniste CB 2 puissant et sélectif . | ||
| AM-1235 | 1,5 | 20,4 | CB 1 (13 ×) |

|
Un agoniste sélectif modérément CB 1 . | ||
| AM-1241 | 3.4 | CB 2 (80 ×) |

|
Un agoniste analgésique CB 2 puissant et sélectif . | |||
| AM-1248 | CB 1 |

|
Un agoniste modérément puissant avec une certaine sélectivité pour CB 1 , contenant une substitution inhabituelle 3- (adamant-1-oyl) sur le cycle indole. | ||||
| AM-1710 | Cannabilactone | CB 2 (54 ×) | Une cannabilactone sélective CB 2 . Agit comme un double agoniste CB 2 / antagoniste CB 1 . | ||||
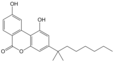
| AM-1714 | Cannabilactone | CB 2 (490 ×) | 6,17 |
|
Une cannabilactone sélective CB 2 . | ||
| AM-1902 | Un cannabinoïde non classique | ||||||
| AM-2201 | 1.0 | 2.6 | CB 1 | 5,18 |

|
Un agoniste puissant à la fois CB 1 et CB 2 avec une sélectivité modérée pour CB 1 . | |
| AM-2212 | 1,4 | 18,9 | CB 1 | Un agoniste puissant à la fois CB 1 et CB 2 avec sélectivité dodécale pour CB 1 . | |||
| AM-2213 | 3.0 | 30 | CB 1 (10 ×) | Un agoniste puissant à la fois CB 1 et CB 2 . | |||
| AM-2232 | 0,28 | 1,48 | 4,75 |

|
Un agoniste puissant à la fois CB 1 et CB 2 . | ||
| AM-2233 | 1,8 | 2.2 | CB 1 | 5,09 |

|
L'énantiomère (R) est un agoniste CB 1 puissant et sélectif utilisé sous forme radiomarquée 131 I pour cartographier la distribution des récepteurs CB 1 dans le cerveau. | |
| AM-2389 | 0,16 | CB 1 (26 ×) | 6 |

|
Dérivé cannabinoïde classique. | ||
| AM-3102 | 33 000 | 26 000 | Un analogue de l' oléoyléthanolamide , l'agoniste endogène du récepteur α activé par les proliférateurs ( PPARα ). Il agit également comme un agoniste cannabinoïde faible. | ||||
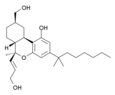
| AM-4030 | 0,7 | 8,6 | CB 1 (12 ×) | 6,17 |
|
Un agoniste puissant à la fois CB 1 et CB 2 , il est dodéciquement sélectif pour CB 1 . C'est un dérivé du HU-210 et représente une structure hybride entre les familles de cannabinoïdes classiques et non classiques. | |
| AM-4054 | 2.2 | CB 1 (40 ×) | Un agoniste puissant mais à action lente. | ||||
| AM-4056 | 0,041 | 6,51 |

|
Un autre nom pour HU-243, c'est un agoniste puissant à la fois les récepteurs CB 1 et CB 2 . | |||
| AM-4113 | CB 1 | Un antagoniste neutre sélectif CB 1 . | |||||
| AM-6545 | CB 1 | 4,06 |

|
Un antagoniste silencieux périphérique sélectif des récepteurs CB 1 . | |||
| AM-7438 |

|
Un agoniste puissant de CB 1 et CB 2 avec une durée d'action réduite. |
Voir également
- Liste des cannabinoïdes CP
- Liste des cannabinoïdes JWH
- Liste des cannabinoïdes HU
- Liste des divers cannabinoïdes de concepteur
Les références
- ^ un b Lan, Ruoxi; Lu, Qian; Fan, Pusheng; Gatley, John; Volkow, Nora D .; Fernando, Susanthi R .; Pertwee, Roger; Makriyannis, Alexandros (1999). "Conception et synthèse de l'antagoniste cannabinoïde sélectif CB1 AM281: Un ligand SPECT humain potentiel" . AAPS PharmSci . 1 (2): 39–45. doi : 10.1208 / ps010204 . PMC 2761119 . PMID 11741201 .
- ^ "Projet de loi 333 du Sénat de l'Alabama - substances contrôlées, annexe I, substances contrôlées synthétiques supplémentaires et substances analogues incluses dans, trafic d'analogues de substances contrôlées, poids requis augmenté, articles 13A-12-231, 20-2-23 am'd" . Mars 2014 . Récupéré le 28 septembre 2015 .
- ^ A b c d Selwood, D. (2009). "Les Récepteurs Cannabinoïdes. Edité par Patricia H. Reggio". ChemMedChem . 4 : 1949. doi : 10.1002 / cmdc.200900286 .
- ^ Pacher, P .; Bátkai, S; Kunos, G (2006). "Le système endocannabinoïde en tant que cible émergente de la pharmacothérapie" . Examens pharmacologiques . 58 (3): 389–462. doi : 10.1124 / pr.58.3.2 . PMC 2241751 . PMID 16968947 .
- ^ A b c Hongfeng Deng. Conception et synthèse de ligands sélectifs des récepteurs cannabinoïdes: Aminoalkylindole et autres analogues hétérocycliques. Thèse de doctorat, Université du Connecticut, 2000.
- ^ Brevet WO 200128557 , Makriyannis A, Deng H, "Dérivés d'indole cannabimimétiques", accordé le 07/06/2001
- ^ Lu, D; Guo, J; Duclos, RI Jr; Bowman, AL; Makriyannis, A (octobre 2008). "Bornyl- et isobornyl-Delta8-tétrahydrocannabinols: une nouvelle classe de ligands cannabinergiques" . Journal de chimie médicinale . 51 (20): 6393–9. doi : 10.1021 / jm8005299 . PMC 3700413 . PMID 18826296 .
- ^ D'ambra, T. (1996). "Aminoalkylindoles attachés en C: mimétiques puissants de cannabinoïdes". Lettres de chimie bioorganique et médicinale . 6 : 17-22. doi : 10.1016 / 0960-894X (95) 00560-G .
- ^ Willis, PG; Pavlova, OA; Chefer, SI; Vaupel, DB; Mukhin, AG; Horti, AG (2005). "Synthèse et relation structure-activité d'une nouvelle série d'aminoalkylindoles avec le potentiel d'imagerie du récepteur cannabinoïde neuronal par tomographie par émission de positrons". Journal de chimie médicinale . 48 (18): 5813–22. doi : 10.1021 / jm0502743 . PMID 16134948 .
- ^ un brevet américain b 7241799 , Makriyannis A, Deng H, "Dérivés d'indole cannabimimétiques", accordé le 2007-07-10
- ^ Poso, A .; Huffman, JW (2008). "Cibler le récepteur cannabinoïde CB2: modélisation et déterminants structurels des ligands sélectifs CB2" . Journal britannique de pharmacologie . 153 (2): 335–46. doi : 10.1038 / sj.bjp.0707567 . PMC 2219524 . PMID 17982473 .
- ^ un b Khanolkar, AD; Lu, D; Ibrahim, M; Duclos, RI Jr; Thakur, GA; Malan, TP; Porreca, F; Veerappan, V; Tian, X; George, C; Parrish, DA; Papahatjis, DP; Makriyannis, A (décembre 2007). "Cannabilactones: une nouvelle classe d'agonistes sélectifs CB2 avec une activité analgésique périphérique". Journal de chimie médicinale . 50 (26): 6493–500. doi : 10.1021 / jm070441u . PMID 18038967 .
- ^ Dhopeshwarkar, Amey; Murataeva, Natalia; Makriyannis, Alex; Straiker, Alex; Mackie, Ken (07/12/2016). "Deux cannabinoïdes Janus qui sont à la fois des agonistes de CB2 et des antagonistes de CB1" . Journal de pharmacologie et thérapeutique expérimentale . Société américaine de pharmacologie et de thérapeutique expérimentale (ASPET). 360 (2): 300–311. doi : 10.1124 / jpet.116.236539 . ISSN 0022-3565 . PMID 27927913 .
- ^ Luk, T; Jin, W; Zvonok, A; Lu, D; Lin, XZ; Chavkin, C; Makriyannis, A; Mackie, K (juin 2004). "Identification d'un puissant et très efficace, mais lentement désensibilisant un agoniste des récepteurs aux cannabinoïdes CB1" . Br J Pharmacol . 142 (3): 495–500. doi : 10.1038 / sj.bjp.0705792 . PMC 1574962 . PMID 15148260 .
- ^ Deng H, Gifford AN, Zvonok AM, Cui G, Li X, Fan P, Deschamps JR, Flippen-Anderson JL, Gatley SJ, Makriyannis A (octobre 2005). "Analogues d'indole cannabinergiques puissants comme agents d'imagerie cérébrale radioiodinables pour le récepteur cannabinoïde CB1". Journal de chimie médicinale . 48 (20): 6386–92. doi : 10.1021 / jm050135l . PMID 16190764 .
- ^ Hanuš, LRO; Mechoulam, R. (2005). "La chimie cannabinoïde: un aperçu". Les cannabinoïdes comme thérapeutiques . Jalons de la pharmacothérapie MDT. p. 23. doi : 10.1007 / 3-7643-7358-X_2 . ISBN 3-7643-7055-6 .
- ^ Shen CP, Xiao JC, Armstrong H, Hagmann W, Fong TM (février 2006). "La substitution de F200A dans la troisième hélice transmembranaire du récepteur de cannabinoïde CB1 humain convertit AM2233 d'agoniste de récepteur en agoniste inverse". Journal européen de pharmacologie . 531 (1–3): 41–6. doi : 10.1016 / j.ejphar.2005.12.026 . PMID 16438957 .
- ^ Dhawan, J .; Deng, H .; Gatley, SJ; Makriyannis, A .; Akinfeleye, T .; Bruneus, M .; Dimaio, AA; Gifford, AN (2006). "Évaluation de l'occupation du récepteur in vivo pour les effets comportementaux des cannabinoïdes en utilisant un agoniste des récepteurs cannabinoïdes radiomarqués, R- [125 / 131I] AM2233" . Synapse . 60 (2): 93-101. doi : 10.1002 / syn.20277 . PMID 16715483 .
- ^ Leung K (12 décembre 2006). "R-2- [131I] Iodophényl- (1- (1-méthylpipéridin-2-ylméthyl) -1H-indol-3-yl) méthanone". Base de données des agents d'imagerie moléculaire et de contraste (MICAD) [Internet] . PMID 20641836 .
- ^ Pei, Y .; et coll. (2008). "Architecture de liaison de ligand du récepteur de cannabinoïde CB2 humain: preuve pour le motif de liaison spécifique au sous-type de récepteur et la modélisation de l'activation de GPCR" . Chimie et biologie . 15 (11): 1207-1219. doi : 10.1016 / j.chembiol.2008.10.011 . PMC 3700404 . PMID 19022181 .
- ^ [Paronis CA, Thakur GA, Vemuri K, Makriyannis A, Bergman J. Effets d'un agoniste et antagoniste sélectif des cannabinoïdes sur la température corporelle chez les rats. Le journal FASEB . Avril 2007 21 (Supplément aux résumés de réunion) A409. http://www.fasebj.org/cgi/content/meeting_abstract/21/5/A409 ]
- ^ Paronis, Californie; Thakur, GA; Bajaj, S.; Nikas, SP; Vemuri, VK; Makriyannis, A .; Bergman, J. (2012). "Les effets diurétiques des cannabinoïdes" . Journal de pharmacologie et thérapeutique expérimentale . 344 (1): 8–14. doi : 10.1124 / jpet.112.199331 . PMC 3533417 . PMID 23019138 .
- ^ Seely, KA; Prather, PL; James, LP; Moran, JH (février 2011). "Médicaments à base de marijuana: thérapies innovantes ou drogues de synthèse abusives?" . Interventions moléculaires . 11 (1): 36–51. doi : 10.1124 / mi.11.1.6 . PMC 3139381 . PMID 21441120 .
- ^ Nikas SP, Sharma R, Paronis CA, Kulkarni S, Thakur GA, Hurst D, Wood JT, Gifford RS, Rajarshi G, Liu Y, Raghav JG, Guo JJ, Järbe TU, Reggio PH, Bergman J, Makriyannis A. Probing la chaîne latérale carboxyester en désactivation contrôlée (-) - δ (8) -tétrahydrocannabinols. J Med Chem . 22 janvier 2015; 58 (2): 665-81. doi : 10.1021 / jm501165d PMID 25470070
