Méthylmalonyl-CoA mutase - Methylmalonyl-CoA mutase
| méthylmalonyl-CoA mutase | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Identifiants | |||||||||
| CE n° | 5.4.99.2 | ||||||||
| N ° CAS. | 9023-90-9 | ||||||||
| Bases de données | |||||||||
| IntEnz | Vue IntEnz | ||||||||
| BRENDA | Entrée BRENDA | ||||||||
| ExPASy | Vue NiceZyme | ||||||||
| KEGG | Entrée KEGG | ||||||||
| MétaCycle | voie métabolique | ||||||||
| PRIAM | profil | ||||||||
| Structures de l' APB | RCSB PDB PDBe PDBsum | ||||||||
| Ontologie des gènes | AmiGO / QuickGO | ||||||||
| |||||||||
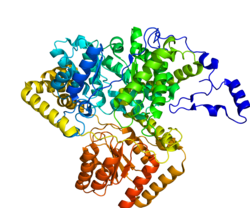
La méthylmalonyl-CoA mutase (MCM), mitochondriale , également connue sous le nom de méthylmalonyl-CoA isomérase , est une protéine qui chez l'homme est codée par le gène MUT . Cette vitamine B 12 enzyme catalyse l'isomérisation dépendante de methylmalonyl-CoA en succinyl-CoA chez l' homme. Des mutations du gène MUT peuvent conduire à divers types d' acidurie méthylmalonique .
Le MCM a été identifié pour la première fois dans le foie de rat et le rein de mouton en 1955. Sous sa forme latente, il a une longueur de 750 acides aminés . Lors de l'entrée dans les mitochondries, la séquence de tête mitochondriale de 32 acides aminés à l'extrémité N-terminale de la protéine est clivée, formant le monomère entièrement transformé. Les monomères s'associent ensuite en homodimères et se lient à AdoCbl (un pour chaque site actif de monomère) pour former la forme holoenzyme active finale .
Structure
Gène
Le gène MUT se trouve sur l' emplacement chromosomique de 6p12.3 et se compose de 13 exons , couvrant plus de 35 kb .
Protéine
L'enzyme mature est un homodimère avec le domaine de liaison à la CoA N-terminal et le domaine de liaison à la cobalamine C-terminal.
Fonction
La méthylmalonyl-CoA mutase est exprimée à des concentrations élevées dans les reins , à des concentrations intermédiaires dans le cœur , les ovaires , le cerveau , les muscles et le foie , et à de faibles concentrations dans la rate . L'enzyme peut être trouvée dans tout le système nerveux central (SNC). Le MCM réside dans les mitochondries, où un certain nombre de substances, y compris les acides aminés à chaîne ramifiée isoleucine et valine , ainsi que la méthionine , la thréonine , la thymine et les acides gras à chaîne impaire , sont métabolisés via le méthylmalonate semialdéhyde (MMlSA) ou le propionyl-CoA (Pr-CoA) en un composé commun - le méthylmalonyl-CoA (MMl-CoA). Le MCM catalyse l'isomérisation réversible de la l‐méthylmalonyl‐CoA en succinyl‐CoA, nécessitant la cobalamine (vitamine B12) sous forme d'adénosylcobalamine (AdoCbl) comme cofacteur. En tant qu'étape importante du catabolisme du propionate, cette réaction est nécessaire pour la dégradation des acides gras à chaîne impaire , les acides aminés valine , isoleucine , méthionine et thréonine , et le cholestérol , canalisant les métabolites de la décomposition de ces acides aminés en acide tricarboxylique cycle .
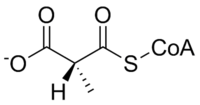
La méthylmalonyl-CoA mutase catalyse la réaction suivante :
| L-méthylmalonyl-CoA | méthylmalonyl-CoA mutase | Succinyl-CoA | |
|

|
||

|
|||
| méthylmalonyl-CoA mutase | |||
Le substrat de la méthylmalonyl-CoA mutase, la méthylmalonyl-CoA , est principalement dérivé du propionyl-CoA , une substance formée à partir du catabolisme et de la digestion de l' isoleucine , de la valine , de la thréonine , de la méthionine , de la thymine , du cholestérol ou des acides gras à chaîne impaire. Le produit de l'enzyme, le succinyl-CoA , est une molécule clé du cycle de l'acide tricarboxylique .
Signification clinique
Un déficit de cette enzyme est responsable d'un trouble héréditaire du métabolisme, le déficit en méthylmalonyl-CoA mutase , qui est l'une des causes de l' acidémie méthylmalonique (également appelée acidurie méthylmalonique ou MMA). Le MMA est une erreur innée héréditaire du métabolisme autosomique récessive , caractérisée par des épisodes récurrents de vomissements, de léthargie, d' acidocétose profonde , d' hyperammoniémie et de pancytopénie pendant la petite enfance, et peut entraîner une mort prématurée. Les complications comprennent une cardiomyopathie , un accident vasculaire cérébral métabolique , une pancréatite et une insuffisance rénale progressive .
Soit des mutations du gène MUT (code pour la méthylmalonyl-CoA mutase), soit du MMAA (code pour une protéine chaperon de la méthylmalonyl-CoA mutase, protéine MMAA ) peuvent conduire à une acidémie de méthylmalonyl. Les mutations en MUT peuvent être classées soit comme MUT 0 (ne démontre aucune activité même en présence d'un excès d'AdoCbl), soit comme MUT 1 (démontre une très faible activité en présence d'un excès d'AdoCbl). Plus de la moitié des mutations de MUT sont des mutations faux- sens tandis que les mutations non-sens constituent une fraction restante significative (environ 14%)
Les méthodes de traitement courantes pour le MMA comprennent une greffe de foie ou une greffe de foie et de rein pour lutter contre la maladie rénale de l'acidémie méthylmalonique. Cependant, des effets neurologiques néfastes peuvent continuer à affecter les patients même après une opération réussie. On pense que cela est dû à la présence répandue de méthylmalonyl-CoA mutase dans tout le système nerveux central. En raison de la perte de fonctionnalité de l'enzyme, les niveaux de substrat s'accumulent dans le SNC. Le substrat, le L-méthylmalonyl-CoA, s'hydrolyse pour former le méthylmalonate (acide méthylmalonique), un acide dicarboxylique neurotoxique qui, en raison des faibles capacités de transport de l'acide dicarboxylique de la barrière hémato-encéphalique, est efficacement piégé dans le SNC, entraînant un affaiblissement neurologique. Pour lutter contre ces effets, des régimes anti-cataboliques périopératoires et aucune interruption de régime sont recommandés.
Le modèle murin s'est avéré un moyen adéquat et précis d'étudier les effets du MMA et les méthodes de traitement potentielles.
Mécanisme
Le mécanisme de réaction MCM commence par le clivage homolytique de la liaison C- Co (III) d'AdoB12 , les atomes C et Co acquièrent chacun l'un des électrons qui ont formé la liaison de paire d'électrons clivée. L'ion Co fluctue donc entre ses états d'oxydation Co(III) et Co(II) [les deux états sont distinguables spectroscopiquement : Co(III) est rouge et diamagnétique (pas d'électrons non appariés), tandis que Co(II) est jaune et paramagnétique (électrons non appariés)]. Ainsi, le rôle de la coenzyme B-12 dans le processus catalytique est celui d'un générateur réversible d'un radical libre . La liaison C-Co(III) est faible, avec une énergie de dissociation = 109 kJ/mol, et semble encore affaiblie par les interactions stériques avec l'enzyme. La réaction homolytique est inhabituelle en biologie, tout comme la présence d'une liaison métal-carbone.
La méthylmalonyl-CoA mutase est un membre de la sous-famille des isomérases des enzymes dépendantes de l'adénosylcobalamine. De plus, il est classé dans la classe I, car il s'agit d'une enzyme « DMB-off »/« His-on ». Cela fait référence à la nature du cofacteur AdoCbl dans le site actif du méthylmalonyl CoA. AdoCbl est composé d'un noyau central de corrine contenant du cobalt , d'un ligand axial supérieur (ligand β-axial) et d'un ligand axial inférieur (ligand α-axial). Dans la méthylmalonyl-CoA mutase, le ligand -axial 5'-désoxy-5'-adénosine s'est dissocié de manière réversible pour donner le radical désoxyadénosyle . Le ligand -axial 5,6-diméthylbenzimidazole (DMB) est impliqué dans l'organisation du site actif pour permettre à l' histidine -610 de se lier au Co, au lieu du DMB (la raison de la notation 'DMB-off'/'His-on' ). La liaison du résidu histidine-610 augmente le taux de rupture de la liaison homolytique ligand -axial - Co d'un facteur 10 12 .

D'autres résidus importants de la méthylmalonyl-CoA mutase comprennent l'histidine-244, qui agit comme un acide général près du substrat et protège les espèces radicalaires des réactions secondaires impliquant l'oxygène, le glutamate -370, dont la liaison hydrogène avec le groupe 2'-OH du ribose du ligand -axial force l'interaction entre l'espèce radicalaire du ligand -axial et le substrat, et la tyrosine -89 qui stabilise les intermédiaires radicaux réactifs et explique la stéréosélectivité de l'enzyme.
La protéine de transformation, la protéine MMAA , remplit le rôle important d'aide au chargement et à l'échange de cofacteur. La protéine MMAA favorise l'association avec l' apoenzyme MCM et permet le transfert du cofacteur AdoCbl vers le site actif de l'enzyme. De plus, si l'AdoCbl lié accumule des dommages oxydatifs au cours du fonctionnement normal, la protéine MMAA favorise l'échange du cofacteur endommagé contre un nouvel AdoCbl via une voie dépendante du GTP .
Interactions
Les références
Lectures complémentaires
- Ledley FD, Rosenblatt DS (1997). « Mutations dans l'acidémie mut méthylmalonique : corrélations cliniques et enzymatiques ». Mutation humaine . 9 (1) : 1–6. doi : 10.1002/(SICI)1098-1004(1997)9:1<1::AID-HUMU1>3.0.CO;2-E . PMID 8999901 .
- Ludwig ML, Matthews RG (1997). « Perspectives basées sur la structure sur les enzymes dépendantes de B12 ». Revue annuelle de biochimie . 66 : 269-313. doi : 10.1146/annurev.biochem.66.1.269 . PMID 9242908 .
- Lubrano R, Elli M, Rossi M, Travasso E, Raggi C, Barsotti P, Carducci C, Berloco P (août 2007). « Transplantation rénale dans l'acidémie méthylmalonique : serait-elle la meilleure option ? Rapport d'un cas à 10 ans et revue de la littérature ». Néphrologie Pédiatrique . 22 (8) : 1209–14. doi : 10.1007/s00467-007-0460-z . PMID 17401587 . S2CID 24610554 .
- Frenkel EP, Kitchens RL (décembre 1975). « Localisation intracellulaire de la propionyl-CoA carboxylase hépatique et de la méthylmalonyl-CoA mutase chez l'homme et les rats normaux et déficients en vitamine B12 ». Journal britannique d'hématologie . 31 (4) : 501–13. doi : 10.1111/j.1365-2141.1975.tb00885.x . PMID 24458 . S2CID 1232083 .
- Crane AM, Jansen R, Andrews ER, Ledley FD (février 1992). "Clonage et expression d'une méthylmalonyl coenzyme A mutase avec une affinité altérée pour la cobalamine qui provoque une acidurie mut-méthylmalonique" . Le Journal d'Investigation Clinique . 89 (2) : 385-91. doi : 10.1172/JCI115597 . PMC 442864 . PMID 1346616 .
- Crane AM, Martin LS, Valle D, Ledley FD (mai 1992). « Phénotype de la maladie chez trois patients présentant des mutations identiques dans la méthylmalonyl CoA mutase ». Génétique humaine . 89 (3) : 259–64. doi : 10.1007/BF00220536 . PMID 1351030 . S2CID 5624280 .
- Raff ML, Crane AM, Jansen R, Ledley FD, Rosenblatt DS (janvier 1991). "Caractérisation génétique d'une mutation du locus MUT discriminant l'hétérogénéité dans l'acidurie mut0 et mut-méthylmalonique par complémentation interallélique" . Le Journal d'Investigation Clinique . 87 (1) : 203-7. doi : 10.1172/JCI114972 . PMC 295026 . PMID 1670635 .
- Jansen R, Ledley FD (novembre 1990). « Mutations hétérozygotes au locus mut dans les fibroblastes avec acidémie méthylmalonique mut0 identifiées par clonage d'ADNc par réaction en chaîne par polymérase » . Journal américain de génétique humaine . 47 (5) : 808-14. PMC 1683687 . PMID 1977311 .
- Nham SU, Wilkemeyer MF, Ledley FD (décembre 1990). « Structure du locus humain méthylmalonyl-CoA mutase (MUT) ». Génomique . 8 (4) : 710-6. doi : 10.1016/0888-7543(90)90259-W . PMID 1980486 .
- Ledley FD, Lumetta M, Nguyen PN, Kolhouse JF, Allen RH (mai 1988). « Clonage moléculaire de la L-méthylmalonyl-CoA mutase : transfert de gènes et analyse de lignées cellulaires mutées » . Actes de l'Académie nationale des sciences des États-Unis d'Amérique . 85 (10) : 3518-21. Bibcode : 1988PNAS ... 85.3518L . doi : 10.1073/pnas.85.10.3518 . PMC 280243 . PMID 2453061 .
- Jansen R, Kalousek F, Fenton WA, Rosenberg LE, Ledley FD (février 1989). « Clonage de méthylmalonyl-CoA mutase pleine longueur à partir d'une bibliothèque d'ADNc en utilisant la réaction en chaîne par polymérase ». Génomique . 4 (2) : 198-205. doi : 10.1016/0888-7543 (89) 90300-5 . PMID 2567699 .
- Fenton WA, Hack AM, Kraus JP, Rosenberg LE (mars 1987). « Études immunochimiques de fibroblastes de patients atteints d'un déficit en apoenzyme méthylmalonyl-CoA mutase : détection d'une mutation interférant avec l'importation mitochondriale » . Actes de l'Académie nationale des sciences des États-Unis d'Amérique . 84 (5) : 1421–4. Bibcode : 1987PNAS ... 84.1421F . doi : 10.1073/pnas.84.5.1421 . PMC 304442 . PMID 2881300 .
- Zoghbi HY, O'Brien WE, Ledley FD (novembre 1988). « Relations de liaison de la mutase humaine méthylmalonyl CoA aux loci HLA et D6S4 sur le chromosome 6 ». Génomique . 3 (4) : 396-8. doi : 10.1016/0888-7543(88)90135-8 . PMID 2907507 .
- Kolhouse JF, Utley C, Allen RH (avril 1980). "Isolement et caractérisation de la méthylmalonyl-CoA mutase du placenta humain" . Le Journal de Chimie Biologique . 255 (7) : 2708-12. doi : 10.1016/S0021-9258 (19) 85795-2 . PMID 6102092 .
- Fenton WA, Hack AM, Willard HF, Gertler A, Rosenberg LE (avril 1982). « Purification et propriétés de la méthylmalonyl coenzyme A mutase du foie humain ». Archives de biochimie et biophysique . 214 (2) : 815–23. doi : 10.1016/0003-9861(82)90088-1 . PMID 6124211 .
- Qureshi AA, Crane AM, Matiaszuk NV, Rezvani I, Ledley FD, Rosenblatt DS (avril 1994). "Clonage et expression de mutations démontrant une complémentation intragénique dans l'acidurie méthylmalonique mut0" . Le Journal d'Investigation Clinique . 93 (4) : 1812–9. doi : 10.1172/JCI117166 . PMC 294249 . PMID 7909321 .
- Crane AM, Ledley FD (juillet 1994). "Groupement de mutations dans la méthylmalonyl CoA mutase associée à l'acidémie mut-méthylmalonique" . Journal américain de génétique humaine . 55 (1) : 42-50. PMC 1918235 . PMID 7912889 .
- Janata J, Kogekar N, Fenton WA (septembre 1997). « Expression et caractérisation cinétique de la méthylmalonyl-CoA mutase chez les patients présentant le phénotype mut : preuves d'une complémentation interallélique naturelle » . Génétique Moléculaire Humaine . 6 (9) : 1457-1464. doi : 10.1093/hmg/6.9.1457 . PMID 9285782 .
Liens externes
- Entrée GeneReviews/NIH/NCBI/UW sur l'acidémie méthylmalonique
- Méthylmalonyl-CoA+Mutase à la National Library of Medicine Medical Subject Headings (MeSH) des États-Unis