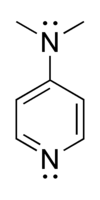
4-Diméthylaminopyridine - 4-Dimethylaminopyridine
|
|
|||
| Noms | |||
|---|---|---|---|
|
Noms IUPAC
N , N -diméthylpyridin-4-amine
Diméthyl (pyridin-4-yl) azane Diméthyl (pyridin-4-yl) amine |
|||
|
Nom IUPAC préféré
N , N -diméthylpyridin-4-amine |
|||
| Autres noms
4- (diméthylamino) pyridine
N , N -diméthyl-4-aminopyridine DMAP 4-diméthylaminopyridine 4- (diméthylamino) azine N , N -diméthyl-4-aminoazine 4- (diméthylamino) azabenzène N , N -diméthyl-4-aminoazabenzène |
|||
| Identifiants | |||
|
Modèle 3D ( JSmol )
|
|||
| ChemSpider | |||
| Carte Info ECHA |
100.013.049 |
||
|
PubChem CID
|
|||
| UNII | |||
|
Tableau de bord CompTox ( EPA )
|
|||
|
|||
|
|||
| Propriétés | |||
| C 7 H 10 N 2 | |||
| Masse molaire | 122,17 g / mol | ||
| Apparence | solide blanc | ||
| Point de fusion | 110 à 113 ° C (230 à 235 ° F; 383 à 386 K) | ||
| Point d'ébullition | 162 ° C (324 ° F; 435 K) à 50 mmHg | ||
| Acidité (p K a ) | 9,6 dans l'eau, 17,95 (p K a d'acide conjugué dans l'acétonitrile) | ||
| Dangers | |||
| Fiche de données de sécurité | |||
| Pictogrammes SGH |

|
||
| Mot de signalisation SGH | Danger | ||
| H301 , H310 , H315 , H319 , H335 | |||
| P280 , P305 + 351 + 338 , P337 + 313 | |||
| Dose ou concentration létale (DL, LC): | |||
|
DL 50 ( dose médiane )
|
souris cerf: par voie orale, 450 mg / kg souris: orale, 350 mg / kg / jour |
||
|
Sauf indication contraire, les données sont données pour les matériaux dans leur état standard (à 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Références Infobox | |||
La 4-diméthylaminopyridine ( DMAP ) est un dérivé de la pyridine de formule chimique (CH 3 ) 2 NC 5 H 4 N.Ce solide incolore est intéressant car il est plus basique que la pyridine , du fait de la stabilisation de la résonance du substituant NMe 2 .
En raison de sa basicité, le DMAP est un catalyseur nucléophile utile pour une variété de réactions telles que les estérifications avec des anhydrides , la réaction de Baylis-Hillman , les hydrosilylations , la tritylation, le réarrangement de Steglich, la synthèse de Staudinger des β-lactames et bien d'autres. Les analogues chiraux de DMAP sont utilisés dans des expériences de résolution cinétique principalement d'alcools secondaires et d'amides de type auxiliaire Evans.
Préparation
Le DMAP peut être préparé selon une procédure en deux étapes à partir de la pyridine, qui est d'abord oxydée en cation 4-pyridylpyridinium. Ce cation réagit alors avec la diméthylamine :
Catalyseur d'estérification
Dans le cas de l' estérification avec des anhydrides acétiques, le mécanisme actuellement accepté comporte trois étapes. Premièrement, le DMAP et l'anhydride acétique réagissent dans une réaction de pré-équilibre pour former une paire d'ions d' acétate et de l'ion acétylpyridinium. Dans la seconde étape, l' alcool s'ajoute à l'acétylpyridinium et l'élimination de la pyridine forme un ester . Ici, l'acétate agit comme une base pour éliminer le proton de l'alcool lorsqu'il ajoute nucléophile à l'acylpyridinium activé. La liaison du groupe acétyle au catalyseur est clivée pour générer le catalyseur et l'ester. Le processus de formation et de rupture de liaison décrit se déroule de manière synchrone et concertée sans l'apparition d'un intermédiaire tétraédrique. L' acide acétique formé protonera alors le DMAP. Dans la dernière étape du cycle catalytique, la base auxiliaire (habituellement la triéthylamine ou la pyridine ) déprotone le DMAP protoné, reformant le catalyseur. La réaction passe par la voie de réaction nucléophile décrite quel que soit l'anhydride utilisé, mais le mécanisme change avec la valeur pKa de l'alcool utilisé. Par exemple, la réaction passe par une voie de réaction catalysée par une base dans le cas d'un phénol. Dans ce cas, le DMAP agit comme une base et déprotone le phénol, et l'ion phénolate résultant s'ajoute à l'anhydride.
Sécurité
Le DMAP a une toxicité relativement élevée et est particulièrement dangereux en raison de sa capacité à être absorbé par la peau. Il est également corrosif.
Composé associé
Les références
- ^ Kaljurand, I .; Kütt, A .; Sooväli, L .; Rodima, T .; Mäemets, V .; Leito, I .; Koppel, IA (2005). "Extension de l'échelle de basicité spectrophotométrique auto-cohérente dans l'acétonitrile à une échelle complète de 28 unités pKa: unification des différentes échelles de basicité". J. Org. Chem . 70 (3): 1019-1028. doi : 10.1021 / jo048252w . PMID 15675863 .
- ^ A b c Sigma-Aldrich Co. , 4- (diméthylamino) pyridine . Récupéré le 03/09/2015.
- ^ A b c d Nachtergael, Amandine; Coulembier, Olivier; Dubois, Philippe; Helvenstein, Maxime; Duez, Pierre; Blankert, Bertrand; Mespouille, Laetitia (9 février 2015). "Paradigme d'organocatalyse revisité: les catalyseurs sans métal sont-ils vraiment inoffensifs?". Biomacromolécules . 16 (2): 507-514. doi : 10.1021 / bm5015443 . PMID 25490408 .
- ^ Donald J Berry; Charles V Digiovanna; Stephanie S Metrick; Ramiah Murugan (2001). "Catalyse par 4-dialkylaminopyridines" . Arkivoc : 201-226. Archivé de l'original le 2007-09-27 . Récupéré le 27/11/2006 .
- ^ Höfle, G .; Steglich, W .; Vorbrüggen, H. (1978). "Les 4-dialkylaminopyridines en tant que catalyseurs d'acylation hautement actifs". Angew. Chem. Int. Ed. Engl. 17 (8): 569-583. doi : 10.1002 / anie.197805691 .
- ^ Ryan P. Wurz (2007). "Catalyseurs de Dialkylamine Chiraux dans la Synthèse Asymétrique". Chem. Rev. 107 (12): 5570–5595. doi : 10.1021 / cr068370e . PMID 18072804 .
- ^ Shimizu, Shinkichi; Watanabe, Nanao; Kataoka, Toshiaki; Shoji, Takayuki; Abe, Nobuyuki; Morishita, Sinji; Ichimura, Hisao (2007). "Pyridine et dérivés de pyridine". Encyclopédie Ullmann de chimie industrielle . Weinheim: Wiley-VCH. doi : 10.1002 / 14356007.a22_399 .
- ^ S. Xu; J'ai tenu; B. Kempf; H. Mayr; Wolfgang Steglich ; H. Zipse (2005). "L'acétylation catalysée par DMAP des alcools - une étude mécanistique (DMAP = 4- (diméthylamino) -pyridine)". Chem. EUR. J. 11 (16): 4751–4757. doi : 10.1002 / chem.200500398 . PMID 15924289 .
- ^ DMAP MSDS - Fischer Science
Lectures complémentaires
- B. Neises; W. Steglich (1990). "Estérification des acides carboxyliques avec le dicyclohexylcarbodiimide / 4-diméthylaminopyridine: tert-butyl éthyl fumarate" . Synthèses organiques . ; Volume collectif , 7 , p. 93
- J'ai tenu; P. von den Hoff; DS Stephenson; H. Zipse (2008). "Catalyse Domino dans la Conversion Directe des Acides Carboxyliques en Esters". Adv. Synth. Catal. 11/12 (11-12): 1891-1900. doi : 10.1002 / adsc.200800268 .