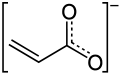
Acrylate - Acrylate
Les acrylates ( IUPAC : prop-2-enoates ) sont les sels , les esters et les bases conjuguées de l' acide acrylique . L' ion acrylate est l'anion C H 2 =CHC OO − . Souvent, l'acrylate fait référence aux esters d'acide acrylique, le membre le plus courant étant l'acrylate de méthyle . Ces acrylates contiennent des groupes vinyle . Ces composés sont intéressants car ils sont bifonctionnels : le groupe vinyle est susceptible de polymérisation et le groupe carboxylate porte une myriade de fonctionnalités. Les acrylates modifiés sont également nombreux, quelques exemples étant les méthacrylates (CH 2 =C(CH 3 )CO 2 R) et les cyanoacrylates (CH 2 =C(CN)CO 2 R). Acrylate peut également se référer à des polyacrylates préparés par polymérisation des groupes vinyle de monomères acrylate.
- Structures de certains acrylates et dérivés
Triméthylolpropane triacrylate (TMPTA), un ester acrylate trifonctionnel
L'acrylate de méthyle , un ester acrylique
Cyanoacrylate d'éthyle , précurseur de la "super colle"
Le tétraacrylate de pentaérythritol (PETA), un acrylate tétrafonctionnel
Utilisation
Les acrylates et les méthacrylates (les sels et les esters de l'acide méthacrylique ) sont des monomères courants dans les plastiques polymères , formant les polymères acrylates . Les acrylates forment facilement des polymères. Divers monomères à fonction acrylate sont connus.
Monomères
Les monomères d' acrylate , utilisés pour former des polymères d'acrylate, sont basés sur la structure de l'acide acrylique , qui est constitué d'un groupe vinyle et d'une extrémité ester d' acide carboxylique ou d'un nitrile. D'autres monomères d'acrylate typiques sont des dérivés d'acide acrylique, tels que le méthacrylate de méthyle dans lequel un hydrogène vinylique et l'hydrogène d'acide carboxylique sont tous deux remplacés par des groupes méthyle , et l' acrylonitrile dans lequel le groupe acide carboxylique est remplacé par le groupe nitrile associé .
D'autres exemples de monomères acrylates sont :
- Méthacrylates
- Acrylate de méthyle
- Acrylate d'éthyle
- 2-chloroéthyl vinyl éther
- Acrylate de 2-éthylhexyle
- Méthacrylate d'hydroxyéthyle
- Acrylate de butyle
- Méthacrylate de butyle
- TMPTA
Production
Les acrylates sont préparés industriellement en traitant l'acide acrylique avec l'alcool correspondant en présence d'un catalyseur. La réaction avec les alcools inférieurs ( méthanol , éthanol ) a lieu à 100–120 °C avec des catalyseurs hétérogènes acides ( échangeur de cations ). La réaction des alcools supérieurs ( n -butanol , 2-éthylhexanol ) est catalysée avec de l'acide sulfurique en phase homogène. Des acrylates d'alcools encore supérieurs peuvent être obtenus par transestérification d'esters inférieurs catalysés par des alcoolates de titane ou des composés organiques de l'étain (par exemple le dilaurate de dibutylétain ).
Voir également
- Polymère acrylique
- Polyacrylate de sodium épaississeurs
- Méthacrylate