Sulfate de cadmium - Cadmium sulfate
|
|
| Des noms | |
|---|---|
|
Nom IUPAC
Sulfate de cadmium (II)
|
|
| Autres noms
Acide sulfurique, sel de cadmium (1: 1),
|
|
| Identifiants | |
|
Modèle 3D ( JSmol )
|
|
| ChEBI | |
| ChemSpider | |
| Carte Info ECHA | 100.030.288 |
| Numéro CE | |
| 8295 | |
|
PubChem CID
|
|
| Numéro RTECS | |
| UNII | |
| Numéro UN | 2570 |
|
Tableau de bord CompTox ( EPA )
|
|
|
|
|
|
| Propriétés | |
| CdSO 4 CdSO 4 · H 2 O (monohydraté) 3CdSO 4 · 8H 2 O (octahydraté) |
|
| Masse molaire | 208,47 g / mol (anhydre) 226,490 g / mol (monohydraté) 769,546 g / mol (octahydraté) |
| Apparence | Blanc hygroscopique solide |
| Odeur | inodore |
| Densité | 4,691 g / cm 3 (anhydre) 3,79 g / cm 3 (monohydraté) 3,08 g / cm 3 (octahydraté) |
| Point de fusion | 1000 ° C (1830 ° F; 1270 K) (anhydre) 105 ° C (monohydraté) 40 ° C (octahydraté) |
| Point d'ébullition | (se décompose en sulfate basique puis en oxyde) |
|
anhydre: 75 g / 100 ml (0 ° C) 76,4 g / 100 ml (25 ° C) 58,4 g / 100 ml (99 ° C) monohydraté: 76,7 g / 100 ml (25 ° C) octahydraté: très soluble |
|
| Solubilité | légèrement soluble dans le méthanol , acétate d'éthyle insoluble dans l' éthanol |
| -59,2 · 10 -6 cm 3 / mol | |
|
Indice de réfraction ( n D )
|
1,565 |
| Structure | |
monoclinique orthorhombique (anhydre) (hepta et octahydraté) |
|
| Thermochimie | |
|
Entropie molaire std ( S |
123 J · mol −1 · K −1 |
| −935 kJ · mol −1 | |
| Dangers | |
| Fiche de données de sécurité | [1] |
| Pictogrammes SGH |
  
|
| Mot de signalisation SGH | Danger |
| H301 , H330 , H340 , H350 , H360 , H372 , H400 , H410 | |
| P201 , P202 , P260 , P264 , P270 , P271 , P273 , P281 , P284 , P301 + 310 , P304 + 340 , P308 + 313 , P310 , P314 , P320 , P321 , P330 , P391 , P403 + 233 , P405 , P501 | |
| NFPA 704 (diamant de feu) | |
| Dose ou concentration létale (DL, LC): | |
|
DL 50 ( dose médiane )
|
280 mg / kg (oral, rat) |
| NIOSH (limites d'exposition pour la santé aux États-Unis): | |
|
PEL (autorisé)
|
[1910.1027] TWA 0,005 mg / m 3 (en Cd) |
|
REL (recommandé)
|
Californie |
|
IDLH (danger immédiat)
|
Ca [9 mg / m 3 (en Cd)] |
| Composés apparentés | |
|
Autres anions
|
L' acétate de cadmium , chlorure de cadmium , le nitrate de cadmium |
|
Autres cations
|
Sulfate de zinc , sulfate de calcium , sulfate de magnésium |
|
Sauf indication contraire, les données sont données pour les matériaux dans leur état standard (à 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Références Infobox | |
Le sulfate de cadmium est le nom d'une série de apparentées des composés inorganiques à la formule CdSO 4 · x H 2 O. La forme la plus commune est le monohydrate CdSO 4 · H 2 O, mais deux autres formes sont connues CdSO 4 · 8 / 3 H 2 O et le sel anhydre (CdSO 4 ). Tous les sels sont incolores et hautement solubles dans l'eau.
Structure, préparation et occurrence
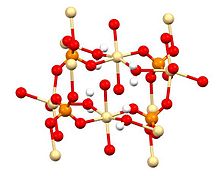
La cristallographie aux rayons X montre que le CdSO 4 · H 2 O est un polymère de coordination typique. Chaque centre Cd 2+ a une géométrie de coordination octaédrique , étant entouré de quatre centres d'oxygène fournis par quatre ligands sulfate et deux centres d'oxygène provenant des ligands d' eau de pontage .
Le sulfate de cadmium octohydraté peut être préparé par réaction du cadmium métallique ou de son oxyde ou hydroxyde avec de l'acide sulfurique dilué:
- CdO + H 2 SO 4 → CdSO 4 + H 2 O
- Cd + H 2 SO 4 → CdSO 4 + H 2
La matière anhydre est préparée à l' aide de persulfate de sodium :
- Cd + Na 2 S 2 O 8 → CdSO 4 + Na 2 SO 4
Le sulfate de cadmium pur se présente sous forme de minéraux très rares: drobécite (CdSO 4 · 4H 2 O), voudourisite (monohydrate) et lazaridisite (le 8/3-hydrate).
Applications
Le sulfate de cadmium est largement utilisé pour la galvanoplastie du cadmium dans les circuits électroniques. C'est également un précurseur de pigment à base de cadmium tel que le sulfure de cadmium . Il est également utilisé pour l' électrolyte dans une cellule standard Weston ainsi que comme pigment dans les écrans fluorescents.
Les références
- ^ Lide, David R., éd. (2006). CRC Handbook of Chemistry and Physics (87e éd.). Boca Raton, Floride: CRC Press . ISBN 0-8493-0487-3.
- ^ un b Zumdahl, Steven S. (2009). Principes chimiques 6e éd . Compagnie Houghton Mifflin. p. A21. ISBN 978-0-618-94690-7.
- ^ A b c NIOSH Pocket Guide de dangers des produits chimiques. "# 0087" . Institut national pour la sécurité et la santé au travail (NIOSH).
- ^ Theppitak, C /; Chainok, K. "Structure cristalline de CdSO 4 (H 2 O): une redétermination" Acta Crystallographica, Section E. Rapports de structure en ligne 2015, volume 71, pi8-pi9. doi : 10.1107 / S2056989015016904

