Cyanation - Cyanation
En synthèse organique , la cyanation est la fixation ou la substitution d'un groupe cyanure sur divers substrats . Ces transformations sont de grande valeur car elles génèrent une liaison CC. En outre, les nitriles sont des groupes fonctionnels polyvalents.
Cyanation pour former des nitriles sp 3
Typiquement, les alkyl nitriles sont formés par cyanation de type S N 1 ou S N 2 avec des alkyl électrophiles. La synthèse du cyanure de benzyle par réaction du chlorure de benzyle et du cyanure de sodium est illustrative . Dans certains cas, le cyanure cuivreux est utilisé à la place du cyanure de sodium.
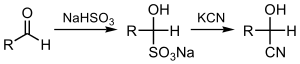
La cyanation des cétones ou des aldéhydes donne les cyanohydrines correspondantes , ce qui peut être fait directement avec l'ion cyanure (la réaction cyanhydrine ) ou en utilisant du bisulfate, suivi d'un déplacement du sulfite:
Une réaction connexe est l' hydrocyanation , qui installe les éléments de H-CN.
Cyanation des arènes
La cyanation des arènes offre un accès aux dérivés d' acide benzoïque , ainsi que l'utilité des aryl nitriles eux-mêmes en tant que produits chimiques fins:
Une variété de voies mécanistiquement distinctes sont connues pour cyanater les arènes:
Avec l'arène comme électrophile à deux électrons
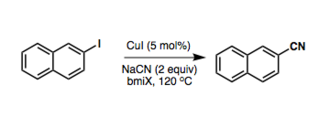
Alors que la réaction classique de Rosenmund Von-Braun utilise le cyanure de cuivre (I) stoechiométrique comme source de cyanation, de nouvelles variantes ont été développées qui sont catalytiques dans le cuivre :
En outre, les cyanations d' halogénures d'aryle catalysées au palladium ont été largement explorées. En général, KCN ou son substitut moins toxique Zn (CN) 2 sont utilisés comme sources de cyanure nucléophile . Pour réduire davantage les problèmes de toxicité , le ferricyanure de potassium a également été utilisé comme source de cyanure. On pense que les cycles catalytiques se déroulent selon une voie Pd (0 / II) standard avec élimination réductrice forgeant la liaison CC clé. La désactivation du Pd (II) avec un excès de cyanure est un problème courant. Les conditions de catalyse du palladium pour les iodures, bromures et même chlorures d'aryle ont été développées:
Les cyanations catalysées par le nickel évitent l'utilisation de métaux précieux et peuvent tirer parti du cyanure de benzyle ou de l' acétonitrile comme source de cyanure, via le clivage réducteur de la liaison CC:
La cyanation Sandmeyer est un moyen de convertir les dérivés d' aniline en benzonitriles. La cyanation est généralement postulée comme étant à deux électrons, tandis qu'avec des médiateurs radicaux en l'absence de métaux, la réaction est probablement radicale.
Avec l'arène comme nucléophile à deux électrons
Les arènes métallisés peuvent être cyanés avec des sources de cyanure électrophile , y compris des cyanamides , des cyanates , du diméthylmalononitrile ou du cyanoacétate d'éthyle (éthoxyméthylène). Ces méthodes peuvent se dérouler avec ou sans médiation par les métaux de transition:
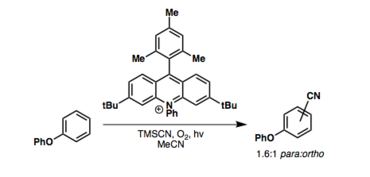
Avec l'arène comme électrophile radical
Des approches radicales de la cyanation de l'arène CH sont connues. Les médiateurs photoredox (métalliques ou organiques) sont les plus courants: