Cyclospora cayetanensis - Cyclospora cayetanensis
| Cyclospora cayetanensis | |
|---|---|

|
|
| Cyclospora cayetanensis oocystes | |
| Classification scientifique | |
| Domaine: | |
| (non classé): | |
| (non classé): | |
| Phylum: | |
| Classer: | |
| Sous-classe: | |
| Commander: | |
| Sous-ordre: | |
| Famille: | |
| Genre: | |
| Espèce: |
C. cayetanensis
|
| Nom binomial | |
|
Cyclospora cayetanensis Ortega, Gilman et Sterling, 1994
|
|
Cyclospora cayetanensis est un parasite coccidien qui provoque une maladie diarrhéique appelée cyclosporose chez l'homme et peut-être chez d'autres primates. Initialement signalé comme un nouveau pathogène de nature coccidienne probable dans les années 1980 et décrit au début des années 1990, il était pratiquement inconnu dans les pays développés jusqu'à ce que la sensibilisation augmente en raison de plusieurs éclosions liées à des produits importés contaminés par les matières fécales . C. cayetanensis est depuis devenu une cause endémique de maladies diarrhéiques dans les pays tropicaux et une cause de diarrhée du voyageur et d'infections d'origine alimentaire dans les pays développés. Cette espèce a été placée dans le genre Cyclospora en raison de la forme sphérique de ses sporocystes. Le nom spécifique fait référence à l' Université Cayetano Heredia à Lima, au Pérou, où les premiers travaux épidémiologiques et taxonomiques ont été effectués.
Histoire
Le premier rapport publié de Cyclospora cayetanensis chez l' homme semble être par Ashford (1979), qui a trouvé non identifié Isospora de la coccidies dans les matières fécales de trois personnes en Papouasie, Nouvelle - Guinée. Les microphotographies dans l'article révèlent un organisme morphologiquement identique à celui que l'on voit actuellement. Plus tard, Narango et al. (1989) ont rapporté ce qui pourrait être le même organisme chez plusieurs Péruviens souffrant de diarrhée chronique et ont appelé l'organisme semblable à Cryptosporidium muris . D'autres chercheurs pensaient que les oocystes non sporulés semblaient plus similaires aux cyanobactéries , et le nom «corps semblable à une cyanobactérie » ou CLB est devenu répandu dans la littérature (parfois, les auteurs ont également utilisé le terme «corps semblable à un coccidien», ou CLB). Finalement, Ortega et al. (1992) ont publié un résumé rapportant qu'ils avaient sporulé et excysté les oocystes, entraînant le placement du parasite dans le genre Cyclospora . Ils ont également créé le nom Cyclospora cayetanensis à cette époque. Cependant, comme aucune information morphologique n'a été présentée dans le résumé, C. cayetanensis est techniquement devenu un nomen nudum (une espèce nommée sans description). Bien qu'Ortega et al. (1993) ont publié plus tard des détails supplémentaires sur ce coccidien, une description morphologique complète n'a été publiée pour valider le nom qu'en 1994. Ainsi, le nom correct de ce parasite est Cyclospora cayetanensis Ortega, Gilman, & Sterling, 1994, et l'étymologie du nomen triviale est dérivé de l'Université Cayetano Heredia de Lima, Pérou. Pendant cette période de deux ans où C. cayetanensis était un nomen nudum , quiconque souhaitait publier une description morphologique complète et changer de nom aurait été libre de le faire.
Caractérisation
Cyclospora cayetanensis est un protozoaire coccidien apicomplexe formant des kystes qui provoque une diarrhée autolimitante. En termes de morphologie, il possède des oocystes sphériques d'un diamètre compris entre 7,5 et 10 μm qui ont également une paroi de 50 nm d' épaisseur avec une couche extérieure en forme de fil qui a été appelée une ride par certains chercheurs. La formule de l'oocyste est O.2.2 car un oocyste contient deux sporocystes et chaque sporocyste contient deux sporozoïtes.
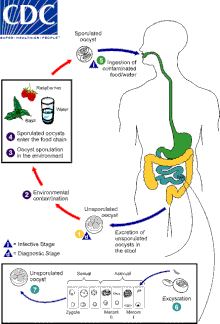
Les seuls hôtes confirmés pour C. cayetanensis sont les humains. Le protozoaire vit son cycle de vie de manière intracellulaire dans les cellules épithéliales et le tractus gastro-intestinal de l'hôte . L'infection est transmise par la voie fécale-orale et commence lorsqu'une personne ingère des oocystes dans des aliments ou de l'eau contaminés par les matières fécales. Divers produits chimiques dans le tractus gastro-intestinal de l'hôte provoquent l'excyste des oocystes et la libération de sporozoïtes ; généralement, deux sont observés par oocyste. Après que ces sporozoïtes ont envahi les cellules épithéliales, ils subissent la mérogonie , une forme de reproduction asexuée qui se traduit par de nombreuses filles mérozoïtes. Ces cellules filles peuvent soit infecter de nouvelles cellules hôtes et initier un autre cycle de mérogonie, soit adopter une voie sexuelle via la gamétogonie : les mérozoïtes filles deviennent des macrogamontes mâles - qui forment de nombreux microgamètes - et des macrogamontes femelles. Après la fécondation par fusion de microgamètes mâles avec un macrogamont femelle, le zygote mûrit en un oocyste et rompt la cellule hôte, à partir de laquelle il passe avec les selles . Les oocystes qui sont transmis ne sont cependant pas immédiatement infectieux. La sporulation peut prendre de une à plusieurs semaines, ce qui signifie que la transmission de personne à personne n'est pas un problème probable. Cela différencie C. cayetanensis de Cryptosporidium parvum - un organisme étroitement apparenté qui cause une maladie similaire - puisque les oocystes de C. parvum sont immédiatement infectieux lorsqu'ils sont libérés par l'hôte.
Symptômes
C. cayetanensis provoque une gastro - entérite , l'étendue de la maladie variant en fonction de l'âge, de l'état de l'hôte et de la taille de la dose infectieuse. Les symptômes comprennent "une diarrhée aqueuse, une perte d'appétit, une perte de poids, des ballonnements et des crampes abdominales, une augmentation des flatulences , des nausées , de la fatigue et une fièvre légère ", bien que cela puisse être augmenté dans les cas plus graves par des vomissements, une perte de poids substantielle, une diarrhée excessive et douleurs musculaires. En règle générale, les patients présentant une diarrhée aqueuse persistante pendant plusieurs jours peuvent être suspectés d'héberger la maladie, en particulier s'ils ont voyagé dans une région où le protozoaire est endémique. La période d'incubation chez l'hôte est généralement d'environ une semaine et la maladie peut durer six semaines avant de s'autolimiter. À moins d'être traitée, la maladie peut rechuter. Les formes les plus graves de la maladie peuvent survenir chez les patients immunodéprimés , tels que ceux atteints du SIDA . La cyclosporose humaine est cliniquement similaire à la cryptosporidiose , l' isosporose , la giardiase et la microsporidiose en raison des caractéristiques cliniques similaires. Un syndrome pseudo-grippal avec myalgies et arthralgies peut précéder l'apparition de la diarrhée. La fièvre est de bas grade et est inhabituelle. Une déshydratation modérée à sévère, une tachycardie compensatrice , une pression artérielle systolique (PAS <90 mmHg) et une diminution de la turgescence cutanée peuvent survenir. Mais une infection bénigne produit peu ou pas de symptômes cliniques. Le système immunitaire peut déterminer l'apparition des symptômes; c'est-à-dire que du stade symptomatique au stade asymptomatique dépend de la résistivité du système immunitaire.
Facteurs de risque
Les personnes vivant ou voyageant dans des zones tropicales ou subtropicales en développement peuvent courir un risque accru de contracter C. cayetanensis , car il est endémique dans ces zones. Les infections dans les régions endémiques ont tendance à montrer une saisonnalité marquée qui est mal comprise, alors que les flambées nord-américaines se produisent le plus souvent à la fin du printemps et en été, en corrélation avec l'augmentation des importations de produits des tropiques. Consommer de la nourriture ou de l'eau lors d'une visite dans les pays en développement est un moyen bien documenté de développer la diarrhée du voyageur. Les voyageurs sont souvent mis en garde contre de telles actions, mais plus de 70 pour cent de certains produits consommés aux États-Unis sont importés de pays en développement, ce qui rend la «diarrhée du voyageur» possible sans les voyages internationaux. Étant donné que les oocystes sont excrétés dans les excréments des personnes infectées et doivent ensuite mûrir dans l'environnement 2 à 14 jours avant de devenir contagieux, il est peu probable qu'une personne soit infectée directement par une autre personne, comme un manipulateur d'aliments infecté.
Reconnaissance
En raison de sa petite taille, de son habitat intracellulaire et de son incapacité à absorber correctement de nombreuses taches histologiques, le diagnostic de C. cayetanensis peut être très difficile. Jusqu'à présent, quatre méthodes ont été établies pour un diagnostic positif du protozoaire: la détection microscopique dans des échantillons de selles d'oocystes; récupération des oocystes dans les échantillons de biopsie du liquide intestinal / de l'intestin grêle; démonstration de la sporulation des oocystes; et amplification par réaction en chaîne par polymérase (PCR) de l' ADN de C. cayetanensis . Étant donné que la détection est si difficile, un résultat négatif ne devrait pas écarter la possibilité de C. cayetanensis : des tests impliquant des échantillons de selles fraîches au cours des prochains jours devraient également être envisagés.
À l'exception de l'amplification par PCR, une fois qu'un échantillon contenant des oocystes suspects a été récupéré, des tests standard sont suivis pour identifier C. cayetanensis . Ces tests comprennent la microscopie à contraste de phase pour vérifier les oocystes sphériques décrits précédemment, la coloration acido-résistante modifiée pour vérifier la coloration variable (du pâle au rouge) et l' autofluorescence avec des lumières UV . L'obtention de ces oocystes est généralement le défi, bien que des études récentes montrent des méthodes plus faciles pour les obtenir. Dans une étude récente sur différentes techniques utilisées dans les examens fécaux pour identifier les oocystes, la centrifugation d'un échantillon de matières fécales dans une solution de saccharose puis le transfert d'une petite quantité sur une lame s'est avérée remarquablement efficace - à la fois dans les oocystes trouvés et la facilité relative du travail - dans la détection des oocystes de C. cayetanensis : en effet, l'article a conclu que les échantillons positifs obtenus étaient d'environ 84%.
C. cayetanensis a été confondu avec d'autres infections à protozoaires dans le passé, le plus souvent étant confondu avec Cryptosporidium parvum . Cependant, plusieurs différences peuvent être notées entre les deux pour assurer un diagnostic correct. Ces différences comprennent: la différence de taille - C. parvum est plus petit; résultats différents de la coloration acido-résistante modifiée - C. parvum a une coloration rouge constante, tandis que C. cayetanensis présente une coloration variable; et l'autofluorescence sous lumière ultraviolette - C. cayetanensis le montre, contrairement à C. parvum .
Les cas d' infection à C. cayetanensis restent souvent inexpliqués, en partie à cause des difficultés associées aux investigations épidémiologiques de ces cas et du manque de méthodes de génotypage. Les tentatives récentes pour une meilleure caractérisation du génotypage comprennent le typage de séquences multilocus basé sur des marqueurs microsatellites et des polymorphismes nucléotidiques simples (SNP) de marqueurs nucléaires.
Traitement
La plupart des personnes qui ont un système immunitaire sain se rétablissent sans traitement. Si elle n'est pas traitée, la maladie peut durer de quelques jours à un mois ou plus. Les symptômes peuvent sembler disparaître puis revenir une ou plusieurs fois (rechute). Les médicaments antidiarrhéiques peuvent aider à réduire la diarrhée, mais consultez un fournisseur de soins de santé avant de prendre le médicament. Les personnes en mauvaise santé ou dont le système immunitaire est affaibli peuvent courir un risque plus élevé de maladie grave ou prolongée. À ce jour, le médicament le plus efficace pour le traitement du protozoaire est une cure de sept jours de triméthoprime-sulfaméthoxazole par voie orale (TMP-SMX). Les effets du médicament comprennent une diminution significative de la durée d'excrétion des oocystes, l'arrêt de la diarrhée et des échantillons de selles négatifs pour les oocystes dans les deux à trois jours. Le TMP-SMX est classé dans la catégorie C pendant la grossesse, ce qui signifie que des effets indésirables potentiels (tels que tératogène, embryocide ou autre) pourraient en résulter et ne devraient être administrés que si le bénéfice potentiel justifie de manière significative le risque. Le médicament doit être évité à court terme, car il existe des potentiels élevés d' hyperbilirubinémie et de kernictère chez les nouveau-nés. De plus, le TMP-SMX peut être excrété dans le lait maternel, ce qui est compatible chez les nouveau-nés en bonne santé à terme, mais doit être évité chez les nourrissons prématurés, malades, stressés ou ayant la jaunisse. Aucun traitement antibiotique hautement alternatif n'a encore été découvert pour les patients qui présentent une allergie aux sulfamides.
La prévention
Aucun vaccin contre ce pathogène n'est disponible. Étant donné que l'infection se produit via des aliments et de l'eau contaminés par les matières fécales dans des environnements endémiques, plusieurs solutions simples ont été suggérées pour la prévention des infections à C. cayetanensis . Le plus simple est d'avertir les voyageurs de ne pas visiter les régions où le protozoaire est endémique (en général, les régions tropicales et subtropicales où l'assainissement est médiocre, comme le Pérou, le Brésil et Haïti), en particulier lorsque la saison est la meilleure pour se propager: les voyageurs devraient également Sachez que le traitement de l'eau ou des aliments avec du chlore ou de l'iode est peu susceptible de tuer les oocystes de Cyclospora . De plus, de meilleures pratiques de santé dans le milieu agricole d'origine - comme s'assurer que les systèmes d'abreuvement des produits ne tirent pas l'eau qui a accès aux excréments humains. De plus, l'utilisation de systèmes de filtration tels qu'un système de filtration au carbone absolu de 1 micron réduira la présence de Cyclospora , diminuant considérablement l'incidence de la propagation de ce parasite. Les chances d'être infecté par Cyclospora et de nombreux autres agents pathogènes d'origine alimentaire peuvent être grandement diminués en lavant soigneusement les fruits et légumes dans de l'eau propre avant de les consommer. Cependant, le simple fait de laver les aliments n'élimine pas 100% des oocystes présents.
Cyclospora et framboises
Une étude réalisée sur des échantillons de selles de travailleurs agricoles de framboisiers a montré une incidence plus élevée d' oocystes de Cyclospora dans leurs spécimens par rapport à d'autres personnes de la région. Cela pourrait être dû au fait que Cyclospora spp. sont très résistants aux désinfectants couramment utilisés par les travailleurs à des fins d'hygiène et de transformation des aliments et de l'eau. Cette résistance est probablement renforcée par des affinités de liaison plus élevées avec certains produits frais. De fines projections ressemblant à des poils sur les framboises aident à faciliter le piégeage des oocystes collants à leurs surfaces par rapport à celles d'autres fruits, comme les mûres. Contraste entre la surface d'une framboise (à gauche) et une mûre (à droite), tel que vu par microscopie électronique à balayage: Notez la surface inégale de la framboise, avec des crevasses et des poils.
Épidémie de 2013 aux États-Unis
Au moins 285 personnes dans 11 États avaient été touchées au 26 juillet 2013. La cause exacte de l'épidémie n'avait pas encore été identifiée selon les Centers for Disease Control and Prevention (CDC) des États - Unis . La majorité des cas étaient localisés dans le Midwest , avec 138 cas signalés dans l' Iowa et 70 dans le Nebraska . Les autres États concernés sont: le Texas , la Floride , la Géorgie , le Wisconsin , le Connecticut , l' Illinois , le Kansas , le Minnesota , le New Jersey et l' Ohio .
Au 29 juillet 2013, le CDC a signalé que 373 personnes dans 15 États avaient été touchées par l'épidémie. Jusqu'à présent, 21 patients de trois États avaient été hospitalisés, sans aucun décès signalé. Aucune source de nourriture n'a été identifiée, mais les responsables de la santé de l'Iowa - l'État qui rapporte le plus de cas - ont déclaré qu'ils soupçonnaient des légumes importés.
Le 30 juillet 2013, le ministère de la Santé et des Services sociaux du Nebraska et le ministère de la Santé de l'Iowa ont annoncé que la salade emballée d'une chaîne de restaurants était le vecteur de la maladie du parasite. Cependant, le CDC et la Food and Drug Administration (FDA) des États-Unis évaluent toujours les informations provenant d'autres États pour voir si les résultats s'appliquent aux maladies là-bas.
Dans une mise à jour du 1er août 2013, le CDC a signalé 397 cas, tandis que l'Iowa et le Texas en ont ajouté 22 autres. Cela a poussé le décompte non officiel à plus de 400 cas. De plus, la Louisiane a signalé son premier cas, portant le nombre total d'États touchés à 16.
Le 3 août 2013, CNN a signalé que l'épidémie avait été attribuée à de la salade emballée servie dans les restaurants Olive Garden et Red Lobster, fabriquée par Taylor Farms de Mexico .
Le 15 août 2013, le CDC a signalé neuf autres infections à Cyclospora , portant son nombre de cas à 548. Le nombre d'États touchés est resté à 19, mais le CDC a déclaré que tous les cas n'étaient pas confirmés comme étant liés à une épidémie dans l'Iowa et le Nebraska. attribuable à un mélange de salade contaminé du Mexique.
Le 19 août 2013, le CDC a signalé 10 autres cas de Cyclospora , portant le décompte non officiel à plus de 600. Le Tennessee a également signalé son premier cas, portant le nombre d'États concernés à 20. Le CDC avertit toujours que si les cas dans tous les États sont liés à des épidémies dans l'Iowa et le Nebraska n'est pas clair.
Au 27 août 2013, l'origine de l'épidémie restait encore un mystère. La FDA a déclaré qu'elle n'avait trouvé aucune violation de la sécurité alimentaire dans l'usine de salade Taylor Farms de Mexico au Mexique qui était liée à certaines des maladies.
Épidémie du Texas en 2015
Dans une déclaration de la FDA, le CDC est cité, "il y a actuellement (en juillet 2015) une autre flambée de cyclosporose en cours aux États-Unis dans laquelle le Texas Department of State Health Services et le Wisconsin Department of Health Services et le Wisconsin Department of L'agriculture, le commerce et la protection des consommateurs ont identifié la coriandre de l'État mexicain de Puebla comme un véhicule suspect en ce qui concerne les différents groupes de maladies. " L'année dernière, le Texas a enregistré 200 cas, dont certains étaient associés à la coriandre de la région de Puebla.
Épidémie de 2016 au Texas
Les responsables de la santé ont déclaré que plus d'une douzaine de cas de cyclosporose avaient été confirmés dans les quatre principaux comtés du nord du Texas et que la source était probablement de la nourriture contaminée. Les services de santé du département d'État du Texas ont déclaré mercredi que le parasite avait été trouvé dans les comtés de Dallas, Tarrant, Collin et Denton et que l'origine pouvait être liée à un produit frais.
Les responsables du comté ont déclaré à NBC 5 que quatre cas avaient été enregistrés dans le comté de Dallas, trois dans le comté de Collin, quatre dans le comté de Denton et sept dans le comté de Tarrant. Les cas du comté de Denton et au moins quatre des cas du comté de Tarrant avaient récemment voyagé hors du pays, remettant en question le point d'origine.
Dans tout l'État, il y avait actuellement 66 cas confirmés de cyclosporose, bien que les sources d'infection n'aient pas été confirmées. Pour la plupart des gens, les symptômes n'étaient pas graves. «Mais pour ceux qui sont très jeunes et ceux qui sont plus âgés, ou ceux qui ont un système immunitaire affaibli, cette maladie peut causer des problèmes majeurs», a déclaré le Dr Khang Tran, médecin-chef du Centre médical de Plano. Au cours des dernières années, de 2012 à 2015, des éclosions de cyclospora ont été associées à de la coriandre fraîche importée de Puebla, au Mexique. Depuis l'été 2015, la Food and Drug Administration a institué une interdiction des importations en provenance de cette région entre avril et août.
Épidémie de légumes dans le Midwest Del Monte en 2018
Del Monte a rappelé les plateaux de légumes emballés Del Monte Fresh Produce, qui contenaient du brocoli, des carottes, du chou-fleur, des bâtonnets de céleri et une trempette à l'aneth, de certains détaillants, dont Kwik Trip et Peapod, selon le CDC. Des résidents de quatre États - l'Iowa, le Michigan, le Minnesota et le Wisconsin sont tombés malades de Cyclospora .
Épidémie de salade McDonald's du Midwest 2018
McDonald's a cessé de vendre des salades fournies par Fresh Express dans quelque 3000 emplacements à travers le pays, principalement dans le Midwest des États-Unis en raison d'une épidémie de parasites à plusieurs états qui avait rendu malade 551 personnes causée par Cyclospora .
Épidémie de salade de jardin en sac Midwestern Fresh Express 2020
En juin 2020, le CDC et d'autres organismes de réglementation ont commencé à enquêter sur une épidémie de cyclosporiose dans le Midwest des États-Unis liée à un mélange de salade en sac. Le 27 juin 2020, Fresh Express a annoncé un rappel volontaire de plus de 91 produits de salade Fresh Express et de marque privée.
| An | Nombre de cas | Taux d'incidence |
|---|---|---|
| 2015 | 316 | |
| 2014 * | 200 | 0,7 |
| 2013 * | 351 | 1,3 |
| 2012 * | 44 | 0,2 |
| 2011 * | 14 | 0,1 |
| 2010 | 9 | 0,0 |
| 2009 | dix | 0,0 |
| 2008 | 6 | 0,0 |
| 2007 | 2 | 0,0 |
| 2006 | 1 | 0,0 |
| 2005 | 1 | 0,0 |
| 2004 | 4 | 0,0 |
| 2003 | 1 | 0,0 |
| 2002 | 1 | 0,0 |
| 2001 | 0 | 0,0 |
IR = taux d'incidence pour 100 000
* les taux d'incidence sont basés sur les données de recensement projetées obtenues du DSHS Center for Health Statistics.
Éclosions de cyclosporose d'origine alimentaire aux États-Unis: 2000-2014
Des flambées de cyclosporiose d'origine alimentaire ont été signalées aux États-Unis depuis le milieu des années 1990 et ont été liées à divers types de produits frais importés, notamment les framboises, le basilic, les pois mange-tout, la laitue mesclun et la coriandre; aucun produit commercialement congelé n'a été impliqué à ce jour. Les éclosions de cyclosporose d'origine alimentaire aux États-Unis qui se sont produites avant 2000 ont été résumées précédemment, tout comme les principales éclosions documentées en 2013 et 2014 . Les éclosions d'origine alimentaire au cours de la période de 15 ans de 2000 à 2014 sont résumées dans le tableau. Le tableau fournit des informations sur 31 éclosions de cyclosporose d'origine alimentaire signalées aux États-Unis entre 2000 et 2014; le nombre total de cas était de 1 562. Aucune éclosion n'a été signalée en 2003, 2007 ou 2010. Dans l'ensemble, une médiane de deux éclosions a été signalée par an, avec une médiane de 20 cas par éclosion (intervalle de 3 à 582 cas). Bien que les éclosions se soient produites pendant 8 mois différents (de décembre à juillet), les mois de pointe ont été mai, juin et juillet. Comme indiqué dans le tableau, un vecteur alimentaire d'infection a été identifié pour 15 des 31 éclosions.
Résumé des flambées de cyclosporose d'origine alimentaire aux États-Unis, 2000-2014
| Années)* | Mois)* | Juridiction (s) * | Nombre de cas † | Véhicule alimentaire et source, si identifiés ‡ |
|---|---|---|---|---|
| 2000 | Peut | Géorgie | 19 | Framboises et / ou mûres (suspectées) |
| 2000 | juin | Pennsylvanie | 54 | Framboises |
| 2001 | Janvier février | Floride | 39 | |
| 2001 | janvier | La ville de New York | 3 | |
| 2001-02 | Décembre janvier | Vermont | 22 | Framboises (probablement) |
| 2002 | Avril Mai | Massachusetts | 8 | |
| 2002 | juin | New York | 14 | |
| 2004 | février | Texas | 38 | |
| 2004 | février | Illinois | 57 | Basilic (probablement) |
| 2004 | Peut | Tennessee | 12 | |
| 2004 | Mai juin | Pennsylvanie | 96 | Pois mange-tout du Guatemala |
| 2005 | Mars mai | Floride | 582 ¶ | Basilic du Pérou |
| 2005 | Peut | Caroline du Sud | 6 | |
| 2005 | avril | Massachusetts | 58 | |
| 2005 | Peut | Massachusetts | 16 | |
| 2005 | juin | Connecticut | 30 | Basil (suspecté) |
| 2006 | juin | Minnesota | 14 | |
| 2006 | juin | New York | 20 | |
| 2006 | juillet | Géorgie | 3 | |
| 2008 | mars | Wisconsin | 4 | Pois sucré (probablement) |
| 2008 | juillet | Californie | 45 ¶ | Framboises et / ou mûres (probablement) |
| 2009 | juin | District de Colombie | 34 | |
| 2011 | juin | Floride | 12 | |
| 2011 | juillet | Géorgie | 100 | |
| 2012 | Juin Juillet | Texas | 16 | |
| 2013 ** | juin | Iowa et Nebraska | 161 | Mélange à salade en sac du Mexique |
| 2013 ** | Juin Juillet | Texas | 38 | Coriandre du Mexique |
| 2013 | juillet | Wisconsin | 8 | Salade de petits fruits (suspectée) |
| 2014 | juin | Michigan | 14 | |
| 2014 †† | Juin Juillet | Texas | 26 | Coriandre du Mexique |
| 2014 | juillet | Caroline du Sud | 13 |
* Les entrées dans les trois premières colonnes font référence aux années, mois et juridictions connus ou probables au cours desquels l'exposition à Cyclospora a eu lieu.
** Pour plus de détails, voir les informations récapitulatives sur les enquêtes sur les flambées en 2013 . Aux fins de ce tableau, le ou les mois d'exposition et le nombre de cas sont limités à ceux explicitement liés dans les enquêtes à l'aliment spécifié dans la dernière colonne.
† Le nombre de cas comprend les cas probables et confirmés en laboratoire de cyclosporose. Par définition, chaque flambée comprenait au moins deux cas liés, dont au moins un avait été confirmé en laboratoire.
‡ Un véhicule alimentaire est spécifié uniquement si un seul ingrédient ou produit a été identifié dans une enquête sur une éclosion.
¶ Les cas survenus chez des voyageurs canadiens à destination des États-Unis n'ont pas été inclus.
†† Pour une perspective supplémentaire, voir les informations récapitulatives sur les enquêtes sur les éclosions en 2014 . Aux fins de ce tableau, les mois d'exposition et le nombre de cas pour l'épidémie au Texas sont limités à ceux explicitement liés dans les enquêtes à l'aliment spécifié dans la dernière colonne.
Les références
- Türk M, Türker M, Ak M, Karaayak B, Kaya T (mars 2004). "Cyclosporiasis associée à la diarrhée chez un patient immunocompétent en Turquie" . J. Med. Microbiol . 53 (Pt 3): 255–7. doi : 10.1099 / jmm.0.45531-0 . PMID 14970253 .
- Kimura K, Kumar Rai S, Takemasa K et coll. (Septembre 2004). "Comparaison de trois techniques microscopiques pour le diagnostic de Cyclospora cayetanensis ". FEMS Microbiol. Lett . 238 (1): 263–6. doi : 10.1016 / j.femsle.2004.07.045 . PMID 15336431 .
- Mansfield LS, Gajadhar AA (décembre 2004). " Cyclospora cayetanensis , un parasite coccidien d'origine alimentaire et hydrique". Vétérinaire. Parasitol . 126 (1–2): 73–90. doi : 10.1016 / j.vetpar.2004.09.011 . PMID 15567580 .
- Yu JR, Sohn WM (octobre 2003). "Un cas de cyclosporose humaine causant la diarrhée du voyageur après avoir visité l'Indonésie" . J. Korean Med. Sci . 18 (5): 738–41. doi : 10.3346 / jkms.2003.18.5.738 . PMC 3055112 . PMID 14555830 .