Maladie de Castleman multicentrique idiopathique - Idiopathic multicentric Castleman disease
| Maladie de Castleman multicentrique idiopathique | |
|---|---|
| Autres noms | Hyperplasie des ganglions lymphatiques géants, hamartome lymphoïde, hyperplasie des ganglions lymphatiques angiofolliculaires |
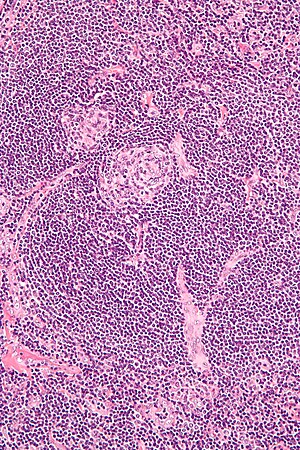 | |
| Micrographie de la biopsie des ganglions lymphatiques démontrant des caractéristiques vasculaires hyalines compatibles avec la maladie de Castleman | |
| Spécialité | Hématologie, immunologie, rhumatologie, pathologie |
| Méthode de diagnostic | Basé sur les antécédents du patient, l'examen physique, les tests de laboratoire, l'imagerie médicale, l'histopathologie |
| La fréquence | environ 1500-1800 nouveaux cas par an aux États-Unis |
La maladie de Castleman multicentrique idiopathique (iMCD) est un sous-type de maladie de Castleman (également connue sous le nom d' hyperplasie des ganglions lymphatiques géants , hamartome lymphoïde ou hyperplasie des ganglions lymphatiques angiofolliculaires ), un groupe de troubles lymphoprolifératifs caractérisés par une hypertrophie des ganglions lymphatiques , caractéristiques de l'analyse microscopique de l'hypertrophie des ganglions lymphatiques. tissu des ganglions lymphatiques et une gamme de symptômes et de résultats cliniques.
Les personnes atteintes d'iMCD ont des ganglions lymphatiques hypertrophiés dans plusieurs régions et présentent souvent des symptômes pseudo-grippaux, des résultats anormaux aux tests sanguins et un dysfonctionnement des organes vitaux, tels que le foie, les reins et la moelle osseuse.
L'iMCD a des caractéristiques souvent trouvées dans les maladies auto-immunes et les cancers, mais le mécanisme de la maladie sous-jacente est inconnu. Le traitement de l'iMCD peut impliquer l'utilisation de divers médicaments, y compris les immunosuppresseurs et la chimiothérapie.
La maladie de Castleman a été nommée d'après le Dr Benjamin Castleman , qui a décrit la maladie pour la première fois en 1956. Le Castleman Disease Collaborative Network est la plus grande organisation axée sur la maladie et est impliquée dans la recherche, la sensibilisation et le soutien aux patients.
Signes et symptômes
Les patients atteints d'iMCD peuvent présenter une hypertrophie des ganglions lymphatiques dans plusieurs régions ganglionnaires; symptômes systémiques (fièvre, sueurs nocturnes, perte de poids involontaire, fatigue); hypertrophie du foie et / ou de la rate ; accumulation de liquide extravasculaire dans les extrémités ( œdème ), l'abdomen ( ascite ) ou la muqueuse des poumons ( épanchement pleural ); symptômes pulmonaires tels que toux et essoufflement; et les découvertes cutanées telles que les hémangiomes de la cerise .
Les causes
La cause de l'iMCD n'est pas connue et aucun facteur de risque n'a été identifié. Des variantes génétiques ont été observées dans des cas de maladie de Castleman; cependant, aucune variante génétique n'a été validée comme causant une maladie.
Contrairement au MCD associé au HHV-8 , l'iMCD n'est pas causé par une infection incontrôlée au HHV-8.
Mécanisme
Le mécanisme de la maladie de l'iMCD n'a pas été entièrement décrit. On sait que l' interleukine-6 (IL-6) , une molécule qui stimule les cellules immunitaires, joue un rôle dans certains cas d'iMCD. Les taux d'IL-6 mesurés chez certains patients atteints d'iMCD augmentent et diminuent avec les changements correspondants de l'activité de la maladie, les souris traitées par l'IL-6 développent des caractéristiques d'iMCD et le blocage de la voie de l'IL-6 à l'aide des médicaments siltuximab et tocilizumab traite efficacement iMCD. Cependant, de nombreux patients atteints d'iMCD ne démontrent pas des niveaux élevés d'IL-6 et les niveaux d'IL-6 ne sont pas fortement corrélés avec la réponse au traitement avec des médicaments anti-IL-6. Dans les cas où l'IL-6 joue un rôle, la cause sous-jacente des niveaux élevés d'IL-6 et les cellules responsables de la production d'IL-6 restent inconnues.
Plusieurs mécanismes théoriques de l'iMCD ont été proposés sur la base des recherches existantes et des similitudes observées entre l'iMCD et d'autres maladies qui présentent des résultats cliniques et une histologie des ganglions lymphatiques similaires:
- Auto -immun - Le système immunitaire peut produire des anticorps qui ciblent les cellules saines du corps au lieu des bactéries et des virus. Les anticorps auto-dirigés sont couramment observés dans les maladies auto-immunes telles que le lupus érythémateux disséminé et la polyarthrite rhumatoïde .
- Auto-inflammatoire - Une mutation dans un gène contrôlant les systèmes inflammatoires peut contribuer à l'activation nocive des voies inflammatoires chez les patients atteints d'iMCD.
- Néoplasique - Les mutations génétiques qui se développent dans les cellules matures ( mutations somatiques ) peuvent provoquer une prolifération de cellules anormales comme dans les cancers tels que le lymphome .
- Agent pathogène - L'herpèsvirus humain 8 (HHV-8) est l'agent causal connu du MCD associé au HHV-8, qui présente des symptômes et des résultats très similaires à l'iMCD. Bien que l'iMCD, par définition, ne soit pas causé par le HHV-8, un virus inconnu peut provoquer la maladie.
Aucun cas de transformation de l'UCD en iMCD n'a été signalé.
Diagnostic
L'iMCD est diagnostiqué selon des critères de diagnostic consensuels fondés sur des preuves, qui nécessitent une évaluation approfondie comprenant les antécédents du patient , un examen physique , des tests de laboratoire , une imagerie radiologique et une analyse microscopique (histologie) du tissu biopsié d'un ganglion lymphatique hypertrophié. Le diagnostic de l'iMCD nécessite des anomalies cliniques, l'exclusion d'autres maladies et une biopsie des ganglions lymphatiques présentant des caractéristiques compatibles avec la maladie de Castleman. Une biopsie des ganglions lymphatiques à elle seule ne suffit pas pour poser le diagnostic.
Tests en laboratoire
Les tests de laboratoire peuvent démontrer une protéine C-réactive élevée , une diminution des taux d'hémoglobine ( anémie ), de faibles taux d' albumine , une créatinine élevée , une augmentation des taux d' immunoglobulines et une numération plaquettaire anormale (élevée ou diminuée) . Les patients peuvent également présenter des élévations des molécules impliquées dans l'inflammation ( cytokines ), telles que l' interleukine 6 (IL-6) et le facteur de croissance de l'endothélium vasculaire (VEGF) .
L'imagerie médicale
L'imagerie radiologique montrera des ganglions lymphatiques hypertrophiés dans plusieurs régions, qui sont généralement avides de 18F-fluorodoxyglucose (FDG) sur la tomographie par émission de positons (TEP) .
Maladies associées
L'iMCD est couramment observé chez les patients atteints du syndrome POEMS , mais on ne sait pas si l'iMCD se produit en tant que processus pathologique indépendant ou en tant que manifestation du syndrome POEMS chez ces patients. Les patients atteints d'iMCD ont un risque accru de tumeurs solides et de cancers du sang. Parfois, les patients atteints d'iMCD présentent une pneumopathie interstitielle lymphocytaire .
Syndrome TAFRO
Imcd patients avec t hrombocytopenia, un nasarca, myélo f ibrosis, r dysfonctionnement énal, et o syndrome rganomegaly (syndrome TAFRO) sont considérés comme ayant un sous - type clinique distincte de IMCD. Les patients présentent souvent une progression rapide des symptômes et développent fréquemment un dysfonctionnement grave des organes. Par rapport aux patients iMCD sans syndrome TAFRO, les patients iMCD atteints du syndrome TAFRO sont plus susceptibles de présenter des douleurs abdominales sévères, de faibles taux de plaquettes, un dysfonctionnement rénal progressif et des taux d'immunoglobulines normaux à légèrement élevés. Alors que l'iMCD avec syndrome TAFRO a été décrit pour la première fois chez des patients japonais en 2010, des cas d'iMCD avec syndrome TAFRO ont depuis été rapportés chez des patients non japonais dans de nombreux autres pays.
Classification
La maladie de Castleman décrit un groupe d'au moins 3 troubles distincts: la maladie de Castleman unicentrique (UCD), la maladie de Castleman multicentrique associée à l'herpèsvirus humain 8 (MCD associée au HHV-8) et la maladie de Castleman multicentrique idiopathique (iMCD) . Il est important d'identifier le sous-type correct de la maladie, car les trois troubles varient considérablement en termes de symptômes, de signes cliniques, de mécanisme de la maladie, d'approche thérapeutique et de pronostic.
- Dans la maladie de Castleman unicentrique, des ganglions lymphatiques hypertrophiés avec des signes microscopiques caractéristiques ne sont présents que dans une seule région ganglionnaire.
- Dans les sous-types multicentriques de la maladie de Castleman, des ganglions lymphatiques hypertrophiés avec des signes caractéristiques sont présents dans plusieurs régions de ganglions lymphatiques. Les variantes multicentriques de la maladie de Castleman sont en outre classées selon les causes connues de la maladie.
- La MCD associée au HHV-8 est causée par une infection incontrôlée par l'herpèsvirus humain 8 (HHV-8).
- Dans la maladie de Castleman multicentrique idiopathique (iMCD), la cause de la maladie est inconnue ( idiopathique ). Le test du HHV-8 doit être négatif pour diagnostiquer l'iMCD.
Maladie de Castleman multicentrique idiopathique
Imcd peut être en outre différenciés par la présence de maladies associées, telles que p olyneuropathy, o rganomegaly, e ndocrinopathy, m protéine onoclonal, s parent change syndrome (syndrome POEMS), ou par des caractéristiques cliniques distinctes, telles que t hrombocytopenia, un nasarca, myélo f ibrosis, r dysfonctionnement énal, et o syndrome rganomegaly (syndrome TAFRO).
Critères diagnostiques
Le diagnostic de l'iMCD nécessite: la présence des deux critères majeurs, de multiples régions de ganglions lymphatiques hypertrophiés comme le démontre l'imagerie médicale; la présence d'au moins deux critères mineurs, dont au moins un doit être un test de laboratoire anormal; et l'exclusion des maladies qui peuvent imiter l'iMCD.
Critère majeur 1: plusieurs régions de ganglions lymphatiques hypertrophiés
L'imagerie radiologique doit mettre en évidence une hypertrophie des ganglions lymphatiques dans plusieurs régions.
Critère majeur 2: analyse microscopique de la biopsie ganglionnaire conforme à l'iMCD
L'aspect microscopique (histologie) du tissu biopsié d'un ganglion lymphatique hypertrophié doit démontrer une constellation de caractéristiques compatibles avec la maladie de Castleman. Il existe trois modèles de caractéristiques histologiques caractéristiques associées à l'iMCD:
- Hypervasculaire - centres germinatifs régressés , proéminence des cellules dendritiques folliculaires , hypervascularité dans les régions interfolliculaires et zones du manteau proéminentes avec une apparence de «peau d'oignon».
- Plasmacytique - augmentation du nombre de follicules avec de grands centres germinatifs hyperplasiques et plasmacytose en forme de feuille (augmentation du nombre de cellules plasmatiques ).
- Mixte - caractéristiques à la fois hypervasculaires et plasmocytaires.
iMCD présente le plus souvent des caractéristiques plasmocytaires; cependant, des caractéristiques hypervasculaires ou un mélange de caractéristiques hypervasculaires et plasmocytaires peuvent également être observées dans les ganglions lymphatiques iMCD. L'utilité clinique du sous-typage de l'iMCD par des caractéristiques histologiques est incertaine, car les sous-types histologiques ne prédisent pas systématiquement la gravité de la maladie ou la réponse au traitement.
La coloration avec l'antigène nucléaire associé à la latence (LANA-1) , un marqueur de l'infection par le HHV-8, doit être négative pour diagnostiquer l'iMCD.
Critères mineurs
Les patients doivent éprouver au moins deux des 11 critères mineurs suivants, au moins un étant un test de laboratoire anormal.
Tests de laboratoire:
- Taux de sédimentation élevé de la protéine C-réactive ou des érythrocytes
- Faible taux d'hémoglobine (anémie)
- Numération plaquettaire anormale (faible ou élevée)
- Faible taux d'albumine
- Créatinine élevée
- Augmentation des taux d'immunoglobulines (hypergammaglobulinémie)
Caractéristiques cliniques:
- Symptômes pseudo-grippaux
- Hypertrophie du foie et / ou de la rate
- Accumulation de liquide (œdème, ascite, épanchements pleuraux)
- Découvertes cutanées telles que hémangiomes de cerise ou papules violacées
- Pneumopathie interstitielle lymphocytaire
Maladies à exclure
Le diagnostic nécessite l'exclusion des maladies qui peuvent présenter des résultats cliniques similaires et une apparence similaire lors de l'analyse microscopique d'un tissu à partir d'un ganglion lymphatique élargi. Les maladies qui doivent être exclues du diagnostic de l'iMCD comprennent les maladies infectieuses, telles que la MCD associée au HHV-8 , la mononucléose du virus d'Epstein-Barr et la lymphadénopathie réactive ; les maladies auto-immunes, telles que le lupus érythémateux disséminé et la polyarthrite rhumatoïde ; et les cancers, y compris le lymphome , le myélome multiple et le plasmocytome des ganglions lymphatiques primaires .
Traitement
En raison de la rareté de l'iMCD, les données concernant le traitement sont limitées et basées sur une combinaison de séries de cas d'observation, de rapports de cas et d'un seul essai clinique randomisé. Contrairement à l'UCD, pour laquelle la chirurgie est le traitement de choix et curatif pour la plupart des patients, la chirurgie n'est pas efficace en iMCD. Au lieu d'un traitement chirurgical, une variété de médicaments sont utilisés en fonction de la gravité de la maladie et de la réponse du patient aux traitements antérieurs. Le siltuximab , un anticorps monoclonal ciblant l' IL-6 , est le seul médicament approuvé par la Food and Drug Administration (FDA) des États-Unis pour le traitement de l'iMCD; cependant, l'utilisation réussie d'autres médicaments a été rapportée dans la littérature.
En 2018, les premières lignes directrices de traitement consensuelles fondées sur des données probantes pour l'iMCD ont été publiées par un groupe international d'experts dans le domaine. En plus de créer un algorithme de traitement pour iMCD, ces directives de traitement ont établi des définitions communes de la gravité de la maladie et de la réponse au traitement.
Évaluation de la gravité de l'iMCD
Les patients atteints d'iMCD sont classés comme ayant une maladie grave ou non grave sur la base des 5 critères énumérés ci-dessous. Les patients avec 2 ou plus des critères ci-dessous sont classés comme ayant une maladie grave tandis que les patients avec 0 à 1 des critères sont classés comme ayant une maladie non sévère.
- État de performance de l' Eastern Cooperative Oncology Group (ECOG) ≥ 2
- Taux de filtration glomérulaire estimé (DFGe) <30 ou Créatinine> 3,0 mg / dL
- Anasarque et / ou ascite et / ou épanchement pleural et / ou épanchement péricardique
- Hémoglobine ≤ 8,0 g / dL
- Atteinte pulmonaire (par exemple, pneumopathie interstitielle avec dyspnée)
Réponse au traitement
Les patients atteints d'iMCD sont évalués pour la réponse au traitement en fonction des changements des symptômes, de la taille des ganglions lymphatiques impliqués et des tests de laboratoire. Chaque catégorie est classée comme réponse complète, réponse partielle, maladie stable ou maladie évolutive. La réponse globale au traitement est déterminée par la note la plus basse de la catégorie. Par exemple, un patient avec une réponse de laboratoire complète , une réponse partielle aux symptômes et une réponse complète des ganglions lymphatiques recevrait une réponse globale au traitement de réponse partielle . Voir ci-dessous pour les descriptions des critères et la notation des réponses.
Essais en laboratoire
Les tests de laboratoire comprennent tous les éléments suivants: protéine C-réactive, hémoglobine, albumine et DFGe.
- Réponse complète - Toutes les valeurs de laboratoire dans les plages normales
- Réponse partielle -> 50% dans toutes les valeurs de laboratoire
- Maladie stable - Toutes les valeurs de laboratoire entre <50% d'amélioration et <25% d'aggravation
- Maladie évolutive - aggravation de> 25% quelle que soit la valeur de laboratoire
Symptômes
Quatre symptômes sont évalués à l'aide des critères de terminologie communs des événements indésirables du National Cancer Institute (version 4): fatigue, anorexie, fièvre et poids corporel
- Réponse complète - Normalisation à la ligne de base avant la maladie
- Réponse partielle - Amélioration des 4 symptômes, mais pas par rapport à la ligne de base avant la maladie
- Maladie stable - Amélioration d'au moins 1 (mais pas de tous) symptômes
- Maladie évolutive - Aggravation d'au moins 1 symptôme sur 2 évaluations ou plus
Ganglion lymphatique
La réponse au traitement des ganglions lymphatiques est évaluée à l'aide de l'imagerie radiologique et classée comme réponse complète, réponse partielle, maladie stable et maladie progressive sur la base de critères de Cheson modifiés.
Algorithme de traitement
L'algorithme de traitement pour iMCD est basé principalement sur la gravité de la maladie et la réponse au traitement. En raison du taux élevé de rechute avec arrêt du traitement, la plupart des patients atteints d'iMCD sont traités indéfiniment avec des médicaments.
Maladie non sévère
Le siltuximab, un inhibiteur de l'IL-6, est le traitement recommandé pour tous les patients atteints d'iMCD non sévère, quels que soient les taux d'IL-6 mesurés. Le tocilizumab , un médicament qui cible également la voie IL-6, est couramment utilisé comme alternative au siltuximab lorsque le siltuximab n'est pas disponible. Des corticostéroïdes peuvent être ajoutés au traitement anti-IL-6 en fonction de la présentation clinique. Le rituximab , un médicament ciblant les cellules B, est principalement recommandé comme traitement de deuxième intention chez les patients qui ne répondent pas au siltuximab ou au tocilizumab, mais peut être utilisé comme agent de première intention chez les patients appropriés.
Pour les patients atteints d'une maladie non sévère qui ne répondent pas au siltuximab, au tocilizumab et au rituximab, les recommandations de traitement ne sont pas bien définies. Il a été rapporté que les chimiothérapies cytotoxiques induisent une rémission chez les patients atteints d'iMCD non sévère; Cependant, l'utilisation de chimiothérapies cytotoxiques n'est actuellement pas recommandée pour les iMCD non sévères en raison de la forte probabilité de rechute et des profils d'effets secondaires graves. Comme alternative, des immunomodulateurs tels que la thalidomide, la cyclosporine A, le sirolimus, le bortézomib et l'anakinra sont recommandés en raison de leurs taux de réponse similaires et de profils d'effets secondaires à long terme plus favorables.
Maladie sévère
Le traitement initial recommandé pour tous les patients atteints d'iMCD sévère consiste en des stéroïdes à forte dose associés à un agent anti-IL-6 tel que le siltuximab ou le tocilizumab, quels que soient les taux d'IL-6 mesurés. Pour les patients qui s'améliorent immédiatement avec ce régime, les stéroïdes peuvent être progressivement diminués, mais l'agent anti-IL-6 doit être poursuivi indéfiniment en raison du taux élevé de rechute à l'arrêt du traitement. En raison du risque élevé de complications associé à un iMCD sévère, si les patients s'aggravent ou ne s'améliorent pas avec des stéroïdes à forte dose et des thérapies anti-IL-6, des schémas de chimiothérapie cytotoxique sont recommandés. Les patients atteints d'une maladie potentiellement mortelle, en particulier ceux atteints du syndrome TAFRO, peuvent nécessiter des mesures avancées telles qu'une assistance respiratoire avec un ventilateur mécanique ou un traitement par dialyse pour une insuffisance rénale.
Suite à l'amélioration de l'état de la maladie, le traitement d'entretien avec un agent anti-IL-6 ou un médicament immunosuppresseur est généralement poursuivi indéfiniment, car l'arrêt de ces médicaments peut entraîner une rechute.
Suivre
Les patients atteints d'iMCD nécessitent une évaluation de routine de la réponse au traitement et de la progression de la maladie. Il est recommandé que les visites de suivi comprennent une évaluation des symptômes, un examen physique, des tests de laboratoire et une imagerie radiologique.
Pronostic
L'iMCD peut se présenter comme une maladie aiguë potentiellement mortelle chez certains patients ou une maladie chronique chez d'autres. Certains patients ont une maladie stable de longue date tandis que d'autres souffrent de poussées de maladie grave qui peuvent s'améliorer avec le traitement. Un traitement efficace contrôle les symptômes et le dysfonctionnement des organes associés à l'iMCD, améliore les symptômes et le dysfonctionnement des organes lors des poussées de maladie et prévient les futures poussées de maladies.
La survie observée dans une étude récente de patients iMCD était de 92% à 2 ans, 76% à 5 ans et 59% à 10 ans.
Épidémiologie
Il y a environ 1500-1800 nouveaux cas d'iMCD diagnostiqués par an aux États-Unis. L'iMCD peut survenir à tout âge, mais l'âge médian à la présentation est d'environ 50 ans. Il y a une incidence légèrement accrue d'iMCD chez les femmes.
Il n'y a eu aucune étude épidémiologique publiée sur la maladie de Castleman en dehors des États-Unis; cependant, il n'y a pas eu de données publiées démontrant une augmentation ou une diminution de l'incidence de la maladie de Castleman dans des régions ou des ethnies spécifiques.
Histoire
La maladie de Castleman a été décrite pour la première fois par le Dr Benjamin Castleman en 1956. La Journée mondiale de la maladie de Castleman a été créée en 2018 et a lieu chaque année le 23 juillet.
Culture
Le réseau de collaboration sur la maladie de Castleman a été fondé en 2012 et est la plus grande organisation axée sur la maladie de Castleman. Il s'agit d'un réseau collaboratif mondial impliqué dans la recherche, la sensibilisation et le soutien aux patients.
Les références
| Classification |
|---|
