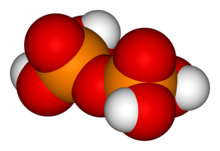
Acide pyrophosphorique - Pyrophosphoric acid

|
|
|
|
| Noms | |
|---|---|
|
Noms IUPAC
Acide diphosphorique
μ-oxido-bis (dihydroxidooxidophosphore) |
|
| Autres noms
Acide diphosphorique
|
|
| Identifiants | |
|
Modèle 3D ( JSmol )
|
|
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| Carte Info ECHA |
100.017.795 |
|
PubChem CID
|
|
| UNII | |
|
Tableau de bord CompTox ( EPA )
|
|
|
|
|
|
| Propriétés | |
| H 4 P 2 O 7 | |
| Masse molaire | 177,97 g / mol |
| Point de fusion | 71,5 ° C (160,7 ° F; 344,6 K) |
| Extrêmement soluble | |
| Solubilité | Très soluble dans l' alcool , l' éther |
| Base conjuguée | Pyrophosphate |
|
Sauf indication contraire, les données sont données pour les matériaux dans leur état standard (à 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Références Infobox | |
L'acide pyrophosphorique , également appelé acide diphosphorique , est le composé inorganique de formule H 4 P 2 O 7 ou, plus descriptivement, [(HO) 2 P (O)] 2 O. Incolore et inodore, il est soluble dans l' eau , l'éther diéthylique et l'alcool éthylique . L'acide anhydre cristallise en deux polymorphes qui fondent à 54,3 ° C et 71,5 ° C. Le composé n'est pas particulièrement utile, sauf qu'il est un composant de l'acide polyphosphorique et de l'acide conjugué de l'anion pyrophosphate. Les anions , sels et esters de l'acide pyrophosphorique sont appelés pyrophosphates .
Préparation
Il est préférable de le préparer par échange d'ions à partir du pyrophosphate de sodium ou en traitant le pyrophosphate de plomb avec du sulfure d'hydrogène . Il n'est pas préparé par déshydratation de l'acide phosphorique. Au lieu de cela, l'acide pyrophosphorique n'est produit que comme l'un des produits.
Réactions
Lorsqu'il est fondu, l'acide pyrophosphorique forme rapidement un mélange à l'équilibre d'acide phosphorique, d'acide pyrophosphorique et d'acides polyphosphoriques. Le pourcentage en poids d'acide pyrophosphorique est d'environ 40% et il est difficile de recristalliser dans la masse fondue. En solution aqueuse, l'acide pyrophosphorique, comme tous les acides polyphosphoriques, s'hydrolyse et finalement un équilibre s'établit entre l'acide phosphorique, l'acide pyrophosphorique et les acides polyphosphoriques.
- H 4 P 2 O 7 + H 2 O ⇌ 2H 3 PO 4
L'acide pyrophosphorique est un acide inorganique moyennement fort .
Sécurité
Bien que l'acide pyrophosporique soit corrosif, il n'est pas connu pour être autrement toxique.
Histoire
Le nom d'acide pyrophosphorique a été donné par un «M. Clarke de Glasgow» en 1827 à qui on attribue sa découverte suite au chauffage à la chaleur rouge d'un sel de phosphate de sodium. On a découvert que l'acide phosphorique, lorsqu'il est chauffé à la chaleur rouge, formait de l'acide pyrophosphorique qui était facilement converti en acide phosphorique par l'eau chaude.
Voir également
- Pyrophosphate de sodium
- Maladie des dépôts de pyrophosphate de calcium dihydraté
- Pyrophosphate de diméthylallyle
- ADP
- ATP
- Acides ortho
- acide triphosphorique
Les références
- ^ Corbridge, D. (1995). "Chapitre 3: Phosphates". Etudes en chimie inorganique vol. 20 . Elsevier Science BV pp. 169–305. doi : 10.1016 / B978-0-444-89307-9.50008-8 . ISBN 0-444-89307-5 .
- ^ Fiche signalétique: acide pyrophosphorique MSDS www.sciencelab.com
- ^ Beck, Lewis Caleb (1834). Un manuel de chimie: contenant une vue condensée de l'état actuel de la science, avec de nombreuses références à des traités plus étendus, des documents originaux, etc. EW & C Skinner. p. 160 . Récupéré le 30 janvier 2015 .
