Acide maléique - Maleic acid

|
|
|
|
|
|

|
|
| Noms | |
|---|---|
|
Nom IUPAC préféré
Acide (2 Z ) -But-2-énedioïque |
|
| Autres noms
Acide ( Z ) -butènedioïque; acide cis- butènedioïque; Acide malénique; Acide maléinique; Acide toxique
|
|
| Identifiants | |
|
Modèle 3D ( JSmol )
|
|
| 3DMet | |
| 605762 | |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| DrugBank | |
| Carte Info ECHA |
100,003,403 |
| Numéro CE | |
| 49854 | |
| KEGG | |
|
PubChem CID
|
|
| Numéro RTECS | |
| UNII | |
|
Tableau de bord CompTox ( EPA )
|
|
|
|
|
|
| Propriétés | |
| C 4 H 4 O 4 | |
| Masse molaire | 116,072 g · mol −1 |
| Apparence | Solide blanc |
| Densité | 1,59 g / cm³ |
| Point de fusion | 135 ° C (275 ° F; 408 K) (se décompose) |
| 478,8 g / L à 20 C | |
| Acidité (p K a ) | p k a1 = 1,9 p k a2 = 6,07 |
| -49,71 · 10 -6 cm 3 / mol | |
| Dangers | |
| Fiche de données de sécurité | Fiche signalétique de JT Baker |
| Pictogrammes SGH |

|
| Mot de signalisation SGH | Avertissement |
| H302 , H315 , H317 , H319 , H335 | |
| P261 , P264 , P270 , P271 , P272 , P280 , P301 + 312 , P302 + 352 , P304 + 340 , P305 + 351 + 338 , P312 , P321 , P330 , P332 + 313 , P333 + 313 , P337 + 313 , P362 , P363 , P403 + 233 , P405 , P501 | |
| NFPA 704 (diamant de feu) | |
| Composés apparentés | |
|
Acides carboxyliques apparentés
|
acide fumarique acide succinique acide crotonique |
|
Composés apparentés
|
maléimide anhydride maléique |
|
Sauf indication contraire, les données sont données pour les matériaux dans leur état standard (à 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Références Infobox | |
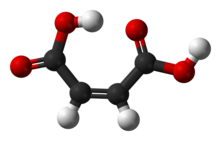
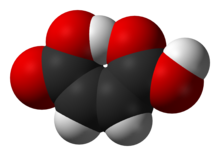
L'acide maléique ou acide cis- butènedioïque est un composé organique qui est un acide dicarboxylique , une molécule à deux groupes carboxyle . Sa formule chimique est HO 2 CCH = CHCO 2 H. L'acide maléique est l' isomère cis de l'acide butènedioïque, tandis que l'acide fumarique est l' isomère trans . Il est principalement utilisé comme précurseur de l'acide fumarique, et par rapport à son anhydride maléique parent , l'acide maléique a peu d'applications.
Propriétés physiques
L'acide maléique a une chaleur de combustion de -1 355 kJ / mol., 22,7 kJ / mol supérieure à celle de l'acide fumarique. L'acide maléique est plus soluble dans l'eau que l'acide fumarique . Le point de fusion de l'acide maléique (135 ° C) est également bien inférieur à celui de l'acide fumarique (287 ° C). Les deux propriétés de l'acide maléique peuvent être expliquées en raison de la liaison hydrogène intramoléculaire qui a lieu dans l'acide maléique au détriment des interactions intermoléculaires, et qui ne sont pas possibles dans l'acide fumarique pour des raisons géométriques.
Production et applications industrielles
Dans l'industrie, l'acide maléique est dérivé par hydrolyse de l'anhydride maléique , ce dernier étant produit par oxydation du benzène ou du butane .
L'acide maléique est une matière première industrielle pour la production d' acide glyoxylique par ozonolyse .
L'acide maléique peut être utilisé pour former des sels d'addition d'acide avec des médicaments pour les rendre plus stables, comme le maléate d'indacatérol.
L'acide maléique est également utilisé comme promoteur d'adhésion pour différents substrats, tels que le nylon et les métaux revêtus de zinc, par exemple l'acier galvanisé, dans les adhésifs à base de méthacrylate de méthyle.
Isomérisation en acide fumarique
La principale utilisation industrielle de l'acide maléique est sa conversion en acide fumarique . Cette conversion, une isomérisation , est catalysée par une variété de réactifs, tels que les acides minéraux et la thiourée . Encore une fois, la grande différence de solubilité dans l'eau facilite la purification de l'acide fumarique.
L' isomérisation est un sujet populaire dans les écoles. L'acide maléique et l'acide fumarique ne s'interconvertissent pas spontanément car la rotation autour d'une double liaison carbone-carbone n'est pas énergétiquement favorable. Cependant, la conversion de l' isomère cis en l' isomère trans est possible par photolyse en présence d'une petite quantité de brome . La lumière convertit le brome élémentaire en un radical brome , qui attaque l'alcène dans une réaction d' addition de radicaux à un radical bromo-alcane; et maintenant la rotation de liaison simple est possible. Les radicaux brome se recombinent et de l'acide fumarique se forme. Dans une autre méthode (utilisée comme démonstration en classe), l'acide maléique est transformé en acide fumarique par le processus de chauffage de l'acide maléique dans une solution d' acide chlorhydrique . L'addition réversible (de H + ) conduit à une rotation libre autour de la liaison CC centrale et à la formation de l'acide fumarique plus stable et moins soluble.
Certaines bactéries produisent l'enzyme maléate isomérase , qui est utilisée par les bactéries dans le métabolisme du nicotinate. Cette enzyme catalyse l'isomérisation entre le fumarate et le maléate.
Autres réactions
Bien que non pratiqué dans le commerce, l'acide maléique peut être converti en anhydride maléique par déshydratation , en acide malique par hydratation et en acide succinique par hydrogénation ( éthanol / palladium sur carbone ). Il réagit avec le chlorure de thionyle ou le pentachlorure de phosphore pour donner le chlorure d'acide maléique (il n'est pas possible d'isoler le mono-chlorure d'acide). L'acide maléique, étant électrophile, participe en tant que diénophile à de nombreuses réactions de Diels-Alder .
Maléates
L' ion maléate est la forme ionisée de l'acide maléique. L'ion maléate est utile en biochimie en tant qu'inhibiteur des réactions de transaminase . Les esters d' acide maléique sont également appelés maléates, par exemple le maléate de diméthyle .
Utilisation dans les médicaments pharmaceutiques
De nombreux médicaments qui contiennent des amines sont fournis sous forme de sel d'acide maléate , par exemple la carfénazine , la chlorphéniramine , la pyrilamine , la méthylergonovine et la thiéthylpérazine .

