Neisseria gonorrhoeae -Neisseria gonorrhoeae
| Neisseria gonorrhoeae | |
|---|---|
|
|
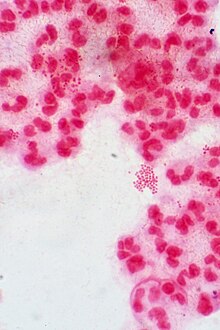
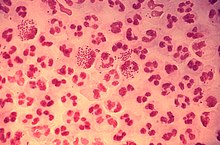
| Coloration de Gram de l' urétrite gonococcique . Notez la distribution dans les neutrophiles et la présence de bactéries intracellulaires et extracellulaires . ( CDC ) | |
|
Classement scientifique |
|
| Domaine: | Bactéries |
| Phylum: | Protéobactéries |
| Classer: | Bêtaprotéobactéries |
| Commander: | Neisseriales |
| Famille: | Neisseriacées |
| Genre: | Neisseria |
| Espèce: |
N. gonorrhoeae
|
| Nom binomial | |
|
Neisseria gonorrhoeae |
|
| Synonymes | |
Neisseria gonorrhoeae , également connu sousnom gonocoque (singulier), ou gonocoques (pluriel), est une espèce de Gram-négatives diplocoques bactéries isolées par Albert Neisser en 1879. Il provoque la sexuellement transmissible telle infection gonorrhée , ainsi queautres formes demaladiey compris gonococcique gonococcémie disséminée, arthrite septique et ophtalmie gonococcique du nouveau-né.
Il est oxydase positif et aérobie, et il survit à la phagocytose et se développe à l'intérieur des neutrophiles . Sa culture nécessite une supplémentation en dioxyde de carbone et une gélose enrichie ( chocolat agar ) avec divers antibiotiques ( Thayer-Martin ). Il présente une variation antigénique par recombinaison génétique de ses pili et des protéines de surface qui interagissent avec le système immunitaire .
La transmission sexuelle se fait par voie vaginale, anale ou orale. La transmission sexuelle peut être évitée grâce à l'utilisation d'une barrière de protection. La transmission périnatale peut se produire pendant l'accouchement et peut être prévenue par un traitement antibiotique de la mère avant la naissance et l'application d'un gel oculaire antibiotique sur les yeux du nouveau-né. Après un épisode d'infection gonococcique, les personnes infectées ne développent pas d'immunité contre les infections futures. La réinfection est possible en raison de la capacité de N. gonorrhoeae à échapper au système immunitaire en faisant varier ses protéines de surface.
N. gonorrhoeae peut provoquer une infection des organes génitaux, de la gorge et des yeux. L'infection asymptomatique est fréquente chez les hommes et les femmes. Une infection non traitée peut se propager au reste du corps (infection gonococcique disséminée), en particulier aux articulations (arthrite septique). Une infection non traitée chez la femme peut provoquer une maladie inflammatoire pelvienne et une stérilité possible en raison des cicatrices qui en résultent. Le diagnostic repose sur la culture , la coloration de Gram ou les tests d'acide nucléique , tels que la réaction en chaîne par polymérase , d'un échantillon d'urine, d'un écouvillonnage urétral ou d'un écouvillon cervical. Le co-test de la chlamydia et le dépistage d'autres IST sont recommandés en raison des taux élevés de co-infection.
Microbiologie
Neisseria espèces sont pointilleux , Cocci Gram négatif qui nécessitentsupplémentationnutriments pourdévelopper danscultures de laboratoire. Neisseria spp. sont facultativement intracellulaires et apparaissent généralement par paires (diplocoques), ressemblant à la forme de grains de café. Nesseria ne forme pas de spores, est capable de se déplacer en utilisant la motilité convulsive et est un aérobie obligatoire (nécessite de l'oxygène pour se développer). Sur les 11 espèces de Neisseria qui colonisent l'homme, seules deux sont des agents pathogènes. N. gonorrhoeae est l'agent causal de la gonorrhée et N. meningitidis est une cause de méningite bactérienne.
Culture et identification
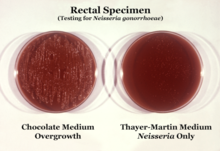
N. gonorrhoeae est généralement isolé sur gélose Thayer-Martin (ou VPN) dans une atmosphère enrichie de 3-7% de dioxyde de carbone. La gélose Thayer-Martin est une plaque de gélose au chocolat (gélose au sang chauffée) contenant des nutriments et des antimicrobiens ( vancomycine , colistine , nystatine et triméthoprime ). Cette préparation de gélose facilite la croissance des espèces de Neisseria tout en inhibant la croissance des bactéries et champignons contaminants. Les géloses Martin Lewis et New York City sont d'autres types de géloses au chocolat sélectives couramment utilisées pour la croissance de Neisseria . N. gonorrhoeae est oxydase positive (possédant la cytochrome c oxydase) et catalase positive (capable de convertir le peroxyde d'hydrogène en oxygène). Lorsqu'il est incubé avec les glucides lactose, maltose , saccharose et glucose , N. gonorrhoeae n'oxyde que le glucose.
Molécules de surface
À sa surface, N. gonorrhoeae porte des pili ressemblant à des cheveux , des protéines de surface ayant diverses fonctions et des sucres appelés lipooligosaccharides . Les pili assurent la médiation de l'adhérence, du mouvement et de l'échange d'ADN. Les protéines Opa interagissent avec le système immunitaire, tout comme les porines . Lipooligosaccharide (LOS) est une endotoxine qui provoque une réponse immunitaire. Tous sont antigéniques et présentent tous une variation antigénique (voir ci-dessous). Les pili présentent le plus de variations. Les pili, les protéines Opa, les porines et même le LOS ont des mécanismes pour inhiber la réponse immunitaire, rendant possible une infection asymptomatique.
Les filaments de protéines polymères dynamiques appelés pili de type IV permettent à N. gonorrhoeae d'adhérer et de se déplacer le long des surfaces. Pour pénétrer dans l'hôte, la bactérie utilise les pili pour adhérer aux surfaces muqueuses et les pénétrer. Les pili sont un facteur de virulence nécessaire pour N. gonorrhoeae ; sans eux, la bactérie est incapable de provoquer une infection. Pour se déplacer, les bactéries individuelles utilisent leurs pili comme un grappin : d'abord, ils s'étendent à partir de la surface cellulaire et se fixent à un substrat . La rétraction subséquente du pilus entraîne la cellule vers l'avant. Le mouvement qui en résulte est appelé motilité de contraction. N. gonorrhoeae est capable de tirer 100 000 fois son propre poids, et les pili utilisés pour le faire sont parmi les moteurs biologiques les plus puissants connus à ce jour, exerçant un nanonewton . Les protéines PilF et PilT ATPase sont respectivement responsables de l'extension et de la rétraction du pilus de type IV. Les fonctions adhésives du pilus gonococcique jouent un rôle dans l' agrégation des microcolonies et la formation de biofilm . Les protéines de surface appelées protéines Opa peuvent être utilisées pour se lier aux récepteurs des cellules immunitaires et empêcher une réponse immunitaire. Au moins 12 protéines Opa sont connues et les nombreuses permutations des protéines de surface rendent plus difficile la reconnaissance de N. gonorrhoeae et la mise en place d'une défense par les cellules immunitaires.
Lipooligosaccharide (LOS) est une version de faible poids de lipopolysaccharide présent sur les surfaces de la plupart des autres bactéries Gram-négatives. Il s'agit d'une chaîne latérale de sucre (saccharide) attachée au lipide A (donc "lipo-") dans la membrane externe recouvrant la paroi cellulaire de la bactérie. La racine "oligo" fait référence au fait qu'elle est plus courte de quelques sucres que le lipopolysaccharide typique. En tant qu'endotoxine, le LOS provoque une inflammation. L'excrétion de LOS par la bactérie est responsable d'une lésion locale dans, par exemple, une maladie inflammatoire pelvienne. Bien que sa fonction principale soit celle d'endotoxine, le LOS peut se déguiser en acide sialique hôte et bloquer l'initiation de la cascade du complément .
Variation antigénique
N. gonorrhoeae échappe au système immunitaire par un processus appelé variation antigénique . Ce processus permet à N. gonorrhoeae de recombiner ses gènes et de modifier les déterminants antigéniques (sites de liaison des anticorps), tels que les pili de type IV, qui ornent sa surface. En termes simples, la composition chimique des molécules est modifiée en raison de changements au niveau génétique. N. gonorrhoeae est capable de faire varier la composition de ses pili, et LOS ; parmi ceux-ci, les pili présentent la variation la plus antigénique due au réarrangement chromosomique. Le gène PilS est un exemple de cette capacité à se réarranger car on estime que sa combinaison avec le gène PilE produit plus de 100 variantes de la protéine PilE. Ces changements permettent de s'adapter aux différences d'environnement local sur le site d'infection, d'échapper à la reconnaissance par les anticorps ciblés et contribuent à l'absence d'un vaccin efficace.
En plus de la capacité de réarranger les gènes qu'il possède déjà, il est aussi naturellement compétent pour acquérir de nouveaux ADN (via des plasmides ), via son pilus de type IV, plus précisément les protéines Pil Q et Pil T. Ces processus permettent à N. gonorrhoeae d'acquérir/ propager de nouveaux gènes, se déguiser avec différentes protéines de surface et empêcher le développement de la mémoire immunologique - une capacité qui a conduit à la résistance aux antibiotiques et a également entravé le développement de vaccins.
Variation de phase
La variation de phase est similaire à la variation antigénique, mais au lieu de changements au niveau génétique modifiant la composition des molécules, ces changements génétiques entraînent l'activation ou la désactivation d'un gène. La variation de phase résulte le plus souvent d'un décalage du cadre de lecture dans le gène exprimé. Les protéines Opacity, ou Opa, de N. gonorrhoeae reposent strictement sur la variation de phase. Chaque fois que les bactéries se répliquent, elles peuvent activer ou désactiver plusieurs protéines Opa par mésappariement des brins glissés . C'est-à-dire que les bactéries introduisent des mutations de décalage du cadre de lecture qui amènent des gènes dans ou hors du cadre. Le résultat est que différents gènes Opa sont traduits à chaque fois. Les pili sont variés par la variation antigénique, mais aussi par la variation de phase. Des décalages de cadre se produisent à la fois dans les gènes pilE et pilC , désactivant efficacement l'expression des pili dans des situations où ils ne sont pas nécessaires, comme après la colonisation lorsque N. gonorrhoeae survit dans les cellules plutôt qu'à leur surface.
Survie des gonocoques
Une fois que les gonocoques ont envahi et transcytosé les cellules épithéliales de l'hôte, ils atterrissent dans la sous-muqueuse, où les neutrophiles les consomment rapidement. Les protéines pili et Opa à la surface peuvent interférer avec la phagocytose, mais la plupart des gonocoques se retrouvent dans les neutrophiles. Les exsudats des individus infectés contiennent de nombreux neutrophiles avec des gonocoques ingérés. Les neutrophiles libèrent une explosion oxydative d' espèces réactives de l'oxygène dans leurs phagosomes pour tuer les gonocoques. Cependant, une fraction importante des gonocoques peut résister à la mort grâce à l'action de leur catalase qui décompose les espèces réactives de l'oxygène et est capable de se reproduire dans les phagosomes neutrophiles.
Stohl et Seifert ont montré que la protéine bactérienne RecA, qui médie la réparation des dommages à l'ADN, joue un rôle important dans la survie des gonocoques. Michod et al. ont suggéré que N. gonorrhoeae pourrait remplacer l'ADN endommagé dans les phagosomes neutrophiles par l'ADN de gonocoques voisins. Le processus par lequel les gonocoques receveurs intègrent l'ADN des gonocoques voisins dans leur génome est appelé transformation.
Génome
Les génomes de plusieurs souches de N . gonorrhoeae ont été séquencés. La plupart d'entre eux ont une taille d'environ 2,1 Mo et codent pour 2 100 à 2 600 protéines (bien que la plupart semblent être dans la plage inférieure). Par exemple, la souche NCCP11945 se compose d'un chromosome circulaire (2 232 025 pb) codant 2 662 cadres de lecture ouverts (ORF) prédits et d'un plasmide (4 153 pb) codant 12 ORF prédits. La densité de codage estimée sur l'ensemble du génome est de 87 % et la teneur moyenne en G+C est de 52,4 %, valeurs proches de celles de la souche FA1090. Le génome NCCP11945 code 54 ARNt et quatre copies d'opérons d'ARNr 16S-23S-5S.
Transfert horizontal de gènes
En 2011, des chercheurs de la Northwestern University ont trouvé des preuves d'un fragment d'ADN humain dans un génome de N. gonorrhoeae , le premier exemple de transfert horizontal de gènes de l'homme à un agent pathogène bactérien.
Maladie
Les symptômes de l'infection par N. gonorrhoeae diffèrent selon le site d'infection et de nombreuses infections sont asymptomatiques indépendamment du sexe. Chez les hommes symptomatiques, le principal symptôme de l'infection génito-urinaire est l'urétrite - brûlure à la miction ( dysurie ), augmentation du besoin d'uriner et écoulement (purulent) ressemblant à du pus du pénis. La décharge peut avoir une odeur nauséabonde. Si elle n'est pas traitée, la cicatrisation de l' urètre peut entraîner des difficultés à uriner. L'infection peut se propager de l'urètre dans le pénis aux structures voisines, y compris les testicules ( épididymite / orchite ), ou à la prostate ( prostatite ). Les hommes qui ont eu une infection gonococcique ont un risque significativement accru d'avoir un cancer de la prostate. Chez les femmes symptomatiques, les principaux symptômes d'une infection génito-urinaire sont une augmentation des pertes vaginales, des brûlures à la miction ( dysurie ), une augmentation du besoin d'uriner, des douleurs lors des rapports sexuels ou des anomalies menstruelles. La maladie inflammatoire pelvienne se produit si N. gonorrhoeae monte dans le péritoine pelvien (via le col de l' utérus , l' endomètre et les trompes de Fallope ). L'inflammation et la cicatrisation des trompes de Fallope qui en résultent peuvent entraîner une infertilité et un risque accru de grossesse extra-utérine. Une maladie inflammatoire pelvienne se développe chez 10 à 20 % des femelles infectées par N. gonorrhoeae . Il est important de noter que selon la voie de transmission, N. gonorrhoeae peut provoquer une infection de la gorge ( pharyngite ) ou une infection de l'anus/du rectum ( rectite ).
Dans l'infection périnatale , la manifestation primaire est une infection de l'œil (conjonctivite néonatale ou ophtalmie néonatale ) lorsque le nouveau-né est exposé à N. gonorrhoeae dans la filière génitale . L'infection oculaire peut entraîner des cicatrices ou une perforation de la cornée, entraînant finalement la cécité. Si le nouveau-né est exposé pendant l'accouchement, la conjonctivite survient dans les 2 à 5 jours suivant la naissance et est sévère. L'ophtalmie gonococcique du nouveau-né, autrefois courante chez les nouveau-nés, est prévenue par l'application de gel d' érythromycine (antibiotique) sur les yeux des bébés à la naissance en tant que mesure de santé publique. Le nitrate d'argent n'est plus utilisé aux États-Unis.
Des infections gonococciques disséminées peuvent survenir lorsque N. gonorrhoeae pénètre dans la circulation sanguine, se propageant souvent aux articulations et provoquant une éruption cutanée (syndrome dermatite-arthrite). Le syndrome dermatite-arthrite se traduit par des douleurs articulaires ( arthrite ), une inflammation des tendons ( ténosynovite ) et une dermatite indolore non prurigineuse (non prurigineuse) . L'infection disséminée et la maladie inflammatoire pelvienne chez les femmes ont tendance à commencer après les règles en raison du reflux pendant les règles, ce qui facilite la propagation. Dans de rares cas, une infection disséminée peut provoquer une infection des méninges du cerveau et de la moelle épinière ( méningite ) ou une infection des valves cardiaques ( endocardite ).
Transmission
N. gonorrhoeae est transmis lors de relations sexuelles vaginales, orales ou anales; la transmission non sexuelle est peu probable en cas d'infection chez l'adulte. Il peut également être transmis au nouveau-né lors du passage dans le canal génital si la mère a une infection génito-urinaire non traitée. Étant donné le taux élevé d'infection asymptomatique, toutes les femmes enceintes devraient subir un test de dépistage de la gonorrhée. Cependant, les bains communs, les serviettes ou le tissu, les thermomètres rectaux et les mains des soignants ont été mis en cause comme moyens de transmission en milieu pédiatrique. Le baiser a également été impliqué comme moyen théorique de transmission dans la population masculine gay, sur la base d'une étude plus récente.
Traditionnellement, on pensait que la bactérie se déplaçait attachée aux spermatozoïdes, mais cette hypothèse n'expliquait pas la transmission de la maladie de la femme à l'homme. Une étude récente suggère qu'au lieu de « surfer » sur des spermatozoïdes agités , les bactéries N. gonorrhoeae utilisent des pili pour s'ancrer sur les protéines du sperme et se déplacer dans le liquide coïtal.
Infection
Pour N. gonorrhoeae , la première étape après une transmission réussie est l'adhérence aux cellules épithéliales trouvées sur le site muqueux qui est infecté. La bactérie repose sur des pili de type IV qui s'attachent et se rétractent, tirant N. gonorrhoeae vers la membrane épithéliale où ses protéines de surface, telles que les protéines d'opacité, peuvent interagir directement. Après adhérence, N. gonorrhoeae se réplique et forme des microcolonies . Pendant la colonisation, N. gonorrhoeae a le potentiel de transcytoser à travers la barrière épithéliale et de se frayer un chemin dans la circulation sanguine. Au cours de la croissance et de la colonisation, N. gonorrhoeae stimule la libération de cytokines et de chimiokines par les cellules immunitaires de l'hôte qui sont pro-inflammatoires . Ces molécules pro-inflammatoires entraînent le recrutement de macrophages et de neutrophiles . Ces cellules phagocytaires absorbent généralement des agents pathogènes étrangers et les détruisent, mais N. gonorrhoeae a développé de nombreux mécanismes qui lui permettent de survivre au sein de ces cellules immunitaires et de contrecarrer les tentatives d'élimination.
La prévention
La transmission est réduite en utilisant des barrières en latex (par exemple des préservatifs ou des digues dentaires ) pendant les rapports sexuels et en limitant les partenaires sexuels. Les préservatifs et les digues dentaires doivent également être utilisés pendant les relations sexuelles orales et anales. Les spermicides, les mousses vaginales et les douches vaginales ne sont pas efficaces pour prévenir la transmission.
Traitement
Le traitement actuel recommandé par le CDC est une double antibiothérapie. Cela comprend une dose unique injectée de ceftriaxone (une céphalosporine de troisième génération ) avec de l' azithromycine administrée par voie orale. L'azithromycine est préférée pour une couverture supplémentaire de la gonorrhée qui peut être résistante aux céphalosporines mais sensible aux macrolides. Les partenaires sexuels (définis par le CDC comme des contacts sexuels au cours des 60 derniers jours) doivent également être informés, testés et traités. Il est important que si les symptômes persistent après avoir reçu le traitement de l' infection à N. gonorrhoeae , une réévaluation soit poursuivie.
Résistance aux antibiotiques
La résistance aux antibiotiques dans la gonorrhée a été notée à partir des années 1940. La gonorrhée a été traitée avec de la pénicilline, mais les doses ont dû être progressivement augmentées pour rester efficace. Dans les années 1970, la gonorrhée résistante à la pénicilline et à la tétracycline est apparue dans le bassin du Pacifique. Ces souches résistantes se sont ensuite propagées à Hawaï, en Californie, dans le reste des États-Unis, en Australie et en Europe. Les fluoroquinolones étaient la ligne de défense suivante, mais bientôt une résistance à cet antibiotique est également apparue. Depuis 2007, le traitement standard repose sur les céphalosporines de troisième génération, comme la ceftriaxone, qui sont considérées comme notre « dernière ligne de défense ».
Récemment, une souche de gonorrhée hautement résistante à la ceftriaxone appelée H041 a été découverte au Japon. Des tests en laboratoire ont révélé qu'il était résistant à des concentrations élevées de ceftriaxone, ainsi qu'à la plupart des autres antibiotiques testés. Dans N. gonorrhoeae , il existe des gènes qui confèrent une résistance à chaque antibiotique utilisé pour guérir la gonorrhée, mais jusqu'à présent, ils ne coexistent pas au sein d'un seul gonocoque. Cependant, en raison de la grande affinité de N. gonorrhoeae pour le transfert horizontal de gènes, la gonorrhée résistante aux antibiotiques est considérée comme une menace émergente pour la santé publique.
Résistance au sérum
En tant que bactérie à Gram négatif, N. gonorrhoeae a besoin de mécanismes de défense pour se protéger contre le système du complément (ou cascade du complément), dont les composants se retrouvent dans le sérum humain . Il existe trois voies différentes qui activent ce système, mais elles entraînent toutes l'activation de la protéine du complément 3 (C3). Une partie clivée de cette protéine, C3b , se dépose sur des surfaces pathogènes et entraîne une opsonisation ainsi que l'activation en aval du complexe d'attaque membranaire . N. gonorrhoeae a plusieurs mécanismes pour éviter cette action. Dans l'ensemble, ces mécanismes sont appelés résistance sérique.
Histoire
Origine du nom
Neisseria gonorrhoeae doit son nom à Albert Neisser, qui l'a isolé comme agent causal de la gonorrhée en 1878. Galien (130 après JC) a inventé le terme « gonorrhée » du grec gonos qui signifie « graine » et rhoe qui signifie « flux ». Ainsi, la gonorrhée signifie "flux de graines", une description faisant référence à l'écoulement blanc du pénis, supposé être du sperme, observé dans l'infection masculine.
Découverte
En 1878, Albert Neisser a isolé et visualisé des diplocoques de N. gonorrhoeae dans des échantillons de pus de 35 hommes et femmes présentant les symptômes classiques d'une infection génito-urinaire par la gonorrhée - dont deux avaient également des infections des yeux. En 1882, Leistikow et Loeffler ont pu développer l'organisme en culture. Puis, en 1883, Max Bockhart a prouvé de manière concluante que la bactérie isolée par Albert Neisser était l'agent causal de la maladie connue sous le nom de gonorrhée en inoculant la bactérie au pénis d'un homme en bonne santé. L'homme a développé les symptômes classiques de la gonorrhée quelques jours plus tard, satisfaisant le dernier des postulats de Koch . Jusqu'à ce point, les chercheurs se demandaient si la syphilis et la gonorrhée étaient des manifestations de la même maladie ou de deux entités distinctes. L'un de ces chercheurs du XVIIIe siècle, John Hunter, a tenté de trancher le débat en 1767 en inoculant à un homme du pus prélevé sur un patient atteint de gonorrhée. Il a conclu à tort que la syphilis et la gonorrhée étaient en effet la même maladie lorsque l'homme a développé l'éruption de couleur cuivre qui est classique pour la syphilis. Bien que de nombreuses sources répètent que Hunter s'est vacciné, d'autres ont soutenu qu'il s'agissait en fait d'un autre homme. Après l'expérience de Hunter, d'autres scientifiques ont cherché à réfuter ses conclusions en inoculant du pus gonorrhéique à d'autres médecins, étudiants en médecine et hommes incarcérés, qui ont tous développé des brûlures et des écoulements de gonorrhée. Un chercheur, Ricord, a pris l'initiative d'effectuer 667 inoculations de pus gonorrhéique sur des patients d'un hôpital psychiatrique, avec zéro cas de syphilis. Notamment, l'avènement de la pénicilline dans les années 1940 a rendu disponibles des traitements efficaces contre la gonorrhée.
Voir également
Les références
Liens externes
| Scholia a un profil thématique pour Neisseria gonorrhoeae . |
- Todar, Kenneth. « Neisseriae pathogène : gonorrhée, ophtalmie néonatale et méningite à méningocoque » . Manuel de bactériologie en ligne de Todar .
- Gonorrhée chez eMedicine
- " Neisseria gonorrhoeae " . Navigateur de taxonomie NCBI . 485.