Pémétrexed - Pemetrexed
 | |
 | |
| Donnée clinique | |
|---|---|
| Appellations commerciales | Alimta, Pemfexy, Ciambra, autres |
| AHFS / Drugs.com | Monographie |
| Données de licence | |
Catégorie de grossesse |
|
| Voies d' administration |
Intraveineux |
| Code ATC | |
| Statut légal | |
| Statut légal | |
| Données pharmacocinétiques | |
| Biodisponibilité | N / A |
| Liaison protéique | 81% |
| Métabolisme | Négligeable |
| Demi-vie d' élimination | 3,5 heures |
| Excrétion | Un rein |
| Identifiants | |
| |
| Numero CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEMBL | |
| Tableau de bord CompTox ( EPA ) | |
| Carte Info ECHA |
100.205.735 |
| Données chimiques et physiques | |
| Formule | C 20 H 21 N 5 O 6 |
| Masse molaire | 427,417 g · mol −1 |
| Modèle 3D ( JSmol ) | |
| |
| |
|
| |
Le pemetrexed , vendu sous le nom de marque Alimta entre autres, est un médicament de chimiothérapie pour le traitement du mésothéliome pleural et du cancer du poumon non à petites cellules (CPNPC).
Usage médical
En février 2004, la Food and Drug Administration (FDA) des États-Unis a approuvé le pemetrexed pour le traitement du mésothéliome pleural malin, un type de tumeur du mésothélium , la fine couche de tissu qui recouvre de nombreux organes internes, en association avec le cisplatine pour les patients dont la maladie est non résécable ou qui ne sont pas autrement des candidats à la chirurgie curative. En septembre 2008, la FDA a accordé son approbation en tant que traitement de première intention, en association avec le cisplatine, contre le cancer du poumon non à petites cellules (CPNPC) localement avancé et métastatique chez des patients présentant une histologie non épidermoïde.
Carboplatine
Le pémétrexed est également recommandé en association avec le carboplatine et le pembrolizumab pour le traitement de première intention du cancer du poumon non à petites cellules avancé. Cependant, l'efficacité ou la toxicité relative du pémétrexed-cisplatine par rapport au pémétrexed-carboplatine n'a pas été établie au-delà de ce que l'on pense généralement au traitement médicamenteux par le cisplatine ou le carboplatine doublet.
Supplémentation
Il est recommandé aux patients de prendre un supplément d'acide folique et de vitamine B 12 même si les taux sont normaux lorsqu'ils sont sous traitement par pemetrexed. (Dans les essais cliniques sur le mésothéliome, la supplémentation en acide folique et en vitamine B12 a réduit la fréquence des événements indésirables.) Il est également recommandé aux patients de prendre un glucocorticoïde (par exemple dexaméthasone ) la veille, le jour et le jour après la perfusion de pemetrexed pour éviter éruptions cutanées.
Effets secondaires
Le pémétrexed, qu'il soit utilisé seul ou en association avec le cisplatine, présente les effets indésirables suivants:
- Faible nombre de cellules sanguines , mesuré par une formule sanguine complète . Il s'agit d'une toxicité limitant la dose.
- Fatigue mentale et somnolence . La fatigue peut être réduite grâce à une prescription de modafinil hors AMM .
- Nausées et vomissements . Les effets émétogènes du pémétrexed sont gérés avec des antiémétiques prophylactiques .
- La diarrhée
- Mucite buccale (plaies dans la bouche, la gorge ou les lèvres). Les ulcères buccaux peuvent être atténués par une bonne hygiène bucco-dentaire, y compris le rinçage de la bouche avec de l'eau salée après la consommation d'aliments ou de boissons.
- Perte d'appétit
- Peau éruption . Les glucocorticoïdes prescrits par le médecin et administrés la veille, le jour de la perfusion et le lendemain de la perfusion évitent généralement les éruptions cutanées.
- Constipation
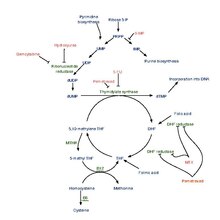
Mécanisme d'action
Le pémétrexed est chimiquement similaire à l'acide folique et appartient à la classe des agents chimiothérapeutiques appelés antimétabolites des folates . Il agit en inhibant trois enzymes utilisées dans la synthèse de la purine et de la pyrimidine: la thymidylate synthase (TS), la dihydrofolate réductase (DHFR) et la glycinamide ribonucléotide formyltransférase (GARFT). En inhibant la formation de nucléotides précurseurs de purine et de pyrimidine , le pemetrexed empêche la formation d' ADN et d' ARN , qui sont nécessaires à la croissance et à la survie des cellules normales et des cellules cancéreuses.
Histoire
La structure moléculaire du pemetrexed a été développée par Edward C. Taylor de l'Université de Princeton et cliniquement développée par le fabricant de médicaments basé à Indianapolis, Eli Lilly and Company en 2004.
Il a été étudié dans l' essai PARAMOUNT .
Société et culture
Appellations commerciales
En plus du nom de marque Alimta, ce médicament est également commercialisé en Inde par Abbott Healthcare sous le nom de Pleumet et par Cadila Healthcare sous le nom de Pemecad . En février 2020, Pemfexy a été approuvé pour une utilisation aux États-Unis.
Coût
Aux États-Unis, en 2015, chaque flacon de médicament coûte entre 2 623 $ US et 3 100 $ US .
Recherche
Une étude de phase III a montré les avantages de l'utilisation d'entretien du pemetrexed pour le CPNPC non squameux. Une activité a été démontrée dans le mésothéliome péritonéal malin. Des essais le testent actuellement contre le cancer de l'œsophage , le chordome et d'autres cancers.
Les références
Liens externes
- "Pemetrexed" . Portail d'information sur les médicaments . Bibliothèque nationale de médecine des États-Unis.
- "Pemetrexed disodique" . Portail d'information sur les médicaments . Bibliothèque nationale de médecine des États-Unis.
- "Pemetrexed disodique" . Dictionnaire des médicaments NCI . Institut national du cancer.
- "Pemetrexed disodique" . Institut national du cancer .