Densité - Density
| Densité | |
|---|---|
 Un cylindre gradué contenant divers liquides colorés non miscibles avec différentes densités
| |
Symboles communs |
ρ , D |
| Unité SI | kg/ m3 |
| Vaste ? | Non |
| Intensif ? | Oui |
| Conservé ? | Non |
Dérivations d' autres quantités |
|
| Dimension | |
La densité (plus précisément, la masse volumique volumique ; également appelée masse spécifique ), d'une substance est sa masse par unité de volume . Le symbole le plus souvent utilisé pour la densité est ρ (la lettre grecque minuscule rho ), bien que la lettre latine D puisse également être utilisée. Mathématiquement, la densité est définie comme la masse divisée par le volume :
où ρ est la densité, m est la masse, et V est le volume. Dans certains cas (par exemple, dans l'industrie pétrolière et gazière des États-Unis), la densité est vaguement définie comme son poids par unité de volume , bien que cela soit scientifiquement inexact - cette quantité est plus précisément appelée poids spécifique .
Pour une substance pure, la densité a la même valeur numérique que sa concentration massique . Différents matériaux ont généralement des densités différentes, et la densité peut être pertinente pour la flottabilité , la pureté et l' emballage . L'osmium et l' iridium sont les éléments connus les plus denses dans des conditions standard de température et de pression .
Pour simplifier les comparaisons de densité entre différents systèmes d'unités, elle est parfois remplacée par la quantité sans dimension « densité relative » ou « densité », c'est-à-dire le rapport de la densité du matériau à celle d'un matériau standard, généralement de l'eau. Ainsi, une densité relative inférieure à un par rapport à l'eau signifie que la substance flotte dans l'eau.
La densité d'un matériau varie avec la température et la pression. Cette variation est généralement faible pour les solides et les liquides, mais beaucoup plus importante pour les gaz. L'augmentation de la pression sur un objet diminue le volume de l'objet et augmente ainsi sa densité. L'augmentation de la température d'une substance (à quelques exceptions près) diminue sa densité en augmentant son volume. Dans la plupart des matériaux, le chauffage du fond d'un fluide entraîne une convection de la chaleur du bas vers le haut, en raison de la diminution de la densité du fluide chauffé, ce qui le fait monter par rapport à un matériau non chauffé plus dense.
La réciproque de la densité d'une substance est parfois appelée son volume spécifique , terme parfois utilisé en thermodynamique . La densité est une propriété intensive en ce sens que l'augmentation de la quantité d'une substance n'augmente pas sa densité ; il augmente plutôt sa masse.
Histoire
Dans bien connu , mais probablement apocryphe conte, Archimedes a été chargé de déterminer si le roi Hiéron de goldsmith détournait l' or lors de la fabrication d'une or couronne dédiée aux dieux et de le remplacer par un autre, moins cher alliage . Archimède savait que la couronne de forme irrégulière pouvait être écrasée en un cube dont le volume pouvait être calculé facilement et comparé à la masse ; mais le roi ne l'approuva pas. Déconcerté, Archimède aurait pris un bain d'immersion et observé à partir de la montée de l'eau en entrant qu'il pouvait calculer le volume de la couronne d'or grâce au déplacement de l'eau. Sur cette découverte, il a sauté de son bain et a couru nu dans les rues en criant : « Eurêka ! Eurêka ! (Εύρηκα! Grec "Je l'ai trouvé"). En conséquence, le terme « eurêka » est entré dans le langage courant et est utilisé aujourd'hui pour indiquer un moment d'illumination.
L'histoire est apparue pour la première fois sous forme écrite dans les livres d'architecture de Vitruve , deux siècles après qu'elle aurait eu lieu. Certains savants ont douté de l'exactitude de ce récit, affirmant entre autres que la méthode aurait nécessité des mesures précises qui auraient été difficiles à faire à l'époque.
Mesure de la densité
Un certain nombre de techniques ainsi que des normes existent pour la mesure de la densité des matériaux. Ces techniques comprennent l'utilisation d'un hydromètre (une méthode de flottabilité pour les liquides), d'une balance hydrostatique (une méthode de flottabilité pour les liquides et les solides), la méthode du corps immergé (une méthode de flottabilité pour les liquides), le pycnomètre (liquides et solides), le pycnomètre de comparaison d'air ( solides), densitomètre oscillant (liquides), ainsi que verser et tapoter (solides). Cependant, chaque méthode ou technique individuelle mesure différents types de densité (par exemple, densité apparente, densité squelettique, etc.), et il est donc nécessaire de comprendre le type de densité mesuré ainsi que le type de matériau en question.
Unité
De l'équation pour la densité ( ρ = m / V ), la densité de masse a une unité qui est la masse divisée par le volume . Comme il existe de nombreuses unités de masse et de volume couvrant de nombreuses grandeurs différentes, il existe un grand nombre d'unités de densité de masse utilisées. L' unité SI de kilogramme par mètre cube (kg/m 3 ) et l' unité cgs de gramme par centimètre cube (g/cm 3 ) sont probablement les unités les plus couramment utilisées pour la densité. Un g/cm 3 est égal à 1000 kg/m 3 . Un centimètre cube (abréviation cc) équivaut à un millilitre. Dans l'industrie, d'autres unités de masse et/ou de volume plus grandes ou plus petites sont souvent plus pratiques et les unités usuelles américaines peuvent être utilisées. Voir ci-dessous pour une liste de certaines des unités de densité les plus courantes.
Matériaux homogènes
La densité en tous points d'un objet homogène est égale à sa masse totale divisée par son volume total. La masse est normalement mesurée avec une balance ou une balance ; le volume peut être mesuré directement (à partir de la géométrie de l'objet) ou par le déplacement d'un fluide. Pour déterminer la densité d'un liquide ou d' un gaz, d' un densimètre , un dasymeter ou un écoulement de Coriolis peut être utilisée, respectivement. De même, la pesée hydrostatique utilise le déplacement d'eau dû à un objet immergé pour déterminer la densité de l'objet.
Matériaux hétérogènes
Si le corps n'est pas homogène, alors sa densité varie entre les différentes régions de l'objet. Dans ce cas, la densité autour d'un emplacement donné est déterminée en calculant la densité d'un petit volume autour de cet emplacement. Dans la limite d'un volume infinitésimal la densité d'un objet inhomogène en un point devient : , où est un volume élémentaire à la position . La masse du corps peut alors être exprimée comme
Matériaux non compacts
En pratique, les matériaux en vrac tels que le sucre, le sable ou la neige contiennent des vides. De nombreux matériaux existent dans la nature sous forme de flocons, de pastilles ou de granulés.
Les vides sont des régions qui contiennent autre chose que le matériau considéré. Généralement, le vide est de l'air, mais il peut également s'agir d'un vide, d'un liquide, d'un solide ou d'un gaz ou d'un mélange gazeux différent.
Le volume en vrac d'un matériau, y compris la fraction de vide, est souvent obtenu par une simple mesure (par exemple avec une tasse à mesurer calibrée) ou géométriquement à partir de dimensions connues.
Masse divisée par masse volumique détermine la masse volumique apparente . Ce n'est pas la même chose que la masse volumique volumique.
Pour déterminer la masse volumique volumique, il faut d'abord actualiser le volume de la fraction de vide. Parfois, cela peut être déterminé par un raisonnement géométrique. Pour le compactage de sphères égales, la fraction non vide peut être au plus d'environ 74%. Elle peut également être déterminée empiriquement. Cependant, certains matériaux en vrac, tels que le sable, ont une fraction de vide variable qui dépend de la façon dont le matériau est agité ou versé. Il peut être lâche ou compact, avec plus ou moins d'espace d'air selon la manipulation.
En pratique, la fraction de vide n'est pas nécessairement aérienne, ni même gazeuse. Dans le cas du sable, il pourrait s'agir d'eau, ce qui peut être avantageux pour la mesure car la fraction de vide pour le sable saturé en eau - une fois que toutes les bulles d'air sont complètement chassées - est potentiellement plus cohérente que le sable sec mesuré avec un vide d'air.
Dans le cas de matériaux non compacts, il faut également veiller à déterminer la masse de l'échantillon de matériau. Si le matériau est sous pression (généralement la pression de l'air ambiant à la surface de la terre), la détermination de la masse à partir d'un poids d'échantillon mesuré peut devoir tenir compte des effets de flottabilité dus à la densité du constituant du vide, selon la façon dont la mesure a été effectuée. Dans le cas du sable sec, le sable est tellement plus dense que l'air que l'effet de flottabilité est généralement négligé (moins d'une partie sur mille).
Le changement de masse lors du déplacement d'un matériau vide par un autre tout en maintenant un volume constant peut être utilisé pour estimer la fraction de vide, si la différence de densité des deux matériaux vides est connue de manière fiable.
Changements de densité
En général, la densité peut être modifiée en changeant soit la pression, soit la température . L'augmentation de la pression augmente toujours la densité d'un matériau. L'augmentation de la température diminue généralement la densité, mais il existe des exceptions notables à cette généralisation. Par exemple, la densité de l' eau augmente entre son point de fusion à 0 °C et 4 °C ; un comportement similaire est observé dans le silicium à basse température.
L'effet de la pression et de la température sur les densités des liquides et des solides est faible. La compressibilité d'un liquide ou d'un solide typique est de 10 -6 bar -1 (1 bar = 0,1 MPa) et une expansivité thermique typique est de 10 -5 K -1 . Cela se traduit à peu près par le besoin d'environ dix mille fois la pression atmosphérique pour réduire le volume d'une substance d'un pour cent. (Bien que les pressions nécessaires puissent être environ mille fois plus faibles pour les sols sableux et certaines argiles.) Une expansion de 1 % du volume nécessite généralement une augmentation de la température de l'ordre de milliers de degrés Celsius .
En revanche, la densité des gaz est fortement affectée par la pression. La densité d'un gaz parfait est
où M est la masse molaire , P est la pression, R est la constante universelle des gaz et T est la température absolue . Cela signifie que la densité d'un gaz parfait peut être doublée en doublant la pression ou en réduisant de moitié la température absolue.
Dans le cas d'une dilatation thermique volumique à pression constante et à de petits intervalles de température, la dépendance de la température de la densité est :
où est la densité à une température de référence, est le coefficient de dilatation thermique du matériau à des températures proches de .
Densité des solutions
La densité d'une solution est la somme des concentrations massiques (massiques) des composants de cette solution.
La concentration en masse (massique) de chaque composant donné ρ i dans une solution s'additionne à la densité de la solution.
Exprimée en fonction des densités des composants purs du mélange et de leur participation volumique , elle permet la détermination des volumes molaires en excès :
à condition qu'il n'y ait pas d'interaction entre les composants.
Connaissant la relation entre les volumes excédentaires et les coefficients d'activité des composants, on peut déterminer les coefficients d'activité.
Densités
Divers matériaux
- Les éléments chimiques sélectionnés sont répertoriés ici. Pour les densités de tous les éléments chimiques, voir Liste des éléments chimiques
| Matériel | ρ (kg / m 3 ) | Remarques |
|---|---|---|
| Hydrogène | 0,0898 | |
| Hélium | 0,179 | |
| Aérographite | 0,2 | |
| Microréseau métallique | 0,9 | |
| Aérogel | 1,0 | |
| Air | 1.2 | Au niveau de la mer |
| Hexafluorure de tungstène | 12.4 | L'un des gaz les plus lourds connus dans des conditions standard |
| Hydrogène liquide | 70 | A env. −255 °C |
| polystyrène | 75 | Environ. |
| Liège | 240 | Environ. |
| Pin | 373 | |
| Lithium | 535 | Métal le moins dense |
| Bois | 700 | Assaisonné, typique |
| chêne | 710 | |
| Potassium | 860 | |
| La glace | 916,7 | A température < 0 °C |
| Huile de cuisson | 910-930 | |
| Sodium | 970 | |
| Eau (fraîche) | 1 000 | A 4 °C, la température de sa densité maximale |
| Eau (sel) | 1 030 | 3% |
| Oxygène liquide | 1 141 | A env. −219 °C |
| Nylon | 1 150 | |
| Plastiques | 1 175 | Environ.; pour polypropylène et PETE / PVC |
| Glycérol | 1 261 | |
| Tétrachloroéthène | 1 622 | |
| Sable | 1 600 | Entre 1600 et 2000 |
| Magnésium | 1 740 | |
| Béryllium | 1 850 | |
| Béton | 2 400 | |
| Un verre | 2500 | |
| Silicium | 2 330 | |
| Quartzite | 2 600 | |
| Granit | 2 700 | |
| Gneiss | 2 700 | |
| Aluminium | 2 700 | |
| Calcaire | 2 750 | Compact |
| Basalte | 3 000 | |
| Diiodométhane | 3 325 | Liquide à température ambiante |
| diamant | 3 500 | |
| Titane | 4 540 | |
| Sélénium | 4 800 | |
| Vanadium | 6 100 | |
| Antimoine | 6 690 | |
| Zinc | 7 000 | |
| Chrome | 7 200 | |
| Étain | 7 310 | |
| Manganèse | 7 325 | Environ. |
| Le fer | 7 870 | |
| Niobium | 8 570 | |
| Laiton | 8.600 | |
| Cadmium | 8.650 | |
| Cobalt | 8 900 | |
| Nickel | 8 900 | |
| Le cuivre | 8 940 | |
| Bismuth | 9 750 | |
| Molybdène | 10 220 | |
| Argent | 10 500 | |
| Mener | 11 340 | |
| Thorium | 11 700 | |
| Rhodié | 12.410 | |
| Mercure | 13 546 | |
| Tantale | 16 600 | |
| Uranium | 18 800 | |
| Tungstène | 19 300 | |
| Or | 19 320 | |
| Plutonium | 19 840 | |
| Rhénium | 21 020 | |
| Platine | 21 450 | |
| Iridium | 22 420 | |
| Osmium | 22 570 | Élément le plus dense |
| Remarques: | ||
Autres
| Entité | ρ (kg / m 3 ) | Remarques |
|---|---|---|
| Milieu interstellaire | 1 × 10 −19 | En supposant 90 % de H, 10 % de He ; variable T |
| La Terre | 5 515 | Densité moyenne. |
| Le noyau interne de la Terre | 13.000 | Env., comme indiqué dans Earth . |
| Le noyau du Soleil | 33 000 à 160 000 | Environ. |
| Un trou noir supermassif | 9 × 10 5 | La densité équivalente d'un trou noir de 4,5 millions de masse solaire Le rayon de l' horizon des événements est de 13,5 millions de km. |
| Étoile naine blanche | 2,1 × 10 9 | Environ. |
| Noyaux atomiques | 2,3 × 10 17 | Ne dépend pas fortement de la taille du noyau |
| Étoile à neutrons | 1 × 10 18 | |
| Trou noir de masse stellaire | 1 × 10 18 | La densité équivalente d'un trou noir de 4 masses solaires Le rayon de l' horizon des événements est de 12 km. |
L'eau
| Temp. (°C) | Densité (kg/m 3 ) |
|---|---|
| −30 | 983.854 |
| −20 | 993,547 |
| -10 | 998.117 |
| 0 | 999.8395 |
| 4 | 999.9720 |
| dix | 999.7026 |
| 15 | 999.1026 |
| 20 | 998.2071 |
| 22 | 997.7735 |
| 25 | 997.0479 |
| 30 | 995.6502 |
| 40 | 992.2 |
| 60 | 983.2 |
| 80 | 971.8 |
| 100 | 958,4 |
| Remarques: | |
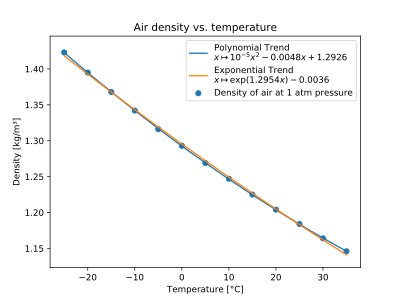
Air
| T (°C) | ρ (kg / m 3 ) |
|---|---|
| -25 | 1.423 |
| −20 | 1,395 |
| -15 | 1,368 |
| -10 | 1,342 |
| -5 | 1.316 |
| 0 | 1,293 |
| 5 | 1.269 |
| dix | 1,247 |
| 15 | 1.225 |
| 20 | 1.204 |
| 25 | 1.184 |
| 30 | 1.164 |
| 35 | 1,146 |
Volumes molaires des phases liquide et solide des éléments
Unités communes
L' unité SI pour la densité est :
- kilogramme par mètre cube (kg/m 3 )
Le litre et les tonnes métriques ne font pas partie du SI, mais peuvent être utilisés avec celui-ci, ce qui donne les unités suivantes :
- kilogramme par litre (kg/L)
- gramme par millilitre (g/mL)
- tonne métrique par mètre cube (t/m 3 )
Les densités utilisant les unités métriques suivantes ont toutes exactement la même valeur numérique, un millième de la valeur en (kg/m 3 ). L' eau liquide a une densité d'environ 1 kg/dm 3 , ce qui rend n'importe laquelle de ces unités SI numériquement pratique à utiliser car la plupart des solides et des liquides ont des densités comprises entre 0,1 et 20 kg/dm 3 .
- kilogramme par décimètre cube (kg/dm 3 )
- gramme par centimètre cube (g/cm 3 )
- 1 g/cm 3 = 1000 kg/m 3
- mégagramme (tonne métrique) par mètre cube (Mg/m 3 )
Aux États-Unis, la densité des unités usuelles peut être indiquée dans :
- Avoirdupois once par pouce cube (1 g/cm 3 ≈ 0.578036672 oz/cu in)
- Avoirdupois once par once liquide (1 g/cm 3 ≈ 1.04317556 oz/US fl oz = 1.04317556 lb/US fl pinte)
- Avoirdupois livre par pouce cube (1 g/cm 3 ≈ 0,036127292 lb/cu in)
- livre par pied cube (1 g/cm 3 ≈ 62,427961 lb/cu ft)
- livre par verge cube (1 g/cm 3 ≈ 1685,5549 lb/cu yd)
- livre par gallon liquide américain (1 g/cm 3 ≈ 8,34540445 lb/gal US)
- livre par boisseau américain (1 g/cm 3 ≈ 77.6888513 lb/bu)
- limace par pied cube
Les unités impériales différentes de ce qui précède (comme le gallon impérial et le boisseau diffèrent des unités américaines) sont rarement utilisées dans la pratique, bien que trouvées dans des documents plus anciens. Le gallon impérial était basé sur le concept qu'une once liquide impériale d'eau aurait une masse d'une once Avoirdupois, et en effet 1 g/cm 3 ≈ 1,00224129 onces par once liquide impériale = 10,0224129 livres par gallon impérial. La densité des métaux précieux pourrait éventuellement être basée sur les onces et les livres troy , une cause possible de confusion.
Connaissant le volume de la maille élémentaire d'un matériau cristallin et son poids de formule (en daltons ), la densité peut être calculée. Un dalton par cubique ångström est égale à une masse volumique de 1,660 539 066 60 g / cm 3 .
Voir également
- Densités des éléments (page de données)
- Liste des éléments par densité
- Densité de l'air
- Densité de surface
- Densité apparente
- Flottabilité
- Densité de charge
- Prédiction de densité par la méthode Girolami
- Dord
- Densité d'énergie
- Plus léger que l'air
- Densité linéaire
- Densité numérique
- Densité orthobarique
- Densité du papier
- Poids spécifique
- Épice (océanographie)
- Température et pression standard
Les références
Liens externes
- . Encyclopédie Britannica . 8 (11e éd.). 1911.
- . . 1914.
- Vidéo : Expérience de densité avec de l'huile et de l'alcool
- Vidéo : Expérience de densité avec du whisky et de l'eau
- Calcul de la densité du verre – Calcul de la densité du verre à température ambiante et du verre fondu à 1000 – 1400°C
- Liste des éléments du tableau périodique - triés par densité
- Calcul des densités de liquide saturé pour certains composants
- Test de densité de champ
- Eau – Densité et poids spécifique
- Dépendance de la température de la densité de l'eau – Conversions d'unités de densité
- Une délicieuse expérience de densité
- Calculateur de densité de l'eau Archivé le 13 juillet 2011 à la Wayback Machine Densité de l'eau pour une salinité et une température données.
- Calculateur de densité de liquide Sélectionnez un liquide dans la liste et calculez la densité en fonction de la température.
- La densité du gaz Calculateur densité Calcul d'un gaz en fonction de la température et de la pression.
- Densités de divers matériaux.
- Détermination de la densité du solide , instructions pour effectuer une expérience en classe.
- prédiction de densité
- prédiction de densité